



科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 分类标准 | 碱性氧化物 | 强电解质 | 含氧酸 | 非电解质 |
| 属于该类的物质 | ① | NaOH | ② | ③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
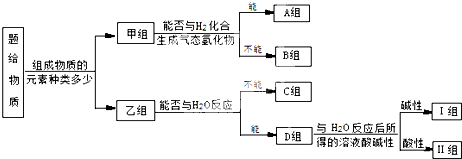
查看答案和解析>>
科目:高中化学 来源: 题型:
A、实验室制氨气:NH4++OH-
| ||||
| B、向NaHCO3溶液中滴入少量澄清的石灰水:2HCO3-+Ca2++2OH-═CaCO3↓+CO32-+2H2O | ||||
| C、酸性KMnO4溶液与H2O2反应:2MnO4-+3H2O2+6H+═2Mn2++4O2↑+6H2O | ||||
| D、碳酸钙与醋酸反应:CaCO3+2H+═Ca2++H2O+CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
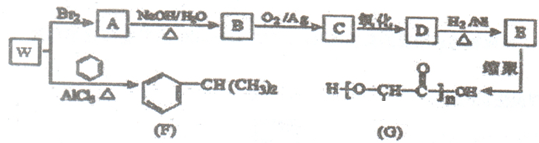
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①③⑤ | B、②④ |
| C、①③④⑤ | D、①②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、滴定管用水洗后,未用标准溶液润洗就装入标准溶液 |
| B、锥形瓶盛待测液前,用待测液润洗 |
| C、读数时,滴定前仰视,滴定后俯视 |
| D、滴定结束后,发现碱式滴定管尖嘴处悬挂一滴碱液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com