

 £¬DŹĒ
£¬DŹĒ £¬EŹĒ
£¬EŹĒ £¬GŹĒ
£¬GŹĒ £®
£® $\stackrel{“߻ƼĮ}{”ś}$
$\stackrel{“߻ƼĮ}{”ś}$ £®
£® £®
£® ·ÖĪö ±½ŗĶ¼×±½µÄijĶ¬ĻµĪļæÉ“ß»ÆČ„ĒāµĆµ½A£¬ŌņAÓ¦ĪŖĢž£¬1molijĢžA³ä·ÖČ¼ÉÕŗóæÉŅŌµĆµ½8molCO2ŗĶ4molH2O£¬¹ŹĢžAµÄ·Ö×ÓŹ½ĪŖC8H8£¬²»±„ŗĶ¶ČĪŖ$\frac{2”Į8+2-8}{2}$=5£¬æÉÄÜŗ¬ÓŠ±½»·£¬ÓÉA·¢Éś¼Ó¾Ū·“Ӧɜ³ÉC£¬¹ŹAÖŠŗ¬ÓŠ²»±„ŗĶ¼ü£¬¹ŹAĪŖ £¬A¼Ó¾ŪµĆBĪŖ
£¬A¼Ó¾ŪµĆBĪŖ £¬AÓėäå·¢Éś¼Ó³É·“Ӧɜ³ÉE£¬EĪŖ
£¬AÓėäå·¢Éś¼Ó³É·“Ӧɜ³ÉE£¬EĪŖ £¬EŌŚĒāŃõ»ÆÄĘ“¼ČÜŅŗ”¢¼ÓČČĢõ¼žĻĀ·¢ÉśĻūČ„·“Ӧɜ³ÉF£¬FĪŖ
£¬EŌŚĒāŃõ»ÆÄĘ“¼ČÜŅŗ”¢¼ÓČČĢõ¼žĻĀ·¢ÉśĻūČ„·“Ӧɜ³ÉF£¬FĪŖ £¬øł¾ŻGµÄ·Ö×ÓŹ½æÉÖŖ£¬FÓėäå·¢Éś¼Ó³É·“Ӧɜ³ÉGĪŖ
£¬øł¾ŻGµÄ·Ö×ÓŹ½æÉÖŖ£¬FÓėäå·¢Éś¼Ó³É·“Ӧɜ³ÉGĪŖ £¬CŌŚÅØĒāŃõ»ÆÄĘ“¼ČÜŅŗÖŠÉś³ÉA£¬ĒŅC¼īŠŌĖ®½āµĆD£¬øł¾Ż
£¬CŌŚÅØĒāŃõ»ÆÄĘ“¼ČÜŅŗÖŠÉś³ÉA£¬ĒŅC¼īŠŌĖ®½āµĆD£¬øł¾Ż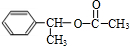 µÄ½į¹¹æÉÖŖ£¬CĪŖ
µÄ½į¹¹æÉÖŖ£¬CĪŖ £¬DĪŖ
£¬DĪŖ £¬AÓė1£¬3-¶”¶žĻ©·¢Éś¼Ó¾Ū·“Ó¦µĆ¶”±½Ļš½ŗĪŖ£ŗ
£¬AÓė1£¬3-¶”¶žĻ©·¢Éś¼Ó¾Ū·“Ó¦µĆ¶”±½Ļš½ŗĪŖ£ŗ £¬¾Ż“Ė“šĢā£»
£¬¾Ż“Ė“šĢā£»
½ā“š ½ā£ŗ±½ŗĶ¼×±½µÄijĶ¬ĻµĪļæÉ“ß»ÆČ„ĒāµĆµ½A£¬ŌņAÓ¦ĪŖĢž£¬1molijĢžA³ä·ÖČ¼ÉÕŗóæÉŅŌµĆµ½8molCO2ŗĶ4molH2O£¬¹ŹĢžAµÄ·Ö×ÓŹ½ĪŖC8H8£¬²»±„ŗĶ¶ČĪŖ$\frac{2”Į8+2-8}{2}$=5£¬æÉÄÜŗ¬ÓŠ±½»·£¬ÓÉA·¢Éś¼Ó¾Ū·“Ӧɜ³ÉC£¬¹ŹAÖŠŗ¬ÓŠ²»±„ŗĶ¼ü£¬¹ŹAĪŖ £¬A¼Ó¾ŪµĆBĪŖ
£¬A¼Ó¾ŪµĆBĪŖ £¬AÓėäå·¢Éś¼Ó³É·“Ӧɜ³ÉE£¬EĪŖ
£¬AÓėäå·¢Éś¼Ó³É·“Ӧɜ³ÉE£¬EĪŖ £¬EŌŚĒāŃõ»ÆÄĘ“¼ČÜŅŗ”¢¼ÓČČĢõ¼žĻĀ·¢ÉśĻūČ„·“Ӧɜ³ÉF£¬FĪŖ
£¬EŌŚĒāŃõ»ÆÄĘ“¼ČÜŅŗ”¢¼ÓČČĢõ¼žĻĀ·¢ÉśĻūČ„·“Ӧɜ³ÉF£¬FĪŖ £¬øł¾ŻGµÄ·Ö×ÓŹ½æÉÖŖ£¬FÓėäå·¢Éś¼Ó³É·“Ӧɜ³ÉGĪŖ
£¬øł¾ŻGµÄ·Ö×ÓŹ½æÉÖŖ£¬FÓėäå·¢Éś¼Ó³É·“Ӧɜ³ÉGĪŖ £¬CŌŚÅØĒāŃõ»ÆÄĘ“¼ČÜŅŗÖŠÉś³ÉA£¬ĒŅC¼īŠŌĖ®½āµĆD£¬øł¾Ż
£¬CŌŚÅØĒāŃõ»ÆÄĘ“¼ČÜŅŗÖŠÉś³ÉA£¬ĒŅC¼īŠŌĖ®½āµĆD£¬øł¾Ż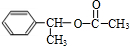 µÄ½į¹¹æÉÖŖ£¬CĪŖ
µÄ½į¹¹æÉÖŖ£¬CĪŖ £¬DĪŖ
£¬DĪŖ £¬AÓė1£¬3-¶”¶žĻ©·¢Éś¼Ó¾Ū·“Ó¦µĆ¶”±½Ļš½ŗĪŖ£ŗ
£¬AÓė1£¬3-¶”¶žĻ©·¢Éś¼Ó¾Ū·“Ó¦µĆ¶”±½Ļš½ŗĪŖ£ŗ £¬
£¬
£Ø¢ń£©ŅŌÉĻ11øö·“Ó¦ÖŠ£¬ŹōÓŚĻūČ„·“Ó¦µÄÓŠ 2øö£¬ĖüĆĒ·Ö±šŹĒ£ŗÓŠC”śA£¬E”śF£¬
¹Ź“š°øĪŖ£ŗ2£»E”śF£»
£Ø¢ņ£©øł¾ŻÉĻĆęµÄ·ÖĪöæÉÖŖ£¬AĪŖ £¬DĪŖ
£¬DĪŖ £¬EĪŖ
£¬EĪŖ £¬GĪŖ
£¬GĪŖ £¬
£¬
¹Ź“š°øĪŖ£ŗ £»
£» £»
£» £»
£» £»
£»
£Ø¢ó£©A”śBµÄ»Æѧ·½³ĢŹ½ĪŖn $\stackrel{“߻ƼĮ}{”ś}$
$\stackrel{“߻ƼĮ}{”ś}$ £¬
£¬
¹Ź“š°øĪŖ£ŗn $\stackrel{“߻ƼĮ}{”ś}$
$\stackrel{“߻ƼĮ}{”ś}$ £»
£»
£Ø¢ō£©øł¾ŻÉĻĆęµÄ·ÖĪöæÉÖŖ£¬¶”±½Ļš½ŗµÄ½į¹¹¼ņŹ½ĪŖ £¬
£¬
¹Ź“š°øĪŖ£ŗ £®
£®
µćĘĄ ±¾Ģāæ¼²éÓŠ»śĶʶĻÓėŗĻ³É£¬Éę¼°Ļ©Ģž”¢Ā±“śĢž”¢“¼µČŠŌÖŹŅŌ¼°Ń§Éśøł¾ŻŠÅĻ¢øųÓč»ńČ”ÖŖŹ¶µÄÄÜĮ¦£¬ŹĒ¶ŌÓŠ»ś»ÆŗĻĪļÖŖŹ¶µÄ×ŪŗĻ漲飬ÄܽĻŗƵÄæ¼²éæ¼ÉśµÄŌĶĮ”¢×ŌѧÄÜĮ¦ŗĶĖ¼Ī¬ÄÜĮ¦£¬ĶʶĻ³öAµÄ·Ö×ÓŹ½øł¾Ż·“Ó¦Ģõ¼ž¼°·“Ó¦ĄąŠĶ£¬ĄūÓĆĖ³ĶĘ·Ø½ųŠŠĶʶĻ£¬ŹĒøßæ¼ČȵćĢāŠĶ£¬ÄѶČÖŠµČ£®


 Č«ÄܲāæŲĘŚÄ©Š”דŌŖĻµĮŠ“š°ø
Č«ÄܲāæŲĘŚÄ©Š”דŌŖĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
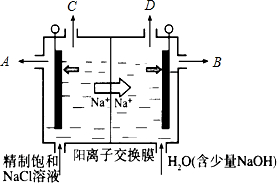 ¶žŃõ»ÆĀČ£ØClO2£©ÕżÖš²½“śĢęCl2³ÉĪŖ¹«ČĻµÄøߊ§”¢¹ćĘ×”¢°²Č«µÄĖ®“¦Ąķ¼Į£®µ±×ŌĄ“Ė®³§ÓĆClO2“¦ĄķŗóĖ®ÖŠŗ¬ClO2ŌŚ0.1”«0.8mg•L-1Ö®¼äŹ±£¬¼““ļµ½ŗĻøń±ź×¼£®
¶žŃõ»ÆĀČ£ØClO2£©ÕżÖš²½“śĢęCl2³ÉĪŖ¹«ČĻµÄøߊ§”¢¹ćĘ×”¢°²Č«µÄĖ®“¦Ąķ¼Į£®µ±×ŌĄ“Ė®³§ÓĆClO2“¦ĄķŗóĖ®ÖŠŗ¬ClO2ŌŚ0.1”«0.8mg•L-1Ö®¼äŹ±£¬¼““ļµ½ŗĻøń±ź×¼£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŌŚK2SO4ÓėBaCl2Į½ČÜŅŗ·“Ó¦Ź±£¬Ōö“óŃ¹Ēæ | |
| B£® | ¼ī½šŹōCsÓėĖ®·“Ó¦Ź±Ōö“óĖ®µÄÓĆĮæ | |
| C£® | FeÓėĻ”ĮņĖį·“Ó¦ÖĘČ”ĒāĘųŹ±£¬øÄÓĆÅØĮņĖį | |
| D£® | AlÓėŃĪĖį·“Ó¦£¬¼Ó¼øµĪĀČ»ÆĶČÜŅŗ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
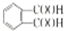 £®
£®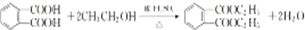 £®
£® £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĘūÓĶ | B£® | “æÖ²ĪļÓĶ | C£® | ÕįĢĒ | D£® | ¾ŪŅŅĻ© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ąė×Ó»ÆŗĻĪļÖŠÖ»ÄÜŗ¬Ąė×Ó¼ü£¬²»ÄÜÓŠ¹²¼Ū¼ü | |
| B£® | ĖłÓŠ·Ē½šŹōÖ®¼äŠĪ³ÉµÄ»Æѧ¼üŅ»¶ØŹĒ¹²¼Ū¼ü | |
| C£® | µē×ÓŹżĻąĶ¬µÄĮ½ÖÖĪ¢Į£Ņ»¶ØŹĒĶ¬Ņ»ŌŖĖŲ | |
| D£® | »Æѧ±ä»ÆŅ»¶ØÓŠ»Æѧ¼üµÄ¶ĻĮŃŗĶŠĪ³É |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com