
����Ŀ�����淴Ӧ��X(g)+2Y(g)![]() 2Z(g)��2M(g)
2Z(g)��2M(g)![]() N(g)+P(g)�ֱ����ܱ�������������Ӧ���н��У���Ӧ��֮������Ħ�����ɻ������ܱո��塣��Ӧ��ʼ�ʹﵽƽ��״̬ʱ�й��������ı仯��ͼ��ʾ(�������෴Ӧ���¶���ͬ)�������ж���ȷ���ǣ�
N(g)+P(g)�ֱ����ܱ�������������Ӧ���н��У���Ӧ��֮������Ħ�����ɻ������ܱո��塣��Ӧ��ʼ�ʹﵽƽ��״̬ʱ�й��������ı仯��ͼ��ʾ(�������෴Ӧ���¶���ͬ)�������ж���ȷ���ǣ�
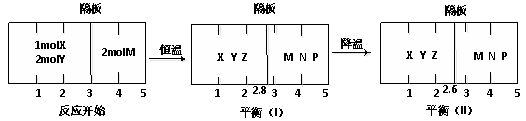
A����Ӧ��������Ӧ�����ȷ�Ӧ
B����ƽ��(I)ʱ��ϵ��ѹǿ�뷴Ӧ��ʼʱ��ϵ��ѹǿ֮��Ϊ14:15
C����ƽ��(I)ʱX��ת����Ϊ5/11
D����ƽ��(I)��ƽ��(II)��M�����������ͬ
���𰸡�C
��������
���������A��������ƽ��(��)��ƽ��(��)�ƶ���ͬʱX��Y��Z�������ʵ������٣�˵��ƽ�������ƶ�������Ӧ���ȣ���A����B��ƽ��ʱ���ұ����ʵ������䣬��ͼ���Կ�����ƽ��(��)ʱ��ϵ��ѹǿ�뷴Ӧ��ʼʱ��ϵ��ѹǿ֮��Ϊ��![]() =
=![]() ����B����C����ƽ��(��)ʱ���ұ���������ʵ������䣬��Ϊ2mol����������ѹǿ��ȣ���ƽ��ʱ�����������ʵ���Ϊxmol�����У�
����B����C����ƽ��(��)ʱ���ұ���������ʵ������䣬��Ϊ2mol����������ѹǿ��ȣ���ƽ��ʱ�����������ʵ���Ϊxmol�����У�![]() =
=![]() ��x=
��x=![]() mol�������ʵ���������3-
mol�������ʵ���������3-![]() =
=![]() mol�����Դ�ƽ��(��)ʱ��X��ת����Ϊ
mol�����Դ�ƽ��(��)ʱ��X��ת����Ϊ![]() ����C��ȷ��D����ƽ��(��)��ƽ��(��)����ѧ��Ӧ�������ƶ���M���������������ȵģ���D������ѡC��
����C��ȷ��D����ƽ��(��)��ƽ��(��)����ѧ��Ӧ�������ƶ���M���������������ȵģ���D������ѡC��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��U��V��W��X��Y��Z��ԭ������������������ֳ���Ԫ�أ�Y�ĵ�����W2��ȼ�յIJ����ʹƷ����Һ��ɫ��Z��WԪ���γɵĻ�����Z3W4���д��ԣ�U�ĵ�����W2��ȼ�տ�����UW��UW2�������塣X�ĵ�����һ�ֽ������ý�����UW2�о���ȼ�����ɺڡ������ֹ��塣
��ش��������⣺
��1��X�����ڱ��е�λ��Ϊ______��UW2�ĵ���ʽΪ______��X��UW2�о���ȼ�����ɵĺڡ������ֹ����л�ѧ������������______��______��
��2��U��V��W�γɵ�10�����⻯���У����ȶ�����______��д��ѧʽ����ͬ�����е���ߵ���______�����H+������ǿ���ǣ�д��ѧʽ��______��
��3��Z3W4��ϡ���ᷴӦ�����ӷ���ʽΪ______��
��4��YW2����ͨ��BaCl2��HNO3�Ļ����Һ�����ɰ�ɫ��������ɫ����VW���йط�Ӧ�����ӷ���ʽΪ______���ɴ˿�֪VW��YW2��ԭ�Խ�ǿ���ǣ�д��ѧʽ��______��
��5����֪YW2��Cl2����ʹƷ����Һ��ɫ���ֽ�һ������YW2��Cl2ͨ��Ʒ����Һ�У�
����Ʒ�첻��ɫ����Ʒ����Һ���������Ļ�ѧ����ʽΪ______��
����Ʒ����ɫ��Ϊ֤��YW2��Cl2˭��������IJ�������������______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��K2SO4���������ʼطʣ�Mn3O4������������������ϵ���Ҫԭ�ϡ������Ṥ ҵ��β�������Ʊ�K2SO4��Mn3O4�Ĺ����������£�
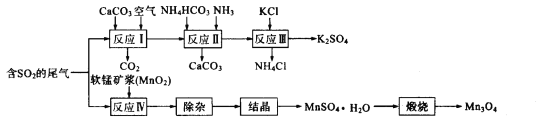

��1�������ε��ܽ�ȼ���ͼ����Ӧ���У���NH4��2SO4��Һ�м���KCl��Һ��ַ�Ӧ��������Ũ����________________��ϴ�ӡ�����Ȳ�������K2SO4��Ʒ��
��2������K2SO4��Ʒ�Ƿ����Ȼ������ʵ�ʵ�������___________________��
��3����Ӧ���Ļ�ѧ����ʽΪ_______________________��
��4��Mn3O4��Ũ�������ʱ������Ӧ�����ӷ���ʽΪ____________________��
��5����ͼ����MnSO4��H2Oʱ�¶���ʣ����������仯���ߡ�
����������B������ʾ���ʵĻ�ѧʽΪ_____________________��
�����չ����й����̺������¶ȵ����߶��������¶ȳ���1000��ʱ������ȴ��ò�������̺���������С���Է����������̺�����С��ԭ��____________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��G�Ǽ������ķ������ģ�ͣ��ݴ˻ش��������⣺

��1�������º�̼����ߵ���̬����________(���Ӧ��ĸ)��
��2���ܹ������ӳɷ�Ӧ������________(������)�֡�
��3��һ±��������������________(���Ӧ��ĸ)��
��4��д��C����ˮ��Ӧ�Ļ�ѧ����ʽ��______________________��
��5��д��F���������Ӧ�Ļ�ѧ����ʽ��____________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ȼ�ϵ�ʹ�úͷ���Ⱦ����ᷢչ��һ�����رܵ�ì�ܻ��⡣
��1���ҹ�����������ú��ů�������ķ�������������Ҫ��Դ֮һ�����о����ֽ�ú̿��O2/CO2��������ȼ�գ��ܹ�����ȼúʱNO���ŷţ���Ҫ��ӦΪ��2NO��g��+2CO��g���TN2��g��+2CO2��g�� ��H
����N2��g��+O2��g���T2NO��g�� ��H1=+180.5 kJ��mol��1
��CO��g���TC��s��+![]() O2��g�� ��H2=+110.5 kJ��mol��1
O2��g�� ��H2=+110.5 kJ��mol��1
��C��s��+O2��g���TCO2��g�� ��H3=��393.5 kJ��mol��1
���H= kJ��mol��1��
��2���״����Բ���Ͳ������ʯ��ȼ��,������Դ���š�һ��������,���ݻ�ΪVL���ܱ������г���a molCO��2a mol H2�ϳɼ״���COƽ��ת�������¶ȡ�ѹǿ�Ĺ�ϵ��ͼ��ʾ��
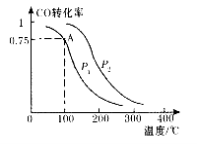
��P1�� P2(����� ����<�� ��=�� ),������
�ڸü״��ϳɷ�Ӧ��A���ƽ�ⳣ��K= (��a��V��ʾ)��
�����д�ʩ���ܹ�ͬʱ��������Ӧ���ʺ����COת���ʵ��� ��(��д��Ӧ��ĸ)
a��ʹ�ø�Ч���� b�����ͷ�Ӧ�¶� c��������ϵѹǿ
d�����Ͻ�CH3OH�ӷ�Ӧ������з������ e�����ӵ����ʵ�����CO��H2
��3����������β��Ҳ�������γɵ�ԭ��֮һ��

�ٽ�������������ڴ���������,���������лӷ�������C3H6����ԭβ���е�NO����������������Ⱦ�����ʡ���д���ù��̵Ļ�ѧ����ʽ�� ��
�ڵ绯ѧ�������������Dzⶨ����β�����õķ���֮һ������CO�������Ĺ���ԭ������ͼ��ʾ�������缫�ķ�ӦʽΪ ��
��4����ҵ�Ͽ�����NaOH��Һ��ˮ���չ�����SO2���ֱ�����NaHSO3��NH4HSO3����ˮ��Һ�������ԡ���ͬ�����£�ͬŨ�ȵ�������ʽ�ε�ˮ��Һ��c��SO32-����С���� �������ֺͻ�ѧ�������ԭ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�����͵��Ҵ���أ����û����������ܼ�������ܷ�ӦΪ��C2H5OH +3O2�� 2CO2+3H2O,���ʾ����ͼ,����˵����ȷ����
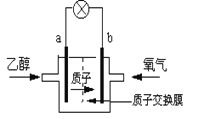
A. a��Ϊ��ص�����
B. ��ع���ʱ������a���ص��߾������ٵ�b��
C. ��ظ����ĵ缫��ӦΪ��4H++ O2+ 4e��= 2H2O
D. ��ع���ʱ,1mol�Ҵ�������ʱ����12mol����ת��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ͻ�������Ͼ�����������������ܣ���������ܵĿ���������Ҫ����
��1��һ���¶��£�ij����Ͻ�M�������������ͼ��ʾ������Ϊƽ��ʱ������ѹǿ��p���������ʾ��������ԭ�������ԭ�ӵĸ����ȣ�H/M������OA�Σ����ܽ���M���γɹ�����MHx����������ѹǿ������H/M���������AB�Σ�MHx�����������⻯��Ӧ�����⻯��MHy���⻯��Ӧ����ʽΪ��zMHx(s)+ H![]() (g)==zMHy(s) ��H(��)����B�㣬�⻯��Ӧ��������һ����������ѹǿ��H/M�������䡣��Ӧ������z=_____���ú�x��y�Ĵ���ʽ��ʾ�����¶�ΪT1ʱ��2gij�Ͻ�4min����������240mL����������v=______mLg-1min-1����Ӧ���ʱ��H(��)_____0���>����<����=����
(g)==zMHy(s) ��H(��)����B�㣬�⻯��Ӧ��������һ����������ѹǿ��H/M�������䡣��Ӧ������z=_____���ú�x��y�Ĵ���ʽ��ʾ�����¶�ΪT1ʱ��2gij�Ͻ�4min����������240mL����������v=______mLg-1min-1����Ӧ���ʱ��H(��)_____0���>����<����=����
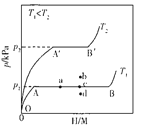
��2���DZ�ʾ��λ��������Ͻ����⻯��Ӧ�ε����������ռ�����������ı��������¶�ΪT1��T2ʱ���ǣ�T1��____ �ǣ�T2�����>����<����=����������Ӧ������ͼ��a��ʱ�������¶Ȳ��䣬�������ϵ��ͨ�������������ﵽƽ���Ӧ�����ܴ���ͼ�е�_____�㣨�b����c����d������������Ͻ��ͨ��________��________�ķ�ʽ�ͷ�������
��3������Ͻ�ThNi5�ɴ���CO��H![]() �ϳ�CH
�ϳ�CH![]() �ķ�Ӧ���¶�ΪTʱ���÷�Ӧ���Ȼ�ѧ����ʽΪ_______ ����֪�¶�ΪTʱ��CH
�ķ�Ӧ���¶�ΪTʱ���÷�Ӧ���Ȼ�ѧ����ʽΪ_______ ����֪�¶�ΪTʱ��CH![]() (g)+2H2O=CO
(g)+2H2O=CO![]() (g)+4H
(g)+4H![]() (g) ��H=+165KJmol1
(g) ��H=+165KJmol1
CO(g)+H2O(g)=CO![]() (g)+H
(g)+H![]() (g) ��H=-41KJmol1
(g) ��H=-41KJmol1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����2L�ܱ������ڣ�800 ��ʱ��Ӧ2NO(g)��O2(g)![]() 2NO2(g)��ϵ�У�n(NO)��ʱ��ı仯�����
2NO2(g)��ϵ�У�n(NO)��ʱ��ı仯�����
ʱ��(s) | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
��1����ͼ��ʾNO2�ı仯��������________����O2��ʾ��0��2 s�ڸ÷�Ӧ��ƽ������v��________���ﵽƽ��ʱNO��ת����Ϊ_______

��2����˵���÷�Ӧ�Ѵﵽƽ��״̬����________(����ĸ��ţ���ͬ)��
A��v (NO2)��2v(O2) B��������ѹǿ���ֲ���
C��v��(NO)��2v��(O2) D���������ܶȱ��ֲ���
��3��Ϊʹ�÷�Ӧ�ķ�Ӧ�����������д�ʩ��ȷ����________��
A������������� B���ʵ������¶�
C������O2��Ũ�� D��ѡ���Ч����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����Ļ����������������й㷺���ڡ�
��1�����Ȱ���NH2Cl���ĵ���ʽΪ ����ͨ����ӦNH3(g)��Cl2(g)=NH2Cl(g)��HCl(g)�Ʊ��Ȱ�����֪���ֻ�ѧ���ļ�����������ʾ���ٶ���ͬ������ͬ�ֻ�ѧ���ļ���һ��������������Ӧ�Ħ�H= ��

��NH2Cl��ˮ��Ӧ����ǿ�����Ե����ʣ�������Ч�������������÷�Ӧ�Ļ�ѧ����ʽΪ ��
��2���ý�̿��ԭNO�ķ�ӦΪ��2NO(g)+C(s) ![]() N2(g)+CO2(g)�����ݻ���Ϊ1 L�ļס��ҡ����������ݺ��£���Ӧ�¶ȷֱ�Ϊ400�桢400�桢T���������зֱ���������Ľ�̿��һ������NO����ø�������n(NO)�淴Ӧʱ��t�ı仯������±���ʾ��
N2(g)+CO2(g)�����ݻ���Ϊ1 L�ļס��ҡ����������ݺ��£���Ӧ�¶ȷֱ�Ϊ400�桢400�桢T���������зֱ���������Ľ�̿��һ������NO����ø�������n(NO)�淴Ӧʱ��t�ı仯������±���ʾ��

���÷�ӦΪ ������ȡ������ȡ�����Ӧ��
����������200 min�ﵽƽ��״̬����0��200 min����NO��Ũ�ȱ仯��ʾ��ƽ����Ӧ����v(NO)= ��
��3���ý�̿��ԭNO2�ķ�ӦΪ��2NO2(g)+2C(s)![]() N2(g)+2CO2(g)���ں��������£�1 mol NO2������C�����÷�Ӧ�����ƽ��ʱNO2��CO2�����ʵ���Ũ����ƽ����ѹ�Ĺ�ϵ��ͼ��ʾ��
N2(g)+2CO2(g)���ں��������£�1 mol NO2������C�����÷�Ӧ�����ƽ��ʱNO2��CO2�����ʵ���Ũ����ƽ����ѹ�Ĺ�ϵ��ͼ��ʾ��
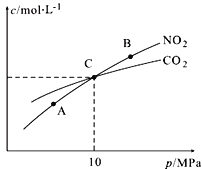
��A��B�����Ũ��ƽ�ⳣ����ϵ��Kc(A) Kc(B)�������������=������
��A��B��C������NO2��ת������ߵ��� ������A������B������C��������
�ۼ���C��ʱ�÷�Ӧ��ѹǿƽ�ⳣ��Kp(C)= ��Kp����ƽ���ѹ����ƽ��Ũ�ȼ��㣬��ѹ����ѹ�����ʵ�����������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com