
| A. | PH3 | B. | H2S | C. | HBr | D. | HCl |
分析 形成共用电子对的两元素的非金属性强弱相差越大,共价键的极性越强,选项中都是H原子分别与P、S、Br、Cl原子形成的极性键,可以根据与P、S、Br、Cl的非金属性判断键的极性最强.
解答 解:由于形成共用电子对的两元素的非金属性强弱相差越大,形成的共价键的极性越强;选项中都是H原子分别与P、S、Br、Cl原子形成的极性键,可以根据与P、S、Br、Cl的非金属性判断键的极性最强.其它元素的非金属性大小关系为:Cl>Br>S>P,所以极性键的极性大小关系为Cl-H>Br-H>S-H>P-H,
故选D.
点评 本题考查了键的极性强弱判断,题目难度不大,侧重对学生灵活运用基础知识解决实际问题的能力的培养,注意形成共用电子对的两元素的非金属性强弱相差越大,共价键的极性越强.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 →
→ .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ①②③④ | C. | ①②③④⑤ | D. | ①②③④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 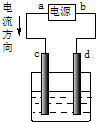 c为阳极,d为阴极 | |
| B. | 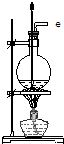 用于实验室蒸馏石油 | |
| C. | 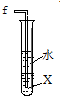 X为CCl4时,可用于吸收氯化氢气体,并防止倒吸 | |
| D. | 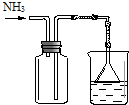 用于收集氨气及并进行尾气吸收 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 家庭装修用的材料能释放出对人体健康有害的物质主要是甲醛 | |
| B. | 工业上用银镜反应来制镜或保温瓶胆 | |
| C. | 工业酒精因含有毒的甲醇,饮后会使人眼睛失明甚至死亡,所以不能饮用 | |
| D. | 生活中的饮料、糖果等常使用芳香族化合物做香料 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
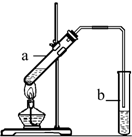
| A. | 向a试管中先加入浓硫酸,然后边摇动试管边慢慢加入乙醇,再加冰醋酸 | |
| B. | 用CH3CH218OH与乙酸反应制取乙酸乙酯,18O 存在于水中 | |
| C. | 试管b中的液体是饱和NaHCO3溶液 | |
| D. | 实验时加热试管a的目的之一是及时将乙酸乙酯蒸出,使平衡向生成乙酸乙酯的方向移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | S(s)在O2(g)中燃烧的反应是放热反应 | |
| B. | 16 g固体硫在空气中充分燃烧,可吸收148.6 kJ的热量 | |
| C. | 1 mol SO2(g)所具有的能量低于1 mol S(s)与1 mol O2(g)所具有的能量之和 | |
| D. | S(g)+O2(g)═SO2(g)△H=b kJ•mol-1,则a>b |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验步骤 | 1.将一小块金属钠放入滴有酚酞溶液的冷水中 2.将一小段用砂纸打磨后的镁带放入试管中,加入少量水,加热至水沸腾,冷却后,向试管中滴加酚酞溶液 3.将一小段镁带投入稀盐酸中 4.将一小片铝投入稀盐酸中 |
| 实验现象 | ①剧烈反应,迅速生成大量的气体 ②浮在水面上,熔成小球,不断游动,小球渐小最终消失,溶液变红 ③反应不剧烈,产生无色气体 ④有气体产生,溶液变成红色 |
| 实验步骤 | 1 | 2 | 3 | 4 |
| 实验现象 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com