
”¾ĢāÄæ”æ±ź×¼×“æöĻĀV L°±ĘųČܽāŌŚ1 LĖ®ÖŠ(Ė®µÄĆÜ¶Č½üĖĘĪŖ1 g/mL)£¬ĖłµĆČÜŅŗµÄĆܶČĪŖ¦Ń g/mL£¬ÖŹĮæ·ÖŹżĪŖ¦Ų£¬ĪļÖŹµÄĮæÅضČĪŖc mol/L£¬ŌņĻĀĮŠ¹ŲĻµÖŠ²»ÕżČ·µÄŹĒ(””””)
A. ¦Ń£½(17V£«22 400)/(22.4£«22.4V)
B. ¦Ų£½17c/(1 000¦Ń)
C. ¦Ų£½17V/(17V£«22 400)
D. c£½1 000V¦Ń/(17V£«22 400)
”¾“š°ø”æC
”¾½āĪö”æA”¢ÓɦŃ=(17V+22400)/(22.4+22.4V)æÉÖŖ£¬øĆČÜŅŗµÄĆܶČ=![]() £¬µ«Źµ¼ŹÉĻČÜŅŗĢå»ż²»µČÓŚ°±ĘųĢå»żÓėĖ®µÄĢå»żÖ®ŗĶ£¬¹ŹA“ķĪó£»
£¬µ«Źµ¼ŹÉĻČÜŅŗĢå»ż²»µČÓŚ°±ĘųĢå»żÓėĖ®µÄĢå»żÖ®ŗĶ£¬¹ŹA“ķĪó£»
B”¢ÓÉc=![]() æÉÖŖ£¬w%=17c/(1000¦Ń)¶ų²»ŹĒw=17c/(1000¦Ń)£¬¹ŹB“ķĪó£»
æÉÖŖ£¬w%=17c/(1000¦Ń)¶ų²»ŹĒw=17c/(1000¦Ń)£¬¹ŹB“ķĪó£»
C”¢°±ĘųµÄĪļÖŹµÄĮæĪŖn£ØNH3£©= ![]() =
=![]() mol£¬¹Ź°±ĘųµÄÖŹĮæĪŖ
mol£¬¹Ź°±ĘųµÄÖŹĮæĪŖ![]() mol”Į17g/mol=
mol”Į17g/mol=![]() g£¬1LĖ®µÄÖŹĮæĪŖ1000g£¬¹ŹøĆČÜŅŗµÄÖŹĮæ·ÖŹżĪŖw%=£Ø
g£¬1LĖ®µÄÖŹĮæĪŖ1000g£¬¹ŹøĆČÜŅŗµÄÖŹĮæ·ÖŹżĪŖw%=£Ø![]() £©”Ā£Ø
£©”Ā£Ø![]() g+1000g£©”Į100%=
g+1000g£©”Į100%=![]() £¬¹ŹC“ķĪó£»
£¬¹ŹC“ķĪó£»
D”¢ÓÉC·ÖĪöæÉÖŖ“ĖČÜŅŗµÄÖŹĮæ·ÖŹżĪŖw%=![]() £¬¹Źc=
£¬¹Źc=![]() =
=![]() =
=
=![]() £¬¹ŹDÕżČ·£»
£¬¹ŹDÕżČ·£»
“ĖĢā“š°øŃ”D


 ĆæČÕ10·ÖÖÓæŚĖćŠÄĖćĖŁĖćĢģĢģĮ·ĻµĮŠ“š°ø
ĆæČÕ10·ÖÖÓæŚĖćŠÄĖćĖŁĖćĢģĢģĮ·ĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”涞Ńõ»Æīę£ØCeO2£©ŹĒŅ»ÖÖÖŲŅŖµÄĻ”ĶĮŃõ»ÆĪļ”£Ę½°åµēŹÓĻŌŹ¾ĘĮÉś²ś¹ż³ĢÖŠ²śÉś“óĮæµÄ·Ļ²£ Į§·ŪÄ©£Øŗ¬SiO2”¢Fe2O3”¢CeO2µČĪļÖŹ£©”£Ä³æĪĢāŠ”×éŅŌ“Ė·ŪÄ©ĪŖŌĮĻ£¬Éč¼Ę׏Ō“»ŲŹÕµÄ¹¤ŅÕĮ÷³ĢČēĻĀ£ŗ 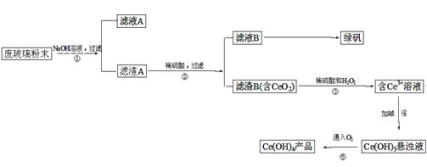
£Ø1£©Š“³öµŚ¢Ł²½·“Ó¦µÄĄė×Ó·½³ĢŹ½”£
£Ø2£©Ļ“µÓĀĖŌüBµÄÄæµÄŹĒĪŖĮĖ³żČ„£ØĢīĄė×Ó·ūŗÅ£©£¬¼ģŃéøĆĄė×ÓŹĒ·ńĻ“¾»µÄ·½·ØŹĒ”£
£Ø3£©Š“³öµŚ¢Ū²½·“Ó¦µÄ»Æѧ·½³ĢŹ½”£
£Ø4£©ÖʱøĀĢ·Æ(FeSO4”¤7H2O)Ź±£¬ĻņFe2(SO4)3ČÜŅŗÖŠ¼ÓČė¹żĮæĢśŠ¼£¬³ä·Ö·“Ó¦ŗ󣬾¹żĀĖµĆµ½FeSO4ČÜŅŗ£¬ŌŁ¾”¢”¢¹żĀĖ”¢Ļ“µÓ”¢øÉŌļµČ²Ł×÷²½ÖčµĆµ½ĀĢ·Æ”£
£Ø5£©Č”ÉĻŹöĮ÷³ĢÖŠµĆµ½µÄCe(OH)4²śĘ·(ÖŹĮæ·ÖŹżĪŖ86%)1.000g£¬¼ÓĮņĖįČܽāŗó£¬ÓĆ0.1000mol/L FeSO4ČÜŅŗµĪ¶ØÖĮÖÕµć£Øīę±»»¹Ō³ÉCe3+£©£¬ŌņŠč×¼Č·µĪ¼Ó±ź×¼ČÜŅŗµÄĢå»żĪŖmL”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠµē×ÓÅŲ¼Ź½²»Źō»łĢ¬µÄŹĒ£Ø £©
A.1s22s12p5
B.1s22s22p6
C.1s22s22p63 s2
D.1s22s22p63s1
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æijĶ¬Ń§ĶعżŅŌĻĀ×°ÖĆ²ā¶ØMѳʷ(Ö»ŗ¬Fe”¢Al”¢Cu) ÖŠø÷³É·ÖµÄÖŹĮæ·ÖŹż”£Č”Į½·ŻÖŹĮæ¾łĪŖmgµÄMѳʷ£¬°“ŹµŃé1£ØČēĶ¼1£©ŗĶŹµŃé2£ØČēĶ¼2£©½ųŠŠŹµŃ飬øĆĶ¬Ń§Ė³ĄūĶź³ÉĮĖŹµŃé²¢²āµĆĘųĢåĢå»ż·Ö±šĪŖV1mLŗĶV2 mL£ØŅŃÕŪĖćµ½±ź×¼×“æöĻĀ£©”£
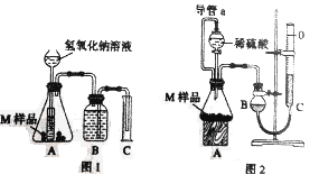
£Ø1£©Š“³öŹµŃé1ÖŠæÉÄÜ·¢Éś·“Ó¦µÄĄė×Ó·½³ĢŹ½£ŗ________________________£»
£Ø2£©Mѳʷ֊ĶµÄÖŹĮæµÄŹżŃ§±ķ“ļŹ½ĪŖ£ØÓĆV1ŗĶV2±ķŹ¾£©£ŗ_________________________”£
£Ø3£©ŹµŃé1½ųŠŠŹµŃéĒ°£¬BĘæÖŠĖ®Ć»ÓŠ×°Āś£¬Ź¹²āµĆĘųĢåĢå»ż________________________”£(Ģī”°Ę«“ó”±”¢”°Ę«Š””±»ņ”°ĪŽÓ°Ļģ”±£¬ĻĀĶ¬)£»Čō²šČ„ŹµŃé2ÖŠµ¼¹Üa£¬Ź¹²āµĆĘųĢåĢå»ż___________________”£
£Ø4£©øĆŹµŃéŠčŅŖ0.50 mol”¤L-1µÄNaOHČÜŅŗ470mL£¬ÅäÖĘŹ±Ó¦ÓĆĶŠÅĢĢģĘ½³ĘĮæ______________gNaOH ”£
£Ø5£©øĆŹµŃéÖŠĖłÓĆĻ”ĮņĖįŹĒÓĆ98%µÄÅØĮņĖį(¦Ń=1.84g/cm3) ÅäÖĘµÄ£¬ÓūÓĆøĆÅØĮņĖįÅäÖĘ³ÉÅضČĪŖ0.5 mol/LµÄĻ”ĮņĖį100mL”£
¢ŁĖłŠčŅĒĘ÷³żÉÕ±”¢²£Į§°ōĶā»¹Šč______________”¢______________”¢______________”£
¢ŚĖłČ”ÅØĮņĖįµÄĢå»żĪŖ_________mL”£
ĻĀĮŠ²Ł×÷ŅżĘšĖłÅäČÜŅŗÅضČĘ«øߵďĒ________________
A.Č”ÅØĮņĖįŹ±ø©ŹÓ B.ŌŚÉÕ±ÖŠĻ”ŹĶÅØĮņĖįŗó£¬Į¢¼“×ŖŅĘ
C.¶ØČŻŹ±ø©ŹÓ D.µßµ¹Ņ”ŌČŗó·¢ĻÖŅŗĆęµĶÓŚæĢ¶ČĻߣ¬µ«Ī“¼ÓĖ®ÖĮæĢ¶ČĻß
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠ¹ŲÓŚµē½āÖŹŗĶ·Ēµē½āÖŹµÄĖµ·ØÕżČ·µÄŹĒ£ŗ£Ø £©
A. BaSO4ÄŃČÜÓŚĖ®£¬ŹĒČõµē½āÖŹ
B. NH3”¢CO2µÄĖ®ČÜŅŗ¾łÄܵ¼µē£¬ĖłŅŌNH3”¢CO2¾łŹĒµē½āÖŹ”£
C. ŹÆÄ«Äܹ»µ¼µē£¬µ«²»ŹĒµē½āÖŹŅ²²»ŹĒ·Ēµē½āÖŹ
D. ČŪČŚNa2OÄܵ¼µē¶ų¹ĢĢåNa2O²»Äܵ¼µē£¬ĖłŅŌČŪČŚNa2OŹĒµē½āÖŹ£¬¹ĢĢåNa2OŹĒ·Ēµē½āÖŹ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĄūÓĆĪ¬ÉśĖŲCÄÜŹ¹µķ·Ū-µāČÜŅŗĶŹÉ«µÄŠŌÖŹ£¬ĶعżŹµŃé(ČēĶ¼ĖłŹ¾)±Č½Ļ¼ÓČėĘ»¹ūÖŗĶ³ČֵĶąÉŁĄ“Č·¶ØĖüĆĒÖŠĪ¬ÉśĖŲCŗ¬ĮæµÄ¶ąÉŁ”£ŅŖµĆ³öÕżČ·½įĀŪ£¬ŌŚŹµŃ鏱ŠčŅŖæŲÖʵÄĢõ¼žŹĒ(””””)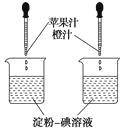
A.ŹµŃ鏱±ŲŠėĻņĮ½ÉÕ±ÖŠĶ¬Ź±µĪ¼ÓŅŗĢå
B.µķ·Ū-µāČÜŅŗµÄĢå»żŗĶÅØ¶Č±ŲŠėĻąµČ
C.½ŗĶ·µĪ¹ÜµĪ³öµÄ¹ūֵĵĪŹż±ŲŠėĻąµČ
D.½ŗĶ·µĪ¹ÜµĪ³öµÄĆæµĪ¹ūÖµÄĢå»ż²»ÓĆĻąµČ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠ·“Ó¦ÖŠ£¬²»ŹōÓŚČ”“ś·“Ó¦µÄŹĒ£Ø £©
A.ŅŅ“¼ÓėÅØĮņĖį¼ÓČȵ½140”ę
B.±½ÓėÅØĻõĖį”¢ÅØĮņĖį»ģŗĻ¹²ČČÖĘČ”Ļõ»ł±½
C.ŅŅ“¼ÓėŃõĘų·“Ӧɜ³ÉČ©
D.ŅŅ“¼ÓėÅØĮņĖį”¢äå»ÆÄĘ¹²ČČ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĖ®ÖŠµÄNO2-ŹĒŗ¬µŖÓŠ»śĪļ·Ö½āµÄ²śĪļ£¬ĘäÅØ¶ČµÄ“óŠ”ŹĒĖ®Ō“ĪŪČ¾µÄ±źÖ¾Ö®Ņ»£®
¼ģ²āĖ®ÖŠµÄNO2-æÉÓƱČÉ«·Ø£¬Ęä²½ÖčŹĒ£ŗ
a£®ÅäÖʱź×¼ČÜŅŗ£ŗ³ĘČ”0.30gNaNO2 £¬ ČÜÓŚĖ®ŗóŌŚČŻĮæĘæÖŠĻ”ŹĶÖĮ1LµĆČÜŅŗA£¬ŅĘČ”5mLČÜŅŗA£¬Ļ”ŹĶÖĮ1L£¬µĆČÜŅŗB£®
b£®ÅäÖʱź×¼É«½×£ŗČ”6Ö»¹ęøńĪŖ10mLµÄ±ČÉ«¹Ü£Ø¼“ÖŹµŲ”¢“óŠ””¢ŗń±”ĻąĶ¬ĒŅ¾ßČūµÄĘ½µ×ŹŌ¹Ü£©£¬·Ö±š¼ÓČėĢå»ż²»µČµÄČÜŅŗB£¬²¢Ļ”ŹĶÖĮ10mL£¬ŌŁ¼ÓČėÉŁŠķ£ØŌ¼0.3g£©¶Ō±½»ĒĖį·ŪÄ©£¬ŹµŃé½į¹ūČēĻĀ±ķĖłŹ¾£ŗ
É«½×ŠņŗÅ | 1 | 2 | 3 | 4 | 5 | 6 |
¼ÓČėČÜŅŗBµÄĢå»ż£ØmL£© | 0 | 2.0 | 4.0 | 6.0 | 8.0 | 10.0 |
c£®¼ģ²ā£ŗČ”10mLĖ®Ńłµ¹Čė±ČÉ«¹ÜÖŠ£¬¼ÓÉŁŠķ¶Ō°±»ł±½»ĒĖį£¬ĻŌÉ«ŗóÓė±ź×¼É«½×¶Ō±Č£®
ĒėĢīŠ“ŅŌĻĀæÕ°×£ŗ
£Ø1£©±ČÉ«·ØµÄ»ł±¾ŅĄ¾ŻŹĒ£»
£Ø2£©ČōĖ®ŃłĻŌÉ«ŗóÓėÉ«½×ÖŠµÄ5ŗÅŃÕÉ«ĻąĶ¬£¬Ōņ±ķĆ÷Ė®ŃłÖŠNO2-ŗ¬ĮæĪŖmg/L£®
£Ø3£©ÓĆNaNO2Ö±½ÓÅäÖĘČÜŅŗBµÄȱµćŹĒ £®
£Ø4£©Čē¹ūĖ®ŃłĻŌÉ«ŗó±Č6ŗÅ»¹Éī£¬Ó¦²ÉČ”µÄ“ėŹ©ŹĒ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÓŠ¹ŲĻĀĮŠ»ÆŗĻĪļµÄĖµ·Ø²»ÕżČ·µÄŹĒ(””””)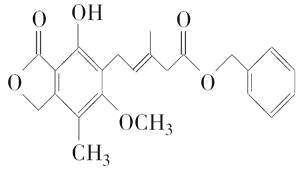
A.¼ČæÉŅŌÓėBr2µÄCCl4ČÜŅŗ·¢Éś¼Ó³É·“Ó¦£¬ÓÖæÉŅŌŌŚ¹āÕÕĻĀÓėBr2·¢ÉśČ”“ś·“Ó¦
B.1 moløĆ»ÆŗĻĪļ×ī¶ąæÉŅŌÓė3 mol NaOH·“Ó¦
C.¼ČæÉŅŌ“߻ƼÓĒā£¬ÓÖæÉŅŌŹ¹ĖįŠŌKMnO4ČÜŅŗĶŹÉ«
D.¼ČæÉŅŌÓėFeCl3ČÜŅŗ·¢ÉśĻŌÉ«·“Ó¦£¬ÓÖæÉŅŌÓėNaHCO3ČÜŅŗ·“Ó¦·Å³öCO2ĘųĢå
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com