合成气(CO和H
2)是重要的化工原料,在工业生产中有着广泛的应用.
(1)工业上用甲烷和水蒸气在高温条件下发生反应制备合成气(CO和H
2),4g甲烷完全反应吸收51.5KJ热量,写该反应的热化学方程式
CH4(g)+H2O(g)=CO(g)+3H2(g)△H=+206KJ/mol
CH4(g)+H2O(g)=CO(g)+3H2(g)△H=+206KJ/mol
(2)已知:CH
4(g)+2O
2(g)═CO
2(g)+2H
2O(g)△H=-802kJ?mol
-1,由反应(1)制备的合成气10m
3(已折成标况),完全燃烧所提供的能量为
1.125×105
1.125×105
kJ
(3)工业上常用合成气来冶炼金属,其中CO还原氧化铁来冶炼生铁方程式如下:
3CO(g)+Fe
2O
3(s)═3CO
2(g)+2Fe(s)△H<0
①如果上述反应在体积不变的密闭容器中发生,当反应达到平衡时,
AD
AD
.
A.容器中Fe
2O
3的质量不随时间而变化 B.反应物不再转化为生成物
C.n (CO):n (CO
2)=1:1 D.容器中气体的压强不随时间而变化
②在一个容积为4L的密闭容器中,1000℃时加入4mol CO(g)和足量Fe
2O
3(s),反应2分钟后达到平衡,测得此时容器内气体的密度为40g/L,求该时间范围内反应的平均反应速率υ(CO
2)=
0.375mol/L?min
0.375mol/L?min
、CO的平衡转化率=
75%
75%
、该反应的化学平衡常数K=
27
27
.
③如果在3分钟时向②的平衡体系中再加入2mol CO(g),其它条件不变,经过2分钟反应又达到平衡.请画出②、③c(CO)、c(CO
2) 随时间变化的图象.

 合成气(CO和H2)是重要的化工原料,在工业生产中有着广泛的应用.
合成气(CO和H2)是重要的化工原料,在工业生产中有着广泛的应用.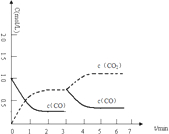



 中考解读考点精练系列答案
中考解读考点精练系列答案 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 (2009?南京二模)工业上可利用合成气(CO和H2的混合气体)生产甲醇(如反应④).已知:
(2009?南京二模)工业上可利用合成气(CO和H2的混合气体)生产甲醇(如反应④).已知:
 )因柔韧性好而被用于制造汽车门窗密封胶条,工业生产乙丙橡胶的单体是
)因柔韧性好而被用于制造汽车门窗密封胶条,工业生产乙丙橡胶的单体是