
分析 先根据n=$\frac{m}{M}$计算出24g C60的物质的量,然后可计算出含有的碳原子的物质的量及数目;碳原子中含有6个电子,结合碳原子的物质的量可计算出含有的核外电子的物质的量.
解答 解:24g C60的物质的量为:$\frac{24g}{12×60g/mol}$=$\frac{1}{30}$mol,含有C原子的物质的量为:$\frac{1}{30}$mol×60=2mol,含有碳原子的数目为2NA,
2mol碳原子中含有核外电子的物质的量为:2mol×6=12mol,
故答案为:2NA;12mol.
点评 本题考查了物质的量的计算,题目难度不大,明确物质的量与摩尔质量、阿伏伽德罗常数之间的关系即可解答,试题侧重基础知识的考查,有利于提高学生的化学计算能力.


 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案科目:高中化学 来源: 题型:选择题
| A. | 当反应相同体积的CH4时反应①②转移的电子数相同 | |
| B. | 由反应①可推知:CH4(g)+4NO2(g)═4NO(g)+CO2(g)+2H2O(l)△H>-574 kJ•mol-1 | |
| C. | 反应②中当生成4.48 L CO2时转移的电子总数为1.60 mol | |
| D. | 若用标准状况下4.48 L CH4还原NO2生成N2和水蒸气,放出的热量为173.4 kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 第三周期元素的离子半径从左到右逐渐减小 | |
| B. | 第二周期元素从左到右,最高正价从+1递增到+7 | |
| C. | 同主族元素的简单阴离子还原性越强,对应单质的氧化性越强 | |
| D. | ⅠA族与ⅦA族元素间可形成共价化合物或离子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
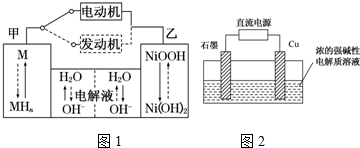
查看答案和解析>>
科目:高中化学 来源:2016-2017学年安徽马鞍山二中高一10月阶段测化学卷(解析版) 题型:计算题
在标准状况下,由20gCO和CO2组成的混合气体,其体积为13.44 L,则此混合物中CO和CO2的质量分别是多少?
查看答案和解析>>
科目:高中化学 来源:2016-2017学年安徽马鞍山二中高一10月阶段测化学卷(解析版) 题型:选择题
同温同压下,相同体积的甲、乙两种气体的质量比为17:14,若乙气体是CO,则甲气体可能为
A.H2S B.HCl C.NH3 D.Cl2
查看答案和解析>>
科目:高中化学 来源:2017届重庆市高三上定时训练8化学卷(解析版) 题型:选择题
下列有关试剂保存的说法错误的是
A. 液溴保存过程中,应在其液面上加少量水进行液封
B. 少量的碱金属单质均应保存在煤油中
C. FeCl3溶液存放时应加少量盐酸
D. AgNO3溶液和KMnO4溶液均应存放在棕色试剂瓶中
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com