
��������(ClO2)��Ŀǰ�����Ϲ��ϵĵ��Ĵ���Ч��
��������������һ�ֻ���ɫ�����壬������ˮ��
��.(1) ClO2����KClO3��H2SO4���ڵ���������Na2SO3��Ӧ�Ƶá���÷�Ӧ�����������뻹ԭ��������ʵ���֮����________��
��.ʵ����Ҳ����NH4Cl�����ᡢNaClO2(��������)Ϊԭ���Ʊ�ClO2�����������£�
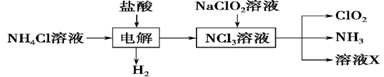
(2) д�����ʱ������Ӧ�Ļ�ѧ����ʽ��____________��
(3) ��ȥClO2�е�NH3��ѡ�õ��Լ���________��(�����)
A������ʳ��ˮ B����ʯ��
C��Ũ���� D��ˮ
(4) �ⶨClO2(����ͼ)�Ĺ������£�����ƿ�м��������ĵ⻯�أ���100 mLˮ�ܽ��
�ټ�3 mL������Һ���ڲ���Һ����м���ˮ�������ɵ�ClO2����ͨ����������ƿ�б����գ�����������е�ˮ��Һ������ƿ�У����뼸�ε�����Һ����c mol·L��1��������Ʊ���Һ�ζ�(I2��2S2O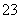 �� 2I����S4O
�� 2I����S4O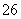 )������ȥV mL�����������Һ��
)������ȥV mL�����������Һ��
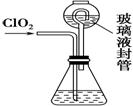
��װ���в���Һ��ܵ�������_______________________________________��
����д��������������������⻯����Һ��Ӧ�����ӷ���ʽ__________________��
�۵ζ��յ��������________________________________________________��
�ܲ��ͨ��ClO2������m(ClO2)��________��(�ú�c��V�Ĵ���ʽ��ʾ)
(5) ��ClO2������������ˮ(pHΪ5.5��6.5)������һ���������岻���������������ClO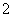
2001���ҹ��������涨������ˮ��ClO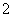 ����Ӧ������0.2 mg·L��1��������ˮ��ClO
����Ӧ������0.2 mg·L��1��������ˮ��ClO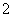 �ĺ������꣬�������м���������Fe2�����÷�Ӧ������������____________ (�ѧʽ)���䷢����Ӧ�����ӷ���ʽΪ_________________ __________��
�ĺ������꣬�������м���������Fe2�����÷�Ӧ������������____________ (�ѧʽ)���䷢����Ӧ�����ӷ���ʽΪ_________________ __________��
��֪ʶ�㡿�ȡ��塢�⼰�仯������ۺ�Ӧ�ã��Ʊ�ʵ�鷽�������
���𰸽�������1�� 1��2 ��1�֣� ��2�� NH4Cl��2HCl  3H2����NCl3 ��2�֣�
3H2����NCl3 ��2�֣�
��3��C ��1�֣�
��4�������ղ���Ķ����������壬��ʹ��ƿ�����ѹǿ��ȡ���2�֣�
��2ClO2��10I����8H����5I2��4H2O��2Cl�� ��2�֣�
����Һǡ������ɫ��Ϊ��ɫ�Ұ��������Һ��ɫ���ٸı� ��1�֣�
��1.35CV��10��2 ��2�֣�
��5��Fe(OH)3 ��1�֣� ClO2����4Fe2����2H2O��8OH����4 Fe(OH)3����Cl����2�֣�
��������1�������������£��������ƺ�����ط���������ԭ��Ӧ��������ء������ơ��������Ⱥ�ˮ���÷�Ӧ����Ԫ�ػ��ϼ���+4�۱�Ϊ+6�ۣ���Ԫ�ػ��ϼ���+5�۱�Ϊ+4�ۣ�����ת�Ƶ����غ�֪�÷�Ӧ�����������뻹ԭ��������ʵ���֮����1��2��
��2�� ����Ȼ�狀���������Һʱ����������ͼ֪������������NCl3�����ⷴӦ����ʽΪ��NH4Cl+2HCl 3H2����NCl3
3H2����NCl3
��3��A��ClO2������ˮ���������ñ���ʳ��ˮ���հ�������A����B����ʯ�Ҳ������հ�������B����C��Ũ����������հ������Ҳ�Ӱ��ClO2����C��ȷ��D��ClO2������ˮ����������ˮ���հ�������D����ѡ��C��
��4������װ���в���Һ��ܵ������ǣ���ˮ�ٴ����ղ���Ķ����������壬��ʹ��ƿ����ѹǿ��ȣ�
������Ŀ��Ϣ��֪��ClO2ͨ����ƿ�����Ե⻯����Һ��Ӧ������I-ΪI2����������ԭΪCl-��ͬʱ����ˮ����Ӧ���ӷ���ʽΪ2ClO2+10I-+8H+=2Cl-+5I2+4H2O��
����Һ����ɫǡ�ñ�Ϊ��ɫ���Ұ�����ڲ���ɫ��˵���ζ����յ㣬
��VmLNa2S2O3��Һ����Na2S2O3���ʵ���ΪV•10-3 L��cmol/L=c•V•10-3 mol����
���ݹ�ϵʽ��2ClO2��5I2��10Na2S2O3��
2 10
n��ClO2�� c•V•10-3 mol
����n��ClO2��=1/5 c•V•10-3 mol������m��ClO2��=1/5 c•V•10-3 mol��67.5g/mol=1.35cv��10-2g
(5) ClO2-���������ԣ��ܰѻ�ԭ�Ե������������ɸ�̬�����ʣ�����PHΪ5.5��6.5���ɳ�������ȥ����PHΪ5.5��6.5���ɳ�����������Fe��OH��3���䷢����Ӧ�����ӷ���ʽΪ: ClO2����4Fe2����2H2O��8OH����4 Fe(OH)3����Cl��
��˼·�㲦�����⿼���Ķ���Ŀ��ȡ��Ϣ������������ԭ��Ӧ�ζ���Ӧ�á��Թ������̼�װ����������ȣ��Ѷ��еȣ�Ҫ��ѧ��Ҫ����ʵ��ʵ�����֪ʶ�����Ӧ����Ϣ��������������ע�����֪ʶ��ȫ�����ա�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��һ������п��100mL 18.5mol•L��1Ũ�����ַ�Ӧ��п��ȫ�ܽ⣬ͬʱ��������A 33.6L����״����������Ӧ�����Һϡ����1L�������Һ��c��H+��=0.1mol•L��1�������������д�����ǣ�������
| �� | A�� | ����AΪSO2��H2�Ļ���� | B�� | ����A��SO2��H2�������Ϊ1��5 |
| �� | C�� | ��Ӧ�����ĵ�Zn������Ϊ97.5 g | D�� | ��Ӧ�й�ת�Ƶ���3 mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
SO2��NO�Ǵ�����Ⱦ�����SO2 ��NO�����Na2S2O4��NH4NO3��Ʒ������ͼ���£�CeΪ��Ԫ�أ���
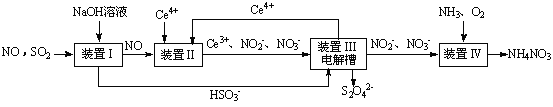
��1��װ�â�������HSO3�������ӷ���Ϊ ��
��2�����������H2SO3��HSO3����SO32����������SO2��NaOH��Һ��Ӧ�����Һ�У����ǵ����ʵ�������X(i)����ҺpH �Ĺ�ϵ����ͼ��ʾ��
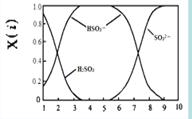
������˵����ȷ���� ������ĸ��ţ���
a��pH=8ʱ����Һ��c(HSO3��) < c(SO32��)
b��pH=7ʱ����Һ��c(Na+) =c(HSO3��)+c(SO32��)
c��Ϊ��þ����ܴ���NaHSO3���ɽ���Һ��pH������4��5����
����pH=5��NaHSO3��Һ�еμ�һ��Ũ�ȵ�CaCl2��Һ����Һ�г��ֻ��ǣ�pH��Ϊ2���û�ѧƽ���ƶ�ԭ��������ҺpH���͵�ԭ�� ��
��3��װ�â��У����������£�NO��Ce4+�����IJ�����Ҫ��NO3����NO2����д������NO3�������ӷ���ʽ ��
��4��װ�â������֮һ������Ce4+����ԭ������ͼ��ʾ��
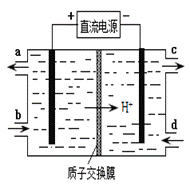
������Ce4+�ĵ缫��ӦʽΪ ��
������Ce4+�ӵ��۵� ������ĸ��ţ���������
��5����֪����װ�â�����Һ�У�NO2����Ũ��Ϊa g·L-1��Ҫʹ1 m3����Һ�е�NO2����ȫת��ΪNH4NO3����������װ�â���ͨ���״���µ�O2 L�����ú�a����ʽ��ʾ������������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����ʵ���������ȷ����
A���������ֹͣ����ʱ��Ӧ�Ȳ������ӳ����ú�����ƿ����Ƥ�ܣ��ٹر�ˮ��ͷȫ��Ʒ��ѧ���� �ú��벻�ˣ�
B����Һ����ʱ����Һ©���е��²�Һ����¿ڷų����ϲ�Һ����Ͽڵ���
C����ȡ����ʱ��Ӧѡ���л���ȡ��������ȡ�����ܶȱ����ˮ��
D������ʱ��Ӧʹ�¶ȼ�ˮ����������ƿ֧�ܿ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ʵ��ʱ��������ע��������
�ķ��������ͼ��װ�õ������ԡ�������������ʱ�����װ����������
�ã����ܹ۲쵽

A������©���¶˹ܿڲ�������
B��ƿ��Һ����������
C������©���ڵ�Һ������
D��ע��������Һ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����ʯ�ǹ�ҵ��������Ҫԭ��֮һ������Ҫ�ɷ�Ϊ����������������в�����Ԫ�غ���Ԫ�أ������ʲ���ϡ���ᷴӦ����ij�о���ѧϰС���ij����ʯ������������Ļ�ѧʽ����̽����
��������衿
����1������ʯ��ֻ��+3������ ����2������ʯ��ֻ��+2������
����3�� ��
���������ϡ�2KMnO4+16HCl��Ũ��=2KCl+2MnCl2+5Cl2��+8H2O
�������о��� ��ʵ��һ��
ȡ����ʯ��Ʒ���飬ʢ���ձ��У�����������X��Һ���ȣ�����ܽ����Һ�ֳ��ķݣ�
�����һ����Һ�еμ�����KSCN��Һ��
����ڶ�����Һ�еμ��������������Һ��
�����������Һ�еμ�����KSCN��Һ���ٵμ�����˫��ˮ��Һ��
������ķ���Һ�еμ���������������Һ��
��1������X��Һ�� ���ϡ���ᡱ����ϡ���ᡱ��Ũ���ᡱ�������������У�һ����֤������ʯ�к�+2�����ķ����� ������ţ���
�������о��� ��ʵ���������ʯ�к������IJⶨ��
�ٰ�ͼ��װ���������װ�õ������ԣ��ڽ�5.0g����ʯ����Ӳ�ʲ������У�����װ���е�ҩƷ��ͼ��ʾ���г�װ������ȥ������A�п�ʼ��Ӧ�����ϵػ��������װ����ͨ����������Dװ�ó��ڴ������鴿��ȼC���ƾ��ƣ��ܳ�ַ�Ӧ�����ƾ��ƣ��ٳ���ͨ������ֱ����ȫ��ȴ��
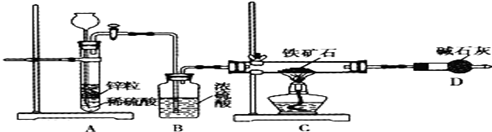
��2���������������ж��ʵ�飬��������������ȷ�������ղ�ý����ƫ�ߣ���������Ľ������Ľ����� �������ȥBװ�ã���ý�����ܻ� ���ƫ�ߡ�����ƫ�͡�����Ӱ�족����
��3���Ľ�������÷�Ӧ��Dװ������1.35g��������ʯ�����İٷֺ���Ϊ ������H2����CO�����貹�� װ�ã���ͬѧ��Ϊ�����ⶨDװ�õľ���������ͨ���ⶨ������ ��Ҳ�ܴﵽʵ��Ŀ�ģ�
��ʵ����������ʯ�к������IJⶨ��
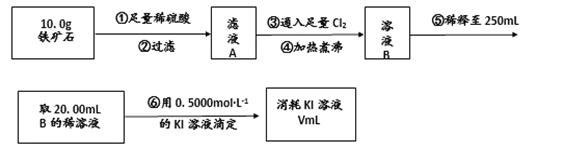
��4����������������� ��
��5����������õ��IJ����������ձ�������������ͷ�ι��⣬���� ��
��6�������йز����˵������ȷ���� ������ţ���
a����Ϊ��ˮΪ��ɫ�����Եζ������в���Ҫ��ָʾ��
b���ζ������п����õ�����Һ��Ϊָʾ��
c���ζ���������ˮϴ�Ӻ����ֱ��װҺ
d����ƿ�����ô�װҺ��ϴ
e���ζ������У��۾�Ӧע�ӵζ�����Һ��仯
f���ζ�������30s����Һ���ָ�ԭ������ɫ���ٶ���
��7�����ζ�����������0.5000mol•L-1��KI��Һ20.00mL��������ʯ�����İٷֺ���Ϊ ���ۺ�ʵ�飨�����Ľ�������������������ʯ������������Ļ�ѧʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ҵ���üױ��������ǻ�����������(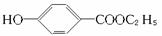 )����������£�
)����������£�

�ݺϳ�·����д���пհף�
(1)�л���A�Ľṹ��ʽ��____________________��B�Ľṹ��ʽ��____________________��
(2)��Ӧ������____________��Ӧ����Ӧ������______________��Ӧ��
(3)�ۺ͢�Ŀ����______________________________________________��
(4)д����Ӧ�Ļ�ѧ����ʽ��__________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�㶹����һ����Ȼ���ϣ������ں��㶹��������ֲ���С���ҵ�ϳ���ˮ��ȩ���������ڴ�������
�¼��ȷ�Ӧ�Ƶã�
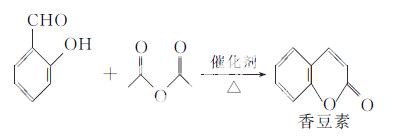
�������ɼױ�Ϊԭ�������㶹�ص�һ�ֺϳ�·��(���ַ�Ӧ����������������ȥ)��
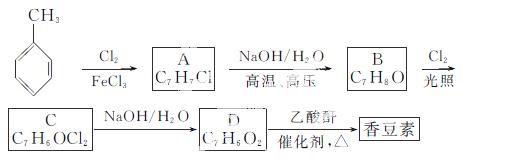
��֪������Ϣ��
��A�������ֲ�ͬ��ѧ�������⣻
��B����FeCl3��Һ������ɫ��Ӧ��
��ͬһ��̼ԭ�������������ǻ�ͨ�����ȶ�������ˮ�γ��ʻ���
��ش��������⣺
(1)�㶹�صķ���ʽΪ__________��
(2)�ɼױ�����A�ķ�Ӧ����Ϊ__________��A�Ļ�ѧ����Ϊ__________��
(3)��B����C�Ļ�ѧ��Ӧ����ʽΪ__________________________________��
(4)B��ͬ���칹���к��б����Ļ���__________�֣������ں˴Ź���������ֻ������������________�֣�
(5)D��ͬ���칹���к��б����Ļ���________�֣����У�
�ټ��ܷ���������Ӧ�����ܷ���ˮ�ⷴӦ����__________(д�ṹ��ʽ)��
���ܹ��뱥��̼��������Һ��Ӧ�ų�CO2����__________(д�ṹ��ʽ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��֪��2CH3OH(g) CH3OCH3(g)��H2O(g)����H����25 kJ��mol��1��ij�¶��µ�ƽ�ⳣ��Ϊ400�����¶��£���1 L���ܱ������м���CH3OH����Ӧ��ijʱ�̲�ø���ֵ����ʵ���Ũ�����±�������˵����ȷ���� (�� ��)
CH3OCH3(g)��H2O(g)����H����25 kJ��mol��1��ij�¶��µ�ƽ�ⳣ��Ϊ400�����¶��£���1 L���ܱ������м���CH3OH����Ӧ��ijʱ�̲�ø���ֵ����ʵ���Ũ�����±�������˵����ȷ���� (�� ��)
| ���� | CH3OH | CH3OCH3 | H2O |
| c/(mol��L��1) | 0.8 | 1.24 | 1.24 |
A. ƽ��������¶ȣ�ƽ�ⳣ��>400
B. ƽ��ʱ��c(CH3OCH3)��1.6 mol��L��1
C. ƽ��ʱ����Ӧ����������������40 kJ
D. ƽ��ʱ���ټ�������ʼ������CH3OH������ƽ���CH3OHת��������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com