
| A、原子半径:C>D>A>B |
| B、A的氧化物一定为酸性氧化物 |
| C、元素B和C只能形成一种化合物 |
| D、A、C、D的最高价氧化物对应的水化物均能两两相互反应 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
 116号元素已被命名为“鉝”;2014年5月,科学家已确认发现117号元素,未命名,元素符号Uus;若将元素周期表的“一列”看作“一族”;则对117号元素的相关表述或性质推断错误的是( )
116号元素已被命名为“鉝”;2014年5月,科学家已确认发现117号元素,未命名,元素符号Uus;若将元素周期表的“一列”看作“一族”;则对117号元素的相关表述或性质推断错误的是( )| A、属第17族元素 |
| B、属卤族元素 |
| C、属非金属元素 |
| D、有放射性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
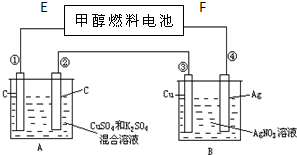 如图所示,用甲醇和氧气以及强碱做电解质溶液的新型燃料电池做电源,对A、B 装置通电一段时间后,发现有1.6g甲醇参加反应且③电极增重(假设工作时无能量损失).请回答下列问题:
如图所示,用甲醇和氧气以及强碱做电解质溶液的新型燃料电池做电源,对A、B 装置通电一段时间后,发现有1.6g甲醇参加反应且③电极增重(假设工作时无能量损失).请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CH4?14H2O | ||
| B、CH4?8H2O | ||
C、CH4?
| ||
| D、CH4?6H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、△H>0,△S>0 |
| B、△H>0,△S<0 |
| C、△H<0,△S>0 |
| D、△H<0,△S<0 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、C3H7OH |
| B、CH3CHO |
| C、CH3CO CH3 |
| D、C2H4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com