
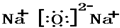 ��
������ ��1�������������
��2��Fe2O3�õ����ӱ���ԭ�����ȷ�Ӧ��ұ���۵�ߵĽ�����
��3��Na2O�����Ӽ���Ϊ���ӻ����
��4��̼�����Ʒֽ�����̼���ơ�ˮ��������̼��
��� �⣺��1�������к��������ṹʽΪN��N���ʴ�Ϊ��N��N��
��2��Fe2O3�õ����ӱ���ԭ����Na��Ӧ���ɵĻ�ԭ����ΪFe�����ȷ�Ӧ��ұ���۵�ߵĽ�������Cr��Mn�ȣ��ʴ�Ϊ��Fe�����۵�ߵĽ�����
��3��Na2O�����Ӽ���Ϊ���ӻ��������ʽΪ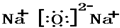 ���ʴ�Ϊ��
���ʴ�Ϊ��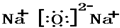 ��
��
��4��̼�����Ʒֽ�����̼���ơ�ˮ��������̼����Ӧ����ʽΪ2NaHCO3$\frac{\underline{\;\;��\;\;}}{\;}$Na2CO3+H2O+CO2�����ʴ�Ϊ��2NaHCO3$\frac{\underline{\;\;��\;\;}}{\;}$Na2CO3+H2O+CO2����
���� ���⿼�����ʵ����ʼ�Ӧ�ã�Ϊ��Ƶ���㣬�������ʵ����ʡ������ķ�Ӧ����;Ϊ���Ĺؼ������ط���������Ӧ�������Ŀ��飬ע�����ȷ�Ӧ��Ӧ�ã���Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 25% | B�� | 35% | C�� | 50% | D�� | 75% |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Li��Be��Bԭ�������������������� | |
| B�� | N��O��F�縺���������� | |
| C�� | P��S��ClԪ����������������� | |
| D�� | Na��K��Rb��һ������������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | IO3- | B�� | Fe3+ | C�� | SO2 | D�� | MnO4- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� |  ��ͼ��ʾװ���Ʊ���ȩ��֬ | B�� |  ��ͼ��ʾװ�òⶨ����Ũ�� | ||
| C�� |  ��ͼ��ʾװ�ù۲�������ʴ | D�� |  ��ͼ��ʾװ����֤������ϩ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 �������������������۾��IJ��ϣ���д�������йط�Ӧ�Ļ�ѧ����ʽ��
�������������������۾��IJ��ϣ���д�������йط�Ӧ�Ļ�ѧ����ʽ��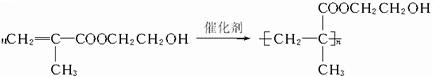 ��
�� ��
�� ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CO | B�� | CaF2 | C�� | CH4 | D�� | NH4Cl |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | dԪ�صķǽ�������ǿ | |
| B�� | ���Ǿ��������ֻ��������ϵ������� | |
| C�� | a������������Ӧ��ˮ������ǿ�� | |
| D�� | b��c��d����̬�⻯����ȶ��ԣ�b��c��d |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��֪H+��aq��+OH-��aq���TH20��l����H=-57.3kJ•mol-1����H2SO4��Ba��OH��2��Ӧ�ķ�Ӧ�ȡ�H=-2����-57.3��kJ•mol-1 | |
| B�� | ��4P��s�����ף��TP4��s�����ף���H=+139.2kJ/mol��֪�����ױȰ����ȶ� | |
| C�� | H2��g����ȼ������285.8kJ•mol-1����2H2O�T2H2��g��+O2��g����H=+571.6KJ•mol-1 | |
| D�� | ���º���ʱ����2molA��1molBͶ���ܱ������У�������Ӧ��2A��g��+B��g��?2C��g������ַ�Ӧ���÷ų�������ΪQkJ����÷�Ӧ�ġ�H=-QkJ/mol |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com