
����Ŀ����֪A��B��C��D��E�Ƕ������е�5�ַǽ���Ԫ��,���ǵ�ԭ��������������AԪ��ԭ���γɵ����Ӻ��������Ϊ��,C��D��Ԫ�����ڱ��д������ڵ�λ�ã�Bԭ�ӵ��������������ڲ��������2����EԪ����DԪ��ͬ����; E�ĵ���Ϊ��ɫ���壬�����ڶ���̼��
��1����д��Ԫ�ط���:
A_______,B_______,C_________,D_________��E__________��
��2������E�������ӵĽṹʾ��ͼ:__________
��3��A�ĵ��ʺ�C�ĵ�����һ�������·�Ӧ���ɻ�����X���÷�Ӧ�Ļ�ѧ����ʽΪ_________����X��ˮ��Һ�е����̪��Һ����۲쵽_____________��
��4����9g B������������D������ȼ�գ���������ͨ��1L lmol/L NaOH��Һ�У���ȫ���պ���Һ�д������ڵ�������___________��
���𰸡� H C N O S S2-: ![]() N2+3H2
N2+3H2![]() 2NH3 ��Һ��� Na+��HCO3-��CO32-
2NH3 ��Һ��� Na+��HCO3-��CO32-
��������A��B��C��D��E�Ƕ������е�5�ַǽ���Ԫ�أ����ǵ�ԭ����������������AԪ��ԭ���γɵ����Ӻ��������Ϊ�㣬��AΪHԪ�أ�Bԭ�ӵ��������������ڲ��������2����ԭ��ֻ����2�����Ӳ㣬����������Ϊ4����BΪ̼Ԫ�أ�E�ĵ���Ϊ��ɫ���壬�����ڶ���̼����EΪSԪ�أ�EԪ����DԪ��ͬ���壬��DΪOԪ�أ�C��D��Ԫ�����ڱ��д������ڵ�λ�ã���D��ԭ����������CΪNԪ����
(1)������������֪��AΪHԪ�ء�BΪCԪ�ء�CΪNԪ�ء�DΪOԪ�أ�EΪSԪ�أ��ʴ�Ϊ��H��C��N��O��S��
(2)E��������ΪS2-�����ӽṹʾ��ͼ��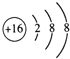 ���ʴ�Ϊ��
���ʴ�Ϊ��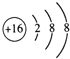 ��
��
(3)A�ĵ�����������C�ĵ����ǵ����������͵�����һ�������·�Ӧ���ɰ�����N2+3H2![]() 2NH3���ڰ�ˮ�д���NH3+H2O=NH3��H2O��NH3��H2O
2NH3���ڰ�ˮ�д���NH3+H2O=NH3��H2O��NH3��H2O ![]() NH4++OH-�����������ˮ��Һ�ʼ��ԣ������̪��Һ����Һ�ʺ�ɫ���ʴ�Ϊ��N2+3H2
NH4++OH-�����������ˮ��Һ�ʼ��ԣ������̪��Һ����Һ�ʺ�ɫ���ʴ�Ϊ��N2+3H2![]() 2NH3 ����Һ�����
2NH3 ����Һ�����
(4)9gC�����ʵ�����0.75mol��C��������������ȼ�գ�����������CO2��C+O2 ![]() CO2���������ɵĶ�����̼��0.75mol��NaOH�����ʵ���Ϊn=1L��1mol/L=1mol��������̼���������Ƶ����ʵ���֮��Ϊ3��4����CO2+NaOH=NaHCO3��CO2+2NaOH=Na2CO3+H2O��֪����������̼���������Ƶ����ʵ�����Ϊ1��1ʱ��������̼�����ƣ���������̼���������Ƶ����ʵ�����Ϊ1��2ʱ��������̼��������������̼�����������Ƶ����ʵ���֮�ȴ���
CO2���������ɵĶ�����̼��0.75mol��NaOH�����ʵ���Ϊn=1L��1mol/L=1mol��������̼���������Ƶ����ʵ���֮��Ϊ3��4����CO2+NaOH=NaHCO3��CO2+2NaOH=Na2CO3+H2O��֪����������̼���������Ƶ����ʵ�����Ϊ1��1ʱ��������̼�����ƣ���������̼���������Ƶ����ʵ�����Ϊ1��2ʱ��������̼��������������̼�����������Ƶ����ʵ���֮�ȴ���![]() С��1ʱ��������̼���ƺ�̼�����ƵĻ������ԣ���Һ�е�������̼���ƺ�̼�����ƣ��ʴ�Ϊ��CO32- HCO3-��Na+��
С��1ʱ��������̼���ƺ�̼�����ƵĻ������ԣ���Һ�е�������̼���ƺ�̼�����ƣ��ʴ�Ϊ��CO32- HCO3-��Na+��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��M��һ����Ҫ���ϵ��м��壬�ṹ��ʽΪ��![]() ���ϳ�M��һ��;�����£�
���ϳ�M��һ��;�����£�

A��F�ֱ����һ���л�������ϳ�·���еIJ��ֲ��P��Ӧ��������ȥ��
��֪����Y�ĺ˴Ź�������ֻ��1�ַ壻
��RCH��CH2 ![]() RCH2CH2OH��
RCH2CH2OH��
�������ǻ�������ͬһ��̼ԭ���ϲ��ȶ�������ˮ��
��ش��������⣺
��1��Y�Ľṹ��ʽ�� ��D�й����ŵ������� ��
��2������ٵķ�Ӧ������ ��
��3������˵������ȷ���� ��
a��A��E���ܷ���������Ӧ b��1 mol B��ȫȼ����6 mol O2
c��C��������������ͭ����Һ��Ӧ d��1 mol F�������3 mol H2��Ӧ
��4������������ѧ����ʽΪ ��
��5������ߵĻ�ѧ��Ӧ����ʽ�� ��
��6��M���������õ�X��C11H12O4����X��ͬ���칹����ͬʱ�������������Ľṹ��ʽΪ ��
a��������ֻ������ȡ�����������ϵ�һ�ȴ�����2��
b��ˮ��ֻ���ɷ��㴼�Ͷ�Ԫ�ᣬ�Ҷ�Ԫ��ĺ˴Ź�������ֻ��2�ַ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧС��ͬѧ������װ�ú��Լ�����ʵ�飬̽��O2��KI��Һ������Ӧ��������

��ѡ�Լ���30%H2O2��Һ��0.lmol/LH2SO4��Һ��MnO2���塢KMnO4����
��1��С��ͬѧ��Ƽס��ҡ�������ʵ�飬��¼����
���� | ���� | |
�� | ��I����ƿ�м���_____����I��_________�м���30%H2O2��Һ������I��. �������� | I�в�����ɫ���岢�����������������������ð������ҺѸ�ٱ��� |
�� | �����м���KMnO4���壬��������������ȼ�ƾ��� | ����������ð������Һ������ |
�� | �����м���KMnO4���壬���м�������0.1 mol/L H2SO4��Һ����������������ȼ�ƾ��� | ����������ð������Һ���� |
��2����ʵ����O2��KI��Һ��Ӧ�����ӷ���ʽ��___________________________��
��3���Ա��ҡ���ʵ���֪��O2��KI��Һ������Ӧ������������__________________��Ϊ��һ��̽���������Է�Ӧ���ʵ�Ӱ�죬�ɲ�ȡ��ʵ���ʩ��___________________________��
��4���ɼס��ҡ�����ʵ���Ʋ⣬��ʵ�������I�еİ���ʹ��Һ������ѧ����I�в���������ֱ��ͨ������__________ ������ĸ����Һ��֤���˰����к���H2O2��
A.���� KMnO4 B. FeC12 C. Na2S D.Ʒ��
��5��������ʾ��KI��Һ�ڿ����о��ù����лᱻ����������4KI+O2+2H2O==2I2+4KOH����С��ͬѧȡ20 mL���õ�KI��Һ�������м��뼸�ε�����Һ�����û�й۲쵽��Һ��ɫ���������Dz�������Ƿ����˷�Ӧ��3I2+6OH-==5I-+IO3-+3H2O��ɵġ������ʵ��֤�����ǵIJ����Ƿ���ȷ��________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������������Ҫ��ҽҩ�м��壬��A��BΪԭ�Ϻϳɱ�����������F·�����£�
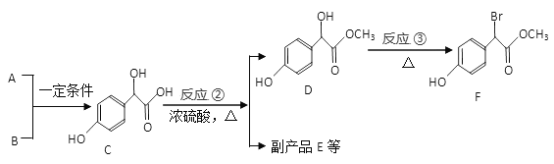
��1�� A �ķ���ʽΪC2H2O3��1molA �����ĺ���2.5 molCu(OH)2 ��������Һ��д����Ӧ���Ļ�ѧ����ʽ_______________________________��
��2��������C ��������������Ϊ______________����һ��������C ������NaOH ��Һ��Ӧ��1molC �������NaOH �����ʵ���Ϊ_________________mol��
��3����Ӧ���ķ�Ӧ����Ϊ___________�� ��д����Ӧ���Ļ�ѧ����ʽ_____________________________��
��4��E ����2 ������C���ɵĺ���3 ����Ԫ���Ļ����E �ķ���ʽΪ____________________��
��5������������F ������ͬ���칹��(�����������칹) ��__________�֣����к˴Ź��������������Ľṹ��ʽΪ____________________��
������һԪ��������� ��������ֻ��2 ��ȡ���� ����FeCl3 ��Һ����ɫ
��6�����������ϳ�·�ߡ��Ա�����Ϊԭ�������Լ���ѡ������Ʊ�A �ĺϳ�·�ߡ���֪RCH2COOH ![]() RCH(Cl)COOH______________________
RCH(Cl)COOH______________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧƽ����Ҫ�о�������һ�෴Ӧ�Ĺ��ɣ�������
A.���ַ�Ӧ
B.�κη�Ӧ
C.���淴Ӧ
D.���巴Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ�������£��ס��������ݻ���ȵ���ƿ�зֱ�װ�����������壨ͬ�¡�ͬѹ���ɷݼ��±�����ֹˮ��K��ʹ����ƿ�������ֽӴ���������ѹǿ��С�����˳����ȷ����
��� | �� | �� | �� |
�������� | H2 | NH3 | NO |
�������� | Cl2 | HCl | O2 |
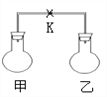
A. �ڢۢ� B. �ۢ٢� C. �ۢڢ� D. �٢ڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʽΪC9H12���л����֪�����ϵ�һ�ȴ���ֻ�����֣�����˵������ȷ���ǣ� ��
A.���л��ﲻ�ܷ���ȡ����Ӧ�����ܷ����ӳɷ�Ӧ
B.���л��ﲻ��ʹ���Եĸ��������Һ��ɫ������ʹ��ˮ��ɫ
C.���л�������е�����ԭ�ӿ�����ͬһƽ����
D.���л����һ�ȴ��������5��ͬ���칹��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���������İ�������粒��������ܱ������У�������Ӧ��NH2COONH4��s��![]() 2NH3��g��+CO2��g�����÷�Ӧ��ƽ�ⳣ���ĸ���������lgK��ֵ���¶ȣ�T���ı仯������ͼ��ʾ������˵������ȷ����
2NH3��g��+CO2��g�����÷�Ӧ��ƽ�ⳣ���ĸ���������lgK��ֵ���¶ȣ�T���ı仯������ͼ��ʾ������˵������ȷ����

A. �÷�Ӧ�ġ�H��0
B. A���Ӧ״̬��ƽ�ⳣ��K��A��=10��2.294
C. NH3�������������ʱ���÷�Ӧһ���ﵽƽ��״̬
D. 30��ʱ��B���Ӧ״̬����������< �����棩
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijͬѧ��������ƽ����п��24.4g��1g���������룩������п���������̣�����������̣�����ƽƽ��ʱ������ȡ��п����ʵ������Ӧ�ǣ��� ��
A. 24.4g B. 25.5g C. 23.6g D. 24g
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com