
 .
.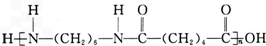 +(2n-1)H2O.
+(2n-1)H2O. 分析 (1)溴乙烷与氢氧化钠溶液反应,发生水解反应生成乙醇;
(2)氯乙烷和氢氧化钠共热,发生消去反应生成乙烯;
(3)醛类可以发生银镜反应生成羧酸铵、金属单质银以及氨气;
(4)反应生成2,4,6-三溴苯酚沉淀和HBr;
(5)发生缩聚反应生成尼龙-66.
解答 解:(1)卤代烃在碱性水溶液加热条件下发生取代反应,由溴乙烷变成乙醇,生成乙醇与溴化钠方程式为CH3CH2Br+NaOH$→_{△}^{H_{2}O}$CH3CH2OH+NaBr,
故答案为:CH3CH2Br+NaOH$→_{△}^{H_{2}O}$CH3CH2OH+NaBr;
(2)氯乙烷和氢氧化钠共热生成乙烯和氯化钠,反应的化学方程式为CH3CH2Cl+NaOH$→_{△}^{乙醇}$CH2=CH2↑+NaCl+H2O,
故答案为:CH3CH2Cl+NaOH$→_{△}^{乙醇}$CH2=CH2↑+NaCl+H2O;
(3)丙醛可以发生银镜反应生成丙酸铵、金属单质银以及氨气,反应为CH3CH2CHO+2Ag(NH3)2OH$→_{△}^{水浴}$CH3CH2COONH4+2Ag↓+3NH3+H2O,
故答案为:CH3CH2CHO+2Ag(NH3)2OH$→_{△}^{水浴}$CH3CH2COONH4+2Ag↓+3NH3+H2O;
(4)苯酚与溴水反应,生成2,4,6-三溴苯酚沉淀和HBr,反应的化学方程式为
故答案为: ;
;
(5)己二酸与己二胺合成尼龙-66 的反应方程式为n HOOC(CH2)4COOH+n H2N(CH2)6NH2$\stackrel{一定条件}{→}$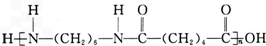 +(2n-1)H2O,
+(2n-1)H2O,
故答案为:n HOOC(CH2)4COOH+n H2N(CH2)6NH2$\stackrel{一定条件}{→}$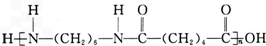 +(2n-1)H2O.
+(2n-1)H2O.
点评 本题考查有机化学反应方程式的书写,为高频考点,把握有机物的结构与性质、反应条件及反应类型为解答的关键,注重基础知识的夯实,题目难度不大.


 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源: 题型:选择题
| A. | 1.2mol•L-1•min-1 | B. | 0.8mol•L-1•min-1 | ||
| C. | 1.0mol•L-1•min-1 | D. | 0.6mol•L-1•min-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硝酸铵和水 | B. | 浓硫酸和水 | C. | 生石灰和水 | D. | 苛性钠和水 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 请回答下列问题:
请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:填空题
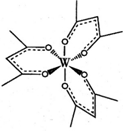 现有原子序数小于36的X、Y、Z、W四种元素.其中X元素的一种核素核内无中子;Y是地壳中含量最多的金属元素;Z原子的质量数为12,质子数与中子数相等;W的基态原子核外3d轨道上的电子数是最外层电子数的3倍.请回答下列问题:
现有原子序数小于36的X、Y、Z、W四种元素.其中X元素的一种核素核内无中子;Y是地壳中含量最多的金属元素;Z原子的质量数为12,质子数与中子数相等;W的基态原子核外3d轨道上的电子数是最外层电子数的3倍.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
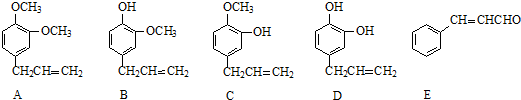
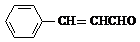 +2Ag(NH3)2OH$\stackrel{△}{→}$
+2Ag(NH3)2OH$\stackrel{△}{→}$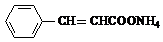 +H2O+2Ag↓+3NH3,Y的结构简式为
+H2O+2Ag↓+3NH3,Y的结构简式为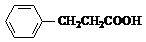 ,反应③属于加成反应.
,反应③属于加成反应.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3:2 | B. | 4:3 | C. | 1:1 | D. | 8:9 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
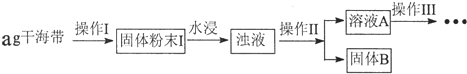
| 序号 | 实验操作 | 实验现象 | 结论 |
| ① | 取少量稀释后的溶液A加入淀粉后再用硫酸酸化,分装于试管Ⅰ、Ⅱ | 无现象 | |
| ② | 往试管I中加入FeCl2溶液,后加入2滴KSCN溶液并振荡; | 无现象 | 证明不是以IO3-形式存在 |
| ③ | 往试管II中加入3%H2O2溶液并振荡 | 溶液变蓝 | 证明以I-形式存在 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子序数:b>a>c>d | B. | 原子半径:A>B>C>D | ||
| C. | 金属性:B>A,非金属性:D>C | D. | 离子半径:D>C>B>A |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com