
【题目】将下列硅酸盐的化学式改写成氧化物的形式:硅酸钠(Na2SiO3) , 滑石[Mg3(Si4O10)(OH)2] .
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.浓H2SO4有脱水性,因而可作干燥剂
B.常温下,浓H2SO4可用铝制密闭容器储运
C.浓H2SO4具有氧化性,稀H2SO4无氧化性
D.浓H2SO4难挥发,因而可在敞口容器中储存
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的数值,下列说法错误的是

A. 256gS8分子(上图)中含S-S键为7NA个
B. 1molNa与O2完全反应,生成Na2O和Na2O2的混合物,转移电子总数为NA个
C. 由1molCH3COONa和少量CH3COOH形成的中性溶液中,CH3COO-数目为NA个
D. 一定条件下,2mo1SO2和1molO2混合在密闭容器中充分反应后容器中的分子数大于2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于SiO2和CO2的说法中正确的是 ( )
A.CO2、SiO2都能与碱及碱性氧化物反应
B.CO2和SiO2与水反应分别生成相应的酸
C.二氧化硅可用来制作干燥剂,因二氧化硅可与水反应
D.CO2和SiO2都是由相应的分子构成的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于化学键的各种叙述中,下列说法中正确的是( )
A.在离子化合物里,只存在离子键
B.共价化合物里,一定不存在离子键
C.非极性键只存在于双原子的单质分子里
D.由非金属元素组成的化合物中只存在共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】蔗糖与浓硫酸的炭化实验会产生大量的有刺激性气味的气体对环境产生污染。为此,某化学兴趣小组设计了如下装置进行实验。玻璃管中①、②、③分别为CO检测试纸 (浸有氯化钯洛液的滤纸,遇CO变黑色)、滴有品红溶液的滤纸、滴有酸性KMn04 溶液的滤纸,a和b分别为两个小气球。

实验步骤如下:按图示连接好仪器,然后检查装置的气密性;装好试剂,夹紧止水夹K,向A瓶中的蔗糖上小心滴加浓硫酸,片刻后可观察到A瓶内蔗糖变黑,体积膨胀,有白雾产生,气球a鼓起,玻璃管中①号滤纸白色变黑色,②号和③号滤纸均褪色。请回答以下问题:
(1)上图中盛有浓硫酸的仪器名称为________。
(2)根据实验中滤纸的现象说明SO2具有的性质分别是:②号_____;③号_____。
A.氧化性 B. 还原性 C. 漂白性 D. 酸性氧化物通性
(3)B瓶中酸性KMnO4溶液的作用是_____________________________________,发生反应的离子方程式为___________________________________________。
(4)打开止水夹K,使气球a内气体缓慢通过B瓶和C瓶,一段时间之后,发现澄清石灰水变浑浊,但此现象并不能证明该反应生成了CO2。为了证明有CO2生成并简化实验装置,可在④号位置放上滴有_____________的滤纸(从以下试剂中选择)。
A.品红溶液 B.酸性高锰酸钾溶液 C.溴水 D.澄清石灰水
(5)若在尾端没有气球b,会有什么不良结果?_____________________________________。
(6)若反应生成的CO2和CO在相同条件下的体积比为2:1,则蔗糖炭化后体积膨胀发生反应的化学方程式可能为_____________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在铜与浓硫酸的反应中,如果转移0.4mol电子,则被还原的硫酸物质的量
A. 0.4mol B. 0.2mol
C. 小于0.4mol D. 小于0.2 mol
【答案】B
【解析】
铜与浓硫酸的反应中,铜元素化合价升高,失去电子,硫元素化合价降低,得到电子,得失电子总数是相等的,均为0.4mol。
Cu和浓硫酸反应方程式为Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O,由方程式可知,1mol硫酸被还原时转移电子物质的量=1mol×(6-4)=2mol,所以如果电子转移0.4mol,则被还原的硫酸的物质的量0.2mol,答案选B。
CuSO4+SO2↑+2H2O,由方程式可知,1mol硫酸被还原时转移电子物质的量=1mol×(6-4)=2mol,所以如果电子转移0.4mol,则被还原的硫酸的物质的量0.2mol,答案选B。
【点睛】
本题考查氧化还原反应的计算,侧重考查分析计算能力,知道作氧化剂的浓硫酸和转移电子的关系,明确浓硫酸的作用是解本题关键。
【题型】单选题
【结束】
18
【题目】下列离子方程式书写正确的是
A. 向Fe(OH)3中加入氢碘酸:Fe(OH)3+3H+=Fe3++3H2O
B. NH4HSO3溶液与足量的NaOH溶液混合加热:NH4++HSO3-+2OH-![]() NH3↑+SO32-+2H2O
NH3↑+SO32-+2H2O
C. 酸性条件下KIO3溶液与KI溶液发生反应生成I2:IO3-+5I-+3H2O=3I2+6OH-
D. 向FeO中加入稀硫酸:2FeO + 8H+ + SO42- =2Fe3+ + SO2 ↑+ 4H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚苹果酸(PMLA)可作为目的合成药物的载体,它的一种化学合成路线如下:
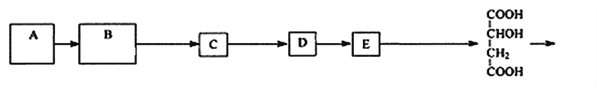
己知:琼斯试剂能选择性氧化含不饱和碳的醇,而醇中的碳碳双键或三键不受影响:RCH=CHCH2OH![]() RCH=CHCOOH
RCH=CHCOOH
回答下列问题:
(1)A的结构简式是_______________, D生成E的反应类型是______________。
(2)D中官能团的名称是______________________。在浓硫酸和加热条件下,1mol苹果酸最多能与_______mol碳酸氢钠反应。
(3)写出B → C的化学方程式:________________________________________。
(4)化合物F是B与氢气的加成产物,F的同分异构体共有_________种(不含立体异构,不包括F)。
(5)參照上述合成路线,以异戊二烯[CH2=C(CH3)CH=CH2]为原料(无机试剂任选)设计制备![]() 的合成路线:______________________。
的合成路线:______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,在某密闭容器中进行如下反应:
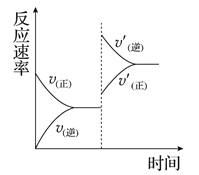
mA(g)+nB(g)![]() pC(g)+qD(g),若增大压强或升高温度,重新达到平衡,
pC(g)+qD(g),若增大压强或升高温度,重新达到平衡,
反应速率随时间的变化过程如图所示,则对该反应的叙述正确的是( )
A. 正反应是吸热反应 B. 逆反应是放热反应
C. m+n<p+q D. m+n>p+q
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com