
在含有Fe3+、Fe2+、Al3+、NH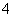 的稀溶液中加入足量Na2O2固体,充分反应后,再加入过量稀盐酸,完全反应,则离子数目没有变化的是( )
的稀溶液中加入足量Na2O2固体,充分反应后,再加入过量稀盐酸,完全反应,则离子数目没有变化的是( )
A.Fe3+、Al3+ B.Al3+
C.Fe2+、NH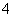 D.Fe3+
D.Fe3+
科目:高中化学 来源: 题型:
某期刊封面上的一个分子球棍模型图如图所示,图中“棍”代表单键、双键或三键,不同颜色的球代表不同元素的原子。该模型图可代表一种( )
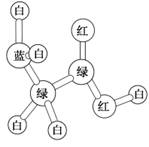
A.氨基酸 B.卤代羧酸
C.醇钠 D.酯
查看答案和解析>>
科目:高中化学 来源: 题型:
现有CuO和Fe2O3组成的混合物a g,向其中加入2 mol·L-1的硫酸溶液50 mL,恰好完全反应。若将a g该混合物在足量H2中加热,使其充分反应,冷却后剩余固体质量为( )
A.1.6a g B.(a-1.6) g
C.(a-3.2) g D.1.6 g
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关Fe2(SO4)3溶液的叙述正确的是( )
A.该溶液中,K+、Fe2+、C6H5OH、Br-可以大量共存
B.和KI溶液反应的离子方程式:Fe3++2I-===Fe2++I2
C.和Ba(OH)2溶液反应的离子方程式:Fe3++SO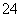 +Ba2++3OH-===Fe(OH)3↓+BaSO4↓
+Ba2++3OH-===Fe(OH)3↓+BaSO4↓
D.1 L 0.1 mol·L-1该溶液和足量的Zn充分反应,生成11.2 g Fe
查看答案和解析>>
科目:高中化学 来源: 题型:
在含有FeCl3和BaCl2的酸性溶液中,通入足量的SO2后有白色沉淀生成,过滤后,向溶液中滴加KSCN溶液,无明显现象,下列叙述不正确的是( )
A.白色沉淀是BaSO4和BaSO3
B.溶液的酸性减弱
C.白色沉淀是BaSO4
D.FeCl3全部被还原为FeCl2
查看答案和解析>>
科目:高中化学 来源: 题型:
含有砒霜(As2O3)的试样和锌、盐酸混合反应,生成的砷化氢(AsH3)在热玻璃管中完全分解成单质砷和氢气。若砷的质量为1.50 mg,则( )
A.被氧化的砒霜为1.98 mg
B.分解产生的氢气为0.672 mL
C.和砒霜反应的锌为3.90 mg
D.转移的电子总数为6×10-5NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com