
| A、常温下,0.01mol/LCH3COOH与pH=12的NaOH溶液混合,若混合后c(CH3COO-)>c(Na+),则混合液一定呈碱性 |
| B、常温下,将等体积0.01mol/LHCl与pH=12的氨水混合,则混合液的pH=7 |
| C、0.1mol/L的某二元弱酸盐Na2A溶液中,c(Na+)=2c(H2A)+2c(HA?)+2c(A2-) |
| D、将5 mL 0.02mol/L的H2SO4与5 mL 0.02mol/LNaOH溶液充分混合,若混合后溶液的体积为10mL,则混合液的pH=2 |
| 0.02mol/L×0.005L×(2-1) |
| 0.01L |
| 0.02mol/L×0.005L×(2-1) |
| 0.01L |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 族 周期 | IA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |||
查看答案和解析>>
科目:高中化学 来源: 题型:
| 盐溶液 | NaCl | Na2CO3 | NH4Cl、 | CH3COONa | Na2SO4 |
| PH值 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、等于8ml | B、大于8ml |
| C、小于8ml | D、无法判断 |
查看答案和解析>>
科目:高中化学 来源: 题型:
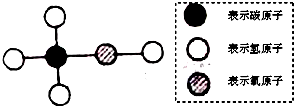
| A、甲醇的化学式为CH4O |
| B、甲醇的相对分子质量为32 |
| C、甲醇中C、H、O三种元素的质量比为1:4:1 |
| D、甲醇中氧元素的质量分数为50% |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、苯中含有苯酚(浓溴水,过滤) |
| B、苯中含有苯酚(氢氧化钠溶液、分液) |
| C、乙酸乙酯中含有乙酸(乙醇、浓硫酸、加热) |
| D、溴乙烷中含有醇(水、分液) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、c(A)=c(B)=c(C) |
| B、单位时间消耗a molA同时消耗b molB |
| C、混合气体的压强保持不变 |
| D、混合气体的密度保持不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向平衡混合物中加入少量W,正、逆反应速率均增大 |
| B、平衡后再加入1 mol X,上述反应的△H增大 |
| C、温度不变,再加入2 mol X,重新达到平衡时X的转化率大于原平衡 |
| D、当容器内混合气体的密度不变时不能证明此反应已达平衡状态 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com