
| A. | 氢氧化铁胶体 | B. | 盐酸 | C. | 氯化钠溶液 | D. | 蔗糖溶液 |
科目:高中化学 来源: 题型:选择题
| A. | 若增大压强,平衡向正方向移动,平衡常数变大 | |
| B. | 将容器体积变为20 L,Z的平衡浓度变为0.015mol/L | |
| C. | 达到平衡时X浓度为0.04 mol/L | |
| D. | 若升高温度,X的体积分数增大,则该反应的△H>0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NO2是红棕色气体,易溶于水,不是酸性氧化物 | |
| B. | NO可以用排水法收集,但不能由N2和O2直接化合而得到 | |
| C. | NO、NO2在一定条件下可相互转化,且二者都是引起光化学烟雾的大气污染物 | |
| D. | NO、NO2都有毒,且NO是汽车尾气的有害成分之一 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2Fe2++4I-+3Cl2═2Fe3++2I2+6Cl- | |
| B. | 2Fe2++4I-+4Br-+5Cl2═2Fe3++2I2+2Br2+10Cl- | |
| C. | 2Fe2++2I-+2Br-+3Cl2═2Fe3++I2+Br2+6Cl- | |
| D. | 2Fe2++2I-+2Cl2═2Fe3++I2+4Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
物质 n/mol T/℃ | 活性炭 | NO | E | F |
| 初始 | 2.030 | 0.100 | 0 | 0 |
| T1 | 2.000 | 0.040 | 0.030 | 0.030 |
| T2 | 2.005 | 0.050 | 0.025 | 0.025 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
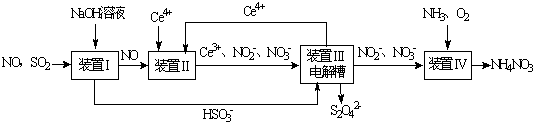
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
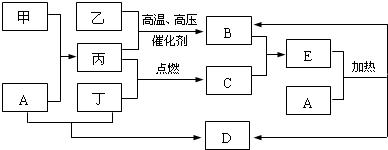
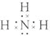 ;
;查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com