
(12分)常温下,ZnS的溶度积常数Ksp=1.20×10-23 ,H2S的电离常数K1=1.32×10-7 K2=7.10×10-15 回答下列问题:
(1)K1>>K2的原因是
(2)0.1 mol/L H2S溶液中氢离子的物质的量浓度是 (填字母)
A、等于0.1mol/L B、等于0.2mol/L
C、小于0.1mol/L D、在0.1~0.2mol/L之间
(3)0.1mol/LNa2S 溶液能使pH试纸变蓝,表明该现象的离子方程式是
(4)已知0.1mol/LNaHS溶液的pH约为9,则0.1mol/LNaHS溶液中各离子浓度由大到小的顺序是 。该溶液中的质子守恒关系式为
。
(5)向0.01mol/L的ZnCl2溶液中通入H2S(g)至饱和(c(H2S)按0.1mol/L计),为保证不产生ZnS沉淀,应控制c(H+)不低于 mol/L(已知7.811/2 =2.8)
(1)H2S第一步电离出的H+,对HS-的电离起到抑制作用,使HS-更难电离出H+
 (2)C (3)S2- +H2O
HS-+ OH-
(2)C (3)S2- +H2O
HS-+ OH-
(4)c(Na+) > c(HS-) >c(OH-) > c(H+)> c(S2-); c(H2S)+c(H+) =c(OH-)+c(S2-)
(5)0.28
【解析】(1)根据电离方程式H2S HS-+H+、HS-
HS-+H+、HS- S2-+H+可知,H2S第一步电离出的H+,对HS-的电离起到抑制作用,使HS-更难电离出H+,所以K1远大于K2。
S2-+H+可知,H2S第一步电离出的H+,对HS-的电离起到抑制作用,使HS-更难电离出H+,所以K1远大于K2。
(2)根据H2S的电离平衡常数可知,溶液中氢离子浓度是
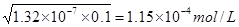 ,所以答案选C。
,所以答案选C。
(3)硫化钠是强碱弱酸盐,S2-水解显碱性。水解方程式为S2- +H2O HS-+ OH-。
HS-+ OH-。
(4)已知0.1mol/LNaHS溶液的pH约为9,说明HS-的水解程度大于HS-的电离程度,所以溶液中各离子浓度由大到小的顺序是c(Na+) > c(HS-) >c(OH-) > c(H+)> c(S2-)。根据电荷守恒c(H+) +c(Na+) ==c(HS-)+c(OH-)+2c(S2-)和物流守恒c(Na+) ==c(HS-)+c(OH-)+c(H2S)可知,质子守恒是c(H2S)+c(H+)=c(OH-)+c(S2-)。
(5)溶液中锌离子浓度是0.01mol/L,所以根据溶度积常数表达式可知,硫离子浓度是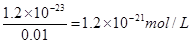 。根据电离平衡常数表达式可知
。根据电离平衡常数表达式可知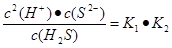 ,所以此时溶液中氢离子浓度是
,所以此时溶液中氢离子浓度是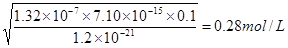 ,即溶液中氢离子不能低于0.28mol/L。
,即溶液中氢离子不能低于0.28mol/L。


 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案科目:高中化学 来源:新课程同步学案专家伴读 化学选修4(化学反应原理) 鲁科版 鲁科版 题型:013
| |||||||||||||||||||||||||||||||
查看答案和解析>>
科目:高中化学 来源: 题型:
描述弱电解质电离情况可以用电离度和电离平衡常数表示,下表是常温下几种弱电解质的电离平衡常数:
| 酸或碱 | 电离常数(Ka或Kb) |
| CH3COOH | 1.8×10-5 |
| HNO2 | 4.6×10-4 |
| HCN | 5×10-10 |
| HClO | 3×10-8 |
| NH3·H2O | 1.8×10-5 |
请回答下面问题:
(1)上述四种酸中,酸性最弱的是_______ (用化学式表示)。下列能使醋酸
溶液中CH3COOH的电离程度增大,而电离常数不变的操作是_____ (填序号)。
A.升高温度
B.加水稀释
C.加少量的CH3COONa固体
D.加少量冰醋酸
(2)CH3COONH4的水溶液呈_____ (选填“酸性”“中性”或“碱性”),理由是____________________________,溶液中各离子浓度大小的关系是_____________________。
(3)物质的量1∶1的NaCN和HCN的混合溶液,其pH>7,该溶液中离子的浓度从大
到小排列为____________________________。
(4)已知一些难溶物的溶度积常数如下表:
| 物质 | FeS | MnS | Cus | PbS | HgS | ZnS |
| Ksp | 6.3×10-18 | 2.5×10-13 | 1.3×10-36 | 3.4×10-28 | 6.4×10-55 | 1.6×10-24 |
某工业废水中含有Cu2+、Pb2+、Hg2+,最适宜向此工业废水中加入过量的 除去它们。(选填序号)
①NaOH ②FeS ③Na2S
查看答案和解析>>
科目:高中化学 来源:2011-2012学年海南省海南中学高二1班下学期期末考试化学试卷(带解析) 题型:填空题
(12分)常温下,ZnS的溶度积常数Ksp=1.20×10-23 ,H2S的电离常数K1=1.32×10-7 K2=7.10×10-15 回答下列问题:
(1)K1>>K2的原因是
(2)0.1 mol/L H2S溶液中氢离子的物质的量浓度是 (填字母)
| A.等于0.1mol/L | B.等于0.2mol/L |
| C.小于0.1mol/L | D.在0.1~0.2mol/L之间 |
查看答案和解析>>
科目:高中化学 来源:2013届山东省潍坊市高二寒假作业化学(三)试卷 题型:填空题
描述弱电解质电离情况可以用电离度和电离平衡常数表示,下表是常温下几种弱电解质的电离平衡常数:
|
酸或碱 |
电离常数(Ka或Kb) |
|
CH3COOH |
1.8×10-5 |
|
HNO2 |
4.6×10-4 |
|
HCN |
5×10-10 |
|
HClO |
3×10-8 |
|
NH3·H2O |
1.8×10-5 |
请回答下面问题:
(1)上述四种酸中,酸性最弱的是_______ (用化学式表示)。下列能使醋酸
溶液中CH3COOH的电离程度增大,而电离常数不变的操作是_____ (填序号)。
A.升高温度
B.加水稀释
C.加少量的CH3COONa固体
D.加少量冰醋酸
(2)CH3COONH4的水溶液呈_____ (选填“酸性”“中性”或“碱性”),理由是____________________________,溶液中各离子浓度大小的关系是_____________________。
(3)物质的量1∶1的NaCN和HCN的混合溶液,其pH>7,该溶液中离子的浓度从大
到小排列为____________________________。
(4)已知一些难溶物的溶度积常数如下表:
|
物质 |
FeS |
MnS |
Cus |
PbS |
HgS |
ZnS |
|
Ksp |
6.3×10-18 |
2.5×10-13 |
1.3×10-36 |
3.4×10-28 |
6.4×10-55 |
1.6×10-24 |
某工业废水中含有Cu2+、Pb2+、Hg2+,最适宜向此工业废水中加入过量的 除去它们。(选填序号)
①NaOH ②FeS ③Na2S
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com