
 、
、 、
、 烯烃的名称:
烯烃的名称:分析 分子式是C5H10的烃一定条件下与足量H2反应生成的物质为戊烷,戊烷有三种同分异构体,分别找出每一种同分异构体中分别去掉相邻碳上的两个H后得到的分子式为C5H10烯烃的同分异构体的个数,最后对符合条件的烯烃命名.
解答 解:分子式是C5H10的烃一定条件下与足量H2反应生成的物质为戊烷,戊烷有三种同分异构体,分别去掉相邻碳上的两个H后得到分子式为C5H10的烯烃,
其中正戊烷有两种,新戊烷没有,异戊烷有3种,分别是 1-甲基-1-丁烯,
1-甲基-1-丁烯, 2-甲基-2-丁烯,
2-甲基-2-丁烯, 3-甲基-1-丁烯,
3-甲基-1-丁烯,
故答案为: 、
、 、
、 ;1-甲基-1-丁烯、2-甲基-2-丁烯、3-甲基-1-丁烯.
;1-甲基-1-丁烯、2-甲基-2-丁烯、3-甲基-1-丁烯.
点评 本题考查了有机物的推断,涉及烷烃和烯烃的同分异构体的书写和烯烃的系统命名法,难度不大,本题应采用逆推法进行分析.


科目:高中化学 来源: 题型:选择题
| A. | ①③⑤⑦⑨ | B. | ②④⑥⑧⑩ | C. | ②⑦⑧⑩ | D. | ②⑤⑧⑩ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
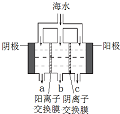 海洋是丰富的资源宝库,通过海水的综合利用可获得许多物质供人类使用.
海洋是丰富的资源宝库,通过海水的综合利用可获得许多物质供人类使用.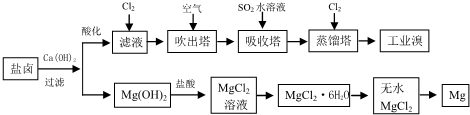
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | KOH溶液与AlCl3溶液 | B. | NaAlO2溶液与盐酸 | ||
| C. | NaHCO3溶液与盐酸 | D. | Na2CO3溶液与盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 ,化合物C所含官能团的名称为羧基.
,化合物C所含官能团的名称为羧基. ,反应类型:氧化反应.
,反应类型:氧化反应. ,写出反应②的反应方程式(标明反应条件):CH3CH2OH$→_{△}^{浓H_{2}SO_{4}}$H2O+CH2=CH2↑.
,写出反应②的反应方程式(标明反应条件):CH3CH2OH$→_{△}^{浓H_{2}SO_{4}}$H2O+CH2=CH2↑.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某学习小组依据SO2具有还原性,推测SO2能被Cl2氧化生成SO2Cl2.
某学习小组依据SO2具有还原性,推测SO2能被Cl2氧化生成SO2Cl2.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CuSO4与Ba(OH)2溶液反应:Ba2++SO42-═BaSO4↓ | |
| B. | AlCl3溶液中加入过量的浓氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O | |
| C. | 用小苏打治疗胃酸过多:HCO3-+H+═H2O+CO2↑ | |
| D. | 醋酸钠和盐酸混合:CH3COONa+H+═CH3COOH+Na+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
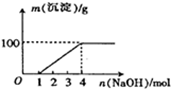
| A. | Mg2+、H+、NO3- | B. | Mg2+、Fe3+、H+、NO3- | ||
| C. | Fe3+、H+、NO3- | D. | Cu2+、H+、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al | B. | Na | C. | Cu | D. | Fe |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com