
下列各组元素的性质递变情况错误的是 ( )
A.Li、C、O原子最外层电子数依次增加
B.P、S、Cl元素最高正化合价依次升高
C.N、O、F原子半径依次增大
D.Li、Na、K的金属性依次增强
科目:高中化学 来源: 题型:
X、Y、Z为前四周期元素,且原子序数依次增大。X与氢元素可形成:H2X、H2X2两种化合物,且在常温下均为液态;Y基态原子的M层电子数是K层的3倍;Z2+的3d轨道中有10个电子。请回答下列问题:
(1)X所在周期中第一电离能最大的主族元素是_______(填元素符号);H2X2分子中X原子的杂化方式是_______。
(2)Y与X可形成YX42-。
①YX42-的立体构型是_____________。
 ②写出一种与YX42-互为等电子体分子的化学式__________。
②写出一种与YX42-互为等电子体分子的化学式__________。
(3)Z的氯化物与氨水反应可形成配合物[Z(NH3)4]Cl2,1 mol该配合物中含有σ键的数目为_____________。
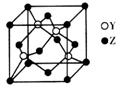
(4)Y与Z形成化合物晶体的晶胞如图所示。已知该晶体的密度为a g·cm-3,则该晶胞的体积为___________cm3(NA表示阿伏加德罗常数的值)。
查看答案和解析>>
科目:高中化学 来源: 题型:
21世纪是钛的世纪。在800℃~1 000℃时电解TiO2可制得钛,装置如右图所示。下列叙述正确的是
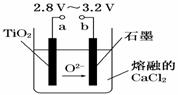 A.a为电源的正极
A.a为电源的正极
B.石墨电极上发生还原反应
C.阴极发生的反应为:TiO2+4e-===Ti+2O2-
D.每生成0.1 mol钛,转移电子0.2 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
已知短周期元素的离子aA2+、bB+、cC3-、dD-都具有相同的电子层结构,则下列叙述正确的是 ( )
A 原子半径A>B>D>C B 原子序数d>c>b>a
C 离子半径C>D>B>A D 单质的还原性A>B>D>C
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法错误的是
A.煤的气化、液化和干馏都属于化学变化 B.石油的裂化可以提高轻质油的产量和质量
C.石油分馏可获得乙烯、丙烯 D.苯等有机物是从煤干馏产物中分离出来的
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA表示阿伏加德罗常数,下列叙述中正确的是( )
A.1molSiO2晶体内含有2NA个Si—O键
B.在0.1mol熔融KHSO4中,含有0.1NA个SO42-
C.在0.5L 1mol·L-1的盐酸中所含粒子总数为NA
D.1molSi晶体内含有2NA个Si—Si键
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com