
利用如图所示装置进行下列实验,能得出相应实验结论的是( )
| 选项 | ① | ② | ③ | 实验结论 |
|
| A | 浓盐酸 | MnO2 | NaOH | 制氯气并吸收尾气 | |
| B | 浓硫酸 | 蔗糖 | 溴水 | 浓硫酸具有脱水性、氧化性 | |
| C | 稀盐酸 | Na2SO3 | Ba(NO3)2溶液 | SO2与可溶性钡盐均可生成白色沉淀 | |
| D | 浓硝酸 | Na2CO3 | Na2SiO3溶液 | 酸性:硝酸>碳酸>硅酸 |
|
| A. | A | B. | B | C. | C | D. | D |
| 实验装置综合.. | |
| 专题: | 实验评价题. |
| 分析: | A.二氧化锰与浓盐酸反应需要加热; B.浓硫酸具有脱水性及强氧化性,蔗糖脱水得到C与浓硫酸发生氧化还原反应生成二氧化硫,二氧化硫与溴水发生氧化还原反应生成硫酸和HBr; C.稀盐酸与亚硫酸钠生成二氧化硫,在③中二氧化硫与Ba(NO3)2溶液发生氧化还原反应生成硫酸钡; D.浓硝酸易挥发,则③中可能发生硝酸与硅酸钠的反应. |
| 解答: | 解:A.二氧化锰与浓盐酸反应需要加热,图中缺少加热装置,故A错误; B.蔗糖与浓硫酸混合,蔗糖脱水得到C与浓硫酸发生氧化还原反应生成二氧化硫,二氧化硫与溴水发生氧化还原反应生成硫酸和HBr,则由实验可知浓硫酸具有脱水性、氧化性,故B正确; C.稀盐酸与亚硫酸钠生成二氧化硫,在③中二氧化硫与Ba(NO3)2溶液发生氧化还原反应生成硫酸钡,则结论不合理,如二氧化硫与氯化钡不反应,故C错误; D.浓硝酸易挥发,则③中可能发生硝酸与硅酸钠的反应,则不能比较酸性碳酸>硅酸,故D错误; 故选B. |
| 点评: | 本题考查实验装置的综合应用,为高频考点,涉及物质的制备、酸性比较、氧化还原反应等,把握实验装置的作用为解答的关键,侧重分析、实验能力的考查,题目难度中等. |


 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案科目:高中化学 来源: 题型:
已知硫酸的第一步电离(H2SO4 = H++HSO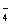 )是完全的,但第二步电离(HSO
)是完全的,但第二步电离(HSO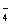
 H+ + SO
H+ + SO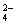 )并不完全。如果25℃时,01 mol·L-1 H2SO4溶液中c(SO
)并不完全。如果25℃时,01 mol·L-1 H2SO4溶液中c(SO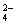 ) = 0.010 mol·L-1,01 mol·L-1 NaHSO4溶液中c(SO
) = 0.010 mol·L-1,01 mol·L-1 NaHSO4溶液中c(SO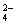 ) = 0.029 mol·L-1,试回答:
) = 0.029 mol·L-1,试回答:
(1)25℃时,01 mol·L-1 H2SO4溶液中pH = ;(可用对数表示)
(2)为何01 mol·L-1 的H2SO4 溶液中的c(SO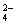 )比01 mol·L-1 的NaHSO4 溶液中c(SO
)比01 mol·L-1 的NaHSO4 溶液中c(SO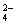 ) 小?
) 小?
(3)0.1 mol·L-1 Na2SO4溶液的pH值 7(填大于、小于或等于)
(4)固体NaHSO4与固体食盐混和共热至600℃,能否得到HCl气体?为什么?
(5)常温下测得0.25 mol·L-1的CuSO4溶液的pH值为5,025 mol·L-1 Cu(ClO4)2溶液的pH值为45,其原因是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
I2(g)+H2(g) 2HI(g) △H<0,在其他条件不变的情况下正确说法是 ( )
2HI(g) △H<0,在其他条件不变的情况下正确说法是 ( )
A.加入催化剂,改变了反应的途径,反应的△H也随之改变
B.改变压强,平衡不发生移动,反应放出的热量不变
C.升高温度,反应速率加快,反应放出的热量不变
D.若在原电池中进行,反应放出的热量不变
查看答案和解析>>
科目:高中化学 来源: 题型:
蛇纹石可用于生产氢氧化镁,简要工艺流程如下:
I.制取粗硫酸镁:用酸液浸泡蛇纹石矿粉,过滤;并在常温常压下结晶,制得粗硫酸镁(其中常含有少量Fe3+、Al3+、Fe2+等杂质离子)。
II.提纯粗硫酸镁:将粗硫酸镁在酸性条件下溶解,加入适量的0.1 mol·L—1 H2O2溶液,再调节溶液pH至7~8,并分离提纯。
III.制取氢氧化镁:向步骤II所得溶液中加入过量氨水。已知:金属离子氢氧化物沉淀所需pH是
| Fe3+ | Al3+ | Fe2+ | Mg2+ | |
| 开始沉淀时 | 1.5 | 3. 3 | 6.5 | 9.4 |
| 沉淀完全时 | 3.7 | 5.2 | 9.7 | 12.4 |
请回答:
(1)步骤II中,可用于调节溶液pH至7~8的最佳试剂是 (填字母序号)。
A.MgO B.Na2CO3 C.蒸馏水
(2)Fe2+与H2O2溶液反应的离子方程式为 。
(3)工业上常以Mg2+的转化率为考察指标,确定步骤III制备氢氧化镁工艺过程的适宜条件。其中,反应温度与Mg2+转化率的关系如图所示。
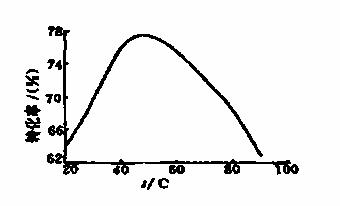
①步骤III中制备氢氧化镁反应的离子方程式为 。
②根据图中所示50℃前温度与Mg2+转化率之间的关系,可判断此反应是
(填“吸热”或“放热”)反应。
③图中,温度升高至50℃以上Mg2+转化率下降的可能原因是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
用石墨做电极电解1mol/L CuSO4溶液,当c(Cu2+)为0.5mol/L时,停止电解,向剩余溶液中加入下列何种物质可使电解质溶液恢复至原来状况( )
|
| A. | CuSO4 | B. | CuO | C. | Cu(OH)2 | D. | CuSO4•5H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关说法正确的是( )
|
| A. | 将0.2mol/L的NH3•H2O与0.1mol/L的HCl溶液等体积混合后PH>7,则c(Cl﹣)>c(NH4+)>c(OH﹣)>c(H+) |
|
| B. | 已知MgCO3的Ksp=6.82×10﹣6,则所有含有固体MgCO3的溶液中,都有C(Mg2+)=C(CO32﹣),且C(Mg2+)•C(CO32﹣)═6.82×10﹣6 mol•L﹣1 |
|
| C. | 0.1mol/LNa2CO3与0.1mol/LNaHCO3溶液等体积混合: c(Na+)=c(CO32﹣)+c(HCO3﹣)+c(H2CO3) |
|
| D. | 用惰性电极电解Na2SO4溶液,阳阴两极产物的物质的量之比为2:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是
A.SO2和NO2都是酸性氧化物,都能与水反应生成酸
B.Na2O和Na2O2组成元素相同,与CO2反应产物也完全相同
C.Al2O3和Na2O按物质的量比1:1投人水中可得到澄清溶液
D.金属铝排在金属活动性顺序表中氢元素的前面,铝与强酸反应一定放出氢气
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是
A.石墨比金刚石稳定,故石墨转化为金刚石的反应可以自发进行
B.吸热反应能自发进行的原因是从外界获得了能量
C.SiO2常温下可以与NaOH溶液和HF溶液反应,说明其具有两性
D.反应A(g)+B(g)=2C(s)可以自发进行,则其必为放热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
某实验报告记录了如下数据,其中数据合理的是
A.用温度计测量出酒精的沸点为78.5℃
B.用50mL量筒量取23.00 mL浓盐酸
C.用广泛pH试纸测得氯水的pH值为2.1
D.用托盘天平称量氧化铜粉末为11.70g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com