
| A. | 加入H+能产生无色无味气体的溶液:OH-、K+、I-、SO32- | |
| B. | 在加入铝粉能产生H2的溶液中:NH4+、Fe2+、SO42-、NO3- | |
| C. | 0.1 mol•L-1NH4HCO3溶液中:K+、Na+、NO3-、Cl- | |
| D. | 在澄清透明的无色溶液中:Na+、Cu2+、Cl-、NO3- |
分析 A.加入H+能产生无色无味气体的溶液可能含CO32-或HCO3-,HCO3-与OH-反应;
B.加入铝粉能产生H2的溶液,为非氧化性酸或强碱溶液;
C.该组离子之间不反应;
D.Cu2+为蓝色.
解答 解:A.加入H+能产生无色无味气体的溶液若含HCO3-,HCO3-与OH-反应不能共存,故A不选;
B.加入铝粉能产生H2的溶液,为非氧化性酸或强碱溶液,碱性溶液中不能大量存在NH4+、Fe2+,酸溶液中Al或Fe2+、NO3-发生氧化还原反应不生成氢气,故B不选;
C.该组离子之间不反应,可大量共存,故C选;
D.Cu2+为蓝色,与无色不符,故D不选;
故选C.
点评 本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重分析与应用能力的考查,注意复分解反应的判断,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 35.5g氯气所含的分子数为6.02×1023 | |
| B. | 常温常压下,22.4L氨气所含原子总数为4×6.02×1023 | |
| C. | 反应每生成1molN2转移电子数约为6×6.02×1023 | |
| D. | 1mol•L-1NH4Cl溶液中,含有Cl-数约为6.02×1023 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
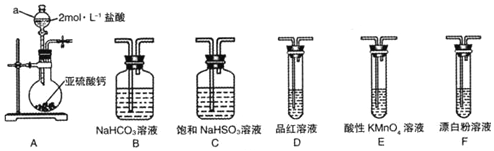
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 稀释浓硫酸时,将水沿器壁慢慢注入酸中 | |
| B. | 点燃氢气前,先检验氢气的纯度 | |
| C. | 加热液体时,试管口不对着人 | |
| D. | 利用丁达尔效应区别胶体和溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2NaBr+Cl2═Br2+2NaCl | |
| B. | AlCl3+3NaAlO2+6H2O═4Al(OH)3↓+3NaCl | |
| C. | 2H2S+SO2═3S↓+2H2O | |
| D. | Cl2+H2O═HCl+HClO |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
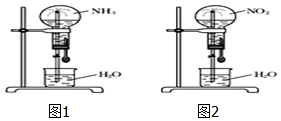 标准状况下,两个等体积的干燥圆底烧瓶中分别充满:①NH3②NO2,进行喷泉实验.下列说法正确的是( )
标准状况下,两个等体积的干燥圆底烧瓶中分别充满:①NH3②NO2,进行喷泉实验.下列说法正确的是( )| A. | 最终液体均能充满烧瓶 | |
| B. | 若在烧杯中的水中滴加酚酞,均能看到美丽的红色喷泉 | |
| C. | 实验结束后,烧瓶中的溶液的浓度均约为0.045mol/L | |
| D. | 喷泉的原理均是气体极易溶于水,使烧瓶内的压强减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 浓氨水中滴加FeCl3饱和溶液可制得Fe(OH)3胶体 | |
| B. | 煎炸食物的花生油和牛油都是可皂化的饱和酯类 | |
| C. | 福尔马林、水玻璃、氨水均为混合物 | |
| D. | KClO3和SO3溶于水后能导电,故KClO3和SO3为电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 水分子间存在氢键,所以水常温下以液态存在并且化学性质非常稳定 | |
| B. | 常温、常压下以液态存在的物质一定都是由分子构成,因此该液体一般无法导电 | |
| C. | 硫酸钾在熔融状态下离子键被削弱,形成定向移动的离子,从而导电 | |
| D. | 冰醋酸晶体溶于水的过程中即破坏了分子间作用力,也破坏了部分分子内作用力 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe3O4溶于足量稀 HNO3 中:Fe3O4+8H+═Fe2++ZFe3++4H2O | |
| B. | NH4HCO3溶液与足量 NaOH 溶液混合:HCO3-+OH-═CO32-+H2O | |
| C. | 将过量的 SO2 通入 NaClO 溶液中:SO2+ClO-+H2O═HClO+HSO3- | |
| D. | 将 0.2mol•L-1KA1(SO4)2 溶液与 0.3mol•L-1Ba(OH)2溶液等体积混合:2Al3++3SO42-+3Ba2++6OH-═2Al(OH)3↓+3BaSO4↓ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com