
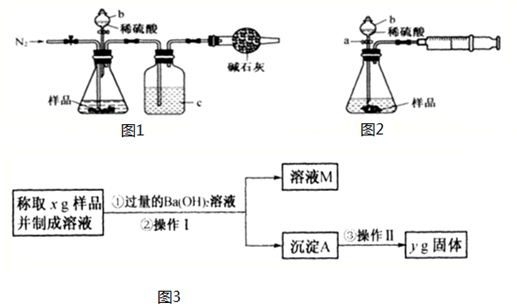
分析 (1)硫酸和样品中的碳酸钠反应生成二氧化碳气体,仪器b是加入液体的仪器可以控制加入的量,应是分液漏斗,浓硫酸具有吸水性,二氧化碳是酸性气体不和浓硫酸发生反应;
(2)①改变瓶内气体的多少而改变瓶内压强,压强增大,瓶内液体则会被压入长颈漏斗内,b下端玻璃管中液面上升,可以说明装置气密性良好;
②装置中加入硫酸和碳酸钠反应生成二氧化碳,注射器活塞被向外推出,可以测定二氧化碳的体积;
(3)①流程分析可知,加入氢氧化钡溶液和碳酸钠 反应生成碳酸钡沉淀;
②沉淀质量计算物质的量,碳元素守恒计算碳酸钠质量,得到样品中碳酸钠的质量分数;
(4)依据CO2+2KOH═K2CO3+H2O CO2+KOH═KHCO3,n(CO2):n(KOH)=1:2,产物为K2CO3,n(CO2):n(KOH)=1:1,产物为KHCO3,以此计算.
解答 解:(1)依据装置和试剂分析,硫酸和样品中的碳酸钠反应,仪器b是加入液体的仪器可以控制加入的量,是分液漏斗;反应过程中含有水蒸气,可以利用浓硫酸干燥二氧化碳气体,
故答案为:Na2CO3;分液漏斗;除去CO2中的水蒸气;
(2)①使用注射器改变瓶内气体的多少而改变瓶内压强;当将针筒活塞向内推压时,瓶内气体被压缩,压强增大,瓶内液体则会被压入长颈漏斗内,b下端玻璃管中液面上升,可以说明装置气密性良好,故答案为:液面;
②在实验完成时,反应后可以利用注射器读取生成气体的体积,能直接测得的数据是CO2的体积,故答案为:体积;
(3)①流程分析可知,加入氢氧化钡溶液和碳酸钠 反应生成碳酸钡沉淀,通过过滤得到沉淀,洗涤后称重得到沉淀碳酸钡质量,
故答案为:过滤;称量;
②流程分析判断沉淀质量为Yg,物质的量=$\frac{yg}{197g/mol}$=$\frac{y}{197}$mol;碳酸钠物质的量和碳酸钡物质的量相同,样品质量为Xg,则碳酸钠质量为 $\frac{y}{197}$mol×106g/mol;
所以碳酸钠的质量分数=$\frac{\frac{106y}{197}mol}{x}$×100%,故答案为:$\frac{106y}{197x}$×100%;
(4)CO2+2KOH═K2CO3+H2O CO2+KOH=KHCO3,n(CO2):n(KOH)=1:2,产物为K2CO3,n(CO2):n(KOH)=1:1,产物为KHCO3,标准状况下,将672mL CO2气体物质的量=$\frac{0.672L}{22.4L/mol}$=0.03mol;通入50mL 1mol/L KOH溶液中,n(KOH)=0.05L×1mol/L=0.05mol,n(CO2):n(KOH)=0.03:0.05=3:5,所以1:2<3:5<1:1,二氧化碳和氢氧化钾全部反应生成碳酸钾和碳酸氢钾,利用直平法写出反应的化学方程式为:3CO2+5KOH═KHCO3+2K2CO3+2H2O,则n(K2CO3):n(KHCO3)=2:1,
故答案为:2:1.
点评 本题考查了物质性质的实验验证和含量测定方法分析判断,混合物中物质质量分数的计算方法和应用,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | Fe和Zn | B. | Mg和Al | C. | Fe、Cu、Zn | D. | Mg、Fe、Cu |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1,3-丁二烯的分子式:C4H6 | B. | 溴乙烷的电子式: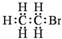 | ||
| C. | 甲醛的结构式: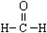 | D. | 葡萄糖的结构简式:CH2OH(CHOH)4CHO |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下的33.6L氯气与27g铝充分反应,转移电子数为3NA | |
| B. | 标准状况下,22.4LNO和11.2L氧气混合,气体的分子总数为1.5 NA | |
| C. | 7.8 g Na2O2含有的阴离子数目为0.1 NA | |
| D. | 80mL10mol/L的浓盐酸与足量MnO2反应,转移电子数为0.4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com