
”¾ĢāÄæ”æÉčNAĪŖ°¢·ü¼ÓµĀĀŽ³£ŹżµÄÖµ£¬ĻĀĮŠŠšŹö“ķĪóµÄŹĒ

A£®ŗ¬16 gŃõŌ×ӵĶžŃõ»Æ¹č¾§ĢåÖŠŗ¬ÓŠµÄ¦Ä¼üŹżÄæĪŖ2NA
B£®23.4 g NaCl¾§ĢåÖŠŗ¬ÓŠ0.1NAøöČēĶ¼ĖłŹ¾µÄ½į¹¹µ„ŌŖ
C£®³£ĪĀ³£Ń¹ĻĀ£¬5 g D2Oŗ¬ÓŠµÄÖŹ×ÓŹż”¢µē×ÓŹż”¢ÖŠ×ÓŹż¾łĪŖ2.5NA
D£®2 mol SO2ŗĶ1 mol O2ŌŚŅ»¶ØĢõ¼žĻĀ·“Ó¦ĖłµĆ»ģŗĻĘųĢå·Ö×ÓŹżŠ”ÓŚ2NA
”¾“š°ø”æD
”¾½āĪö”æ
ŹŌĢā·ÖĪö£ŗA”¢øł¾Ż¶žŃõ»Æ¹čµÄ¾§Ģå½į¹¹ÖŠ1molSiO2¾§ĢåÖŠŗ¬ÓŠ4mol¦Ä¼ü£¬ŗ¬16 gŃõŌ×ӵĶžŃõ»Æ¹č¾§ĢåµÄĪļÖŹµÄĮæĪŖ0.5mol£¬ŗ¬ÓŠµÄ¦Ä¼üŹżÄæĪŖ2NA £¬ÕżČ·£»B”¢øł¾ŻĀČ»ÆÄĘµÄ¾§°ūĄūÓĆĒŠøī·Ø·ÖĪö1mol¾§°ūÖŠŗ¬ÓŠ4molNa+ŗĶ4molCl”Ŗ£¬23.4 g NaClµÄĪļÖŹµÄĮæĪŖ0.4mol£¬ŗ¬ÓŠ0.4molNa+ŗĶ0.4molCl”Ŗ£¬¾§ĢåÖŠŗ¬ÓŠ0.1NAøö½į¹¹µ„ŌŖ£¬ÕżČ·£»C”¢1mol D2Oŗ¬ÓŠµÄÖŹ×ÓŹż”¢µē×ÓŹż”¢ÖŠ×ÓŹż¾łĪŖ10NA£¬D2OµÄĦ¶ūÖŹĮæĪŖ20g/mol£¬³£ĪĀ³£Ń¹ĻĀ£¬5 g D2OµÄĪļÖŹµÄĮæĪŖ0.25mol£¬ŗ¬ÓŠµÄÖŹ×ÓŹż”¢µē×ÓŹż”¢ÖŠ×ÓŹż¾łĪŖ2.5NA£¬ÕżČ·£»D”¢·“Ó¦2SO2+O2![]() 2SO3ĪŖæÉÄę·“Ó¦£¬æÉÄę·“Ó¦²»ÄܽųŠŠµ½µ×£¬¹Ź2 mol SO2ŗĶ1 mol O2ŌŚŅ»¶ØĢõ¼žĻĀ·“Ó¦ĖłµĆ»ģŗĻĘųĢå·Ö×ÓŹż“óÓŚ2NA£¬“ķĪó”£
2SO3ĪŖæÉÄę·“Ó¦£¬æÉÄę·“Ó¦²»ÄܽųŠŠµ½µ×£¬¹Ź2 mol SO2ŗĶ1 mol O2ŌŚŅ»¶ØĢõ¼žĻĀ·“Ó¦ĖłµĆ»ģŗĻĘųĢå·Ö×ÓŹż“óÓŚ2NA£¬“ķĪó”£


 ²½²½øß“ļ±ź¾ķĻµĮŠ“š°ø
²½²½øß“ļ±ź¾ķĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀ±ķĮŠ³öĮĖ¢Ł”«¢į¾ÅÖÖŌŖĖŲŌŚÖÜĘŚ±ķÖŠµÄĪ»ÖĆ”£

Ēė°“ŅŖĒó»Ų“šĻĀĮŠĪŹĢā£ŗ
(1)ŌŖĖŲ¢ßµÄŌ×Ó½į¹¹Ź¾ŅāĶ¼______________________”£¢Ł”¢¢Ü°“Ō×ÓøöŹż±ČĪŖ1£ŗ1×é³ÉµÄ·Ö×ӵĵē×ÓŹ½____________________£»ÓÉ¢Ś”¢¢ÜĮ½ÖÖŌŖĖŲ×é³ÉµÄŅ»ÖÖ»ÆŗĻĪļµÄ½į¹¹Ź½________________£»
(2)¢Ż¢ŽĮ½ÖÖŌŖĖŲµÄŌ×Ó°ė¾¶Óɓ󵽊”µÄĖ³ŠņŹĒ____________£ØĢīŌŖĖŲ·ūŗÅ£©”£
(3)¢ąŗĶ¢įĮ½ÖÖŌŖĖŲµÄ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦µÄĖ®»ÆĪļÖŠĖįŠŌ½ĻČõµÄŹĒ________£ØĢī»ÆѧŹ½£©”£
(4)ŌŖĖŲ¢ŪµÄĘųĢ¬Ēā»ÆĪļŗĶŌŖĖŲ¢ąµÄĘųĢ¬Ēā»ÆĪļŅ×ÓŚÖʱøµÄŹĒ___________£ØĢī»ÆѧŹ½£©”£
(5)ŌŖĖŲ¢ŻµÄ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦µÄĖ®»ÆĪļÓėŌŖĖŲ¢ßµÄ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦Ė®»ÆĪļ·“Ó¦£¬ĘäĄė×Ó·½³ĢŹ½ĪŖ_________________________________________”£
(6)ŌŖĖŲ¢Ł”¢¢Ü”¢¢ŻĮ½Į½Ö®¼äæÉŅŌŠĪ³ÉĮ½ÖÖĄąŠĶµÄ»ÆŗĻĪļ£¬Š“³öŅ»ÖÖ¹²¼Ū»ÆŗĻĪļµÄ»ÆѧŹ½__________________ £»Ņ»ÖÖĄė×Ó»ÆŗĻĪļµÄ»ÆѧŹ½_________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æij¹¤³§µÄ¹¤Ņµ·ĻĖ®ÖŠŗ¬ÓŠ“óĮæµÄ”°FeSO4”±”¢½Ļ¶ąµÄCu2+ŗĶÉŁĮæµÄNa+”£ĪŖĮĖ¼õÉŁĪŪČ¾±ä·ĻĪŖ±¦£¬¹¤³§¼Ę»®“ÓøĆ·ĻĖ®ÖŠ»ŲŹÕĮņĖįŃĒĢśŗĶĶ”£øł¾ŻĮ÷³ĢĶ¼£¬Ķź³É»ŲŹÕĮņĖįŃĒĢśŗĶĶµÄ¼ņµ„ŹµŃé·½°ø”£»Ų“šĻĀĮŠĪŹĢā£ŗ

(1)¼ÓČėŌĮĻ¢ŁĪŖ____________£»²Ł×÷¢ŚµÄĆū³ĘĪŖ___________£¬øĆ²Ł×÷ĖłÓƵ½µÄ²£Į§ŅĒĘ÷Ö÷ŅŖÓŠ______”£
(2)¹ĢĢåAĪŖ____________£»
(3)Š“³ö¼ÓČėŌĮĻ¢ŁŗĶ¢ŚÓŠ¹Ų·“Ó¦µÄĄė×Ó·½³ĢŹ½__________________”¢________________________”£
(4)²Ł×÷¢Ū»ńµĆFeSO4”¤7H2O£¬ŠčŅŖ¾¹ż_____”¢_____”¢¹żĀĖµČ²Ł×÷”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ2017Äź5ŌĀ£¬ÖŠ¹ś¶Ō”°æÉČ¼±ł”±ŹŌ²É³É¹¦”£”°æÉČ¼±ł”±ŹĒĢģČ»ĘųĖ®ŗĻĪļ£¬±»³ĘĪŖĪ“Ą“ŠĀÄÜŌ“”£»Ų“šĻĀĮŠĪŹĢā£ŗ
(1)ÓĆCu2Al2O4×÷“߻ƼĮÖʱøŅŅĖį
ŅŃÖŖ£ŗ![]() £¬ø÷ĪļÖŹĻą¶ŌÄÜĮæ“óŠ”ČēĶ¼”£
£¬ø÷ĪļÖŹĻą¶ŌÄÜĮæ“óŠ”ČēĶ¼”£
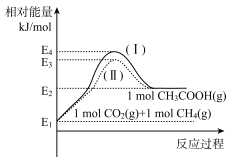
¢Ła=____”£
¢Ś·“Ó¦ĪļµÄ»ī»Æ·Ö×ÓÅØ¶Č“óŠ”£ŗ¹ż³ĢI___ ¹ż³Ģ¢ņ£ØĢī”°“óÓŚ”±”¢”°Š”ÓŚ”±»ņ”°µČÓŚ”±£©”£
(2)¼×Ķ鳬øÉ“ß»ÆÖŲÕū(DRM)ÖʱøCO£¬ŌŚNi”¢CaO¼°Fe3O4µÄ¹²Ķ¬“ß»Æ×÷ÓĆĻĀ£¬æÉŅŌ»ńµĆ¼«øßÅØ¶ČµÄCO£¬Ę仜ĄķČēĻĀ£ŗ
µŚ¢Ł²½£ŗNi»ł“ß»Æ![]()
µŚ¢Ś²½£ŗFeµÄ»¹Ō![]()
µŚ¢Ū²½£ŗCO2µÄ²¶»ń![]()
µŚ¢Ü²½£ŗCO2µÄŹĶ·ÅÓė»¹Ō![]()
Éč¼ĘµŚ¢Ś²½ÓėµŚ¢Ū²½·“Ó¦ÓŠĄūÓŚŹµĻÖĒāĪļÖÖÓė____µÄ³¹µ×·ÖĄė£¬“ÓĄÕĻÄĢŲĮŠŌĄķµÄ½Ē¶Čæ“£¬ÕāŅ²ÓŠĄūÓŚ____£»¹ż³Ģ¢ŁÖŠ£¬µ±Ķ¶ĮĻ±Č![]() = ___Ź±£¬²ÅÄܱ£³Ö“߻ƼĮ×é³É²»±ä”£
= ___Ź±£¬²ÅÄܱ£³Ö“߻ƼĮ×é³É²»±ä”£
(3)¼×Ķé“ß»ÆÖŲÕūÓėŃ¹ĒæµÄ¹ŲĻµ
ŅŃÖŖ£ŗ![]() £¬ĻÖÓŠĪĀ¶ČĻąĶ¬µÄI”¢¢ņ”¢¢óČżøöŗćŃ¹ĆܱÕČŻĘ÷£¬¾łŅŃ³äČė1 mol CH4(g)ŗĶ1 mol CO2 (g)£¬ČżøöČŻĘ÷µÄ·“Ó¦Ń¹Ēæ·Ö±šĪŖP1 atm”¢P2 atm”¢P3 atm£¬ŌŚĘäĖūĢõ¼žĻąĶ¬µÄĒéæöĻĀ£¬·“Ó¦¾ł½ųŠŠµ½t minŹ±£¬CO2)µÄĘ½ŗāĢå»ż·ÖŹż¦Õ(CO2)ČēĻĀ×óĶ¼£¬“ĖŹ±I”¢¢ņ”¢¢óČżøöČŻĘ÷ÖŠŅ»¶Ø“¦ÓŚ»ÆŃ§Ę½ŗāדĢ¬µÄŹĒ ___£ØĢī·¬ŗÅ£©£»ĒóøĆĪĀ¶ČĢõ¼žĻĀ·“Ó¦µÄĘ½ŗā³£ŹżKp=___ £Ø¼ĘĖć±ķ“ļŹ½£©”£”¾ŅŃÖŖ£ŗKpŹĒÓĆ·ÖŃ¹Į¦“śĢęø÷ĪļÖŹµÄÅØ¶Č¼ĘĖćµÄĘ½ŗā³£Źż£¬ČĪŅ»×é·ÖBµÄ·ÖŃ¹p(B)µČÓŚ×ÜŃ¹p³ĖŅŌĖüµÄĢå»ż·ÖŹży(B)”æ
£¬ĻÖÓŠĪĀ¶ČĻąĶ¬µÄI”¢¢ņ”¢¢óČżøöŗćŃ¹ĆܱÕČŻĘ÷£¬¾łŅŃ³äČė1 mol CH4(g)ŗĶ1 mol CO2 (g)£¬ČżøöČŻĘ÷µÄ·“Ó¦Ń¹Ēæ·Ö±šĪŖP1 atm”¢P2 atm”¢P3 atm£¬ŌŚĘäĖūĢõ¼žĻąĶ¬µÄĒéæöĻĀ£¬·“Ó¦¾ł½ųŠŠµ½t minŹ±£¬CO2)µÄĘ½ŗāĢå»ż·ÖŹż¦Õ(CO2)ČēĻĀ×óĶ¼£¬“ĖŹ±I”¢¢ņ”¢¢óČżøöČŻĘ÷ÖŠŅ»¶Ø“¦ÓŚ»ÆŃ§Ę½ŗāדĢ¬µÄŹĒ ___£ØĢī·¬ŗÅ£©£»ĒóøĆĪĀ¶ČĢõ¼žĻĀ·“Ó¦µÄĘ½ŗā³£ŹżKp=___ £Ø¼ĘĖć±ķ“ļŹ½£©”£”¾ŅŃÖŖ£ŗKpŹĒÓĆ·ÖŃ¹Į¦“śĢęø÷ĪļÖŹµÄÅØ¶Č¼ĘĖćµÄĘ½ŗā³£Źż£¬ČĪŅ»×é·ÖBµÄ·ÖŃ¹p(B)µČÓŚ×ÜŃ¹p³ĖŅŌĖüµÄĢå»ż·ÖŹży(B)”æ
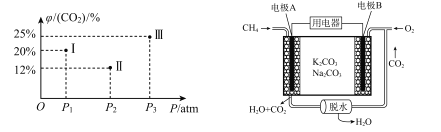
(4)¼×ĶéÓĆÓŚČ¼ĮĻµē³Ų
ŅŃÖŖ£ŗ¼×Ķéµē³ŲµÄ¹¤×÷ŌĄķČēÉĻÓŠĶ¼£¬Ōņøŗ¼«·“Ó¦·½³ĢŹ½ĪŖ ___£»µ±A¼«ĻūŗıźæöĻĀ44.8 LCH4Ź±£¬ĄķĀŪÉĻB¼«×ŖŅʵē×ÓµÄĪļÖŹµÄĮæĪŖ ___mol”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĘÆ°×¼ĮŃĒĀČĖįÄĘ(NaClO2)ŌŚ³£ĪĀÓėŗŚ°µ“¦æɱ£“ęŅ»Äź£¬ŃĒĀČĖį²»ĪȶØæÉ·Ö½ā£¬·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ£ŗ5HClO2===4ClO2”ü£«H£«£«Cl££«2H2O”£(HClO2ĪŖČõĖį)ĻņNaClO2ČÜŅŗÖŠµĪ¼ÓH2SO4£¬æŖŹ¼Ź±HClO2·Ö½ā·“Ó¦»ŗĀż£¬Ėęŗó·“Ó¦ŃøĖŁ¼Óæģ£¬ĘäŌŅņŹĒ
A. ČÜŅŗÖŠµÄCl£Ęš“ß»Æ×÷ÓĆ B. ČÜŅŗÖŠµÄH£«Ęš“ß»Æ×÷ÓĆ
C. ClO2ŅŻ³ö£¬Ź¹·“Ó¦µÄÉś³ÉĪļÅØ¶Č½µµĶ D. ŌŚĖįŠŌĢõ¼žĻĀ£¬ŃĒĀČĖįÄʵÄŃõ»ÆŠŌŌöĒæ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĪļÖŹµÄĖ®ČÜŅŗÖŠ£¬³żĮĖĖ®·Ö×ÓĶā£¬²»“ęŌŚĘäĖū·Ö×ӵďĒ
A. HNO3 B. NaHS C. HF D. NH4Cl
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æNAĪŖ°¢·ü¼ÓµĀĀŽ³£ŹżµÄÖµ”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø £©
A. ±źæöĻĀ11.2L ¼×“¼Ėłŗ¬¹²¼Ū¼üŹżĪŖ5NA
B. 1L 1mol/LĘĻĢŃĢĒČÜŅŗŗ¬ÓŠŃõŌ×ÓŹżĪŖ6NA
C. 46gŅŅ“¼ŌŚ½šŹōĶ“ß»ÆĻĀĶźČ«·“Ӧɜ³ÉŅŅČ©×ŖŅʵē×ÓŹżĪŖ2NA
D. 0.1L 12mol/L ÅØĮņĖįÓė×ćĮæZnĶźČ«·“Ó¦±źæöĻĀÉś³ÉĘųĢå1.2NA
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĀĢÉ«ÄÜŌ“ŹĒÖøŹ¹ÓĆ¹ż³ĢÖŠ²»ÅÅ·Å»ņÅŷż«ÉŁĪŪČ¾ĪļµÄÄÜŌ“£¬ĻĀĮŠ²»ŹōÓŚĀĢÉ«ÄÜŌ“µÄŹĒ
A. Ģ«ŃōÄÜ B. »ÆŹÆÄÜŌ“ C. ·ēÄÜ D. ³±Ļ«ÄÜ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĘÆ°×¼ĮŃĒĀČĖįÄĘ(NaClO2)ŌŚ³£ĪĀÓėŗŚ°µ“¦æɱ£“ęŅ»Äź£¬ŃĒĀČĖį²»ĪȶØæÉ·Ö½ā£¬·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ£ŗ5HClO2===4ClO2”ü£«H£«£«Cl££«2H2O”£(HClO2ĪŖČõĖį)ĻņNaClO2ČÜŅŗÖŠµĪ¼ÓH2SO4£¬æŖŹ¼Ź±HClO2·Ö½ā·“Ó¦»ŗĀż£¬Ėęŗó·“Ó¦ŃøĖŁ¼Óæģ£¬ĘäŌŅņŹĒ
A. ČÜŅŗÖŠµÄCl£Ęš“ß»Æ×÷ÓĆ B. ČÜŅŗÖŠµÄH£«Ęš“ß»Æ×÷ÓĆ
C. ClO2ŅŻ³ö£¬Ź¹·“Ó¦µÄÉś³ÉĪļÅØ¶Č½µµĶ D. ŌŚĖįŠŌĢõ¼žĻĀ£¬ŃĒĀČĖįÄʵÄŃõ»ÆŠŌŌöĒæ
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com