
| A. | 盐发生电离 | B. | 水的电离平衡被破坏 | ||
| C. | 溶液的 pH≠7 | D. | 有中和反应发生 |
分析 强酸弱碱盐、强碱弱酸盐可发生水解反应,盐完全电离,弱酸根离子或弱碱离子破坏水的电离平衡,且水解为吸热反应,以此来解答.
解答 解:A.绝大多数的盐为强电解质,盐存在电离过程,必定存在盐发生电离,故A正确;
B.水解时弱酸根离子或弱碱离子破坏水的电离平衡,强酸强碱盐不水解,水的电离平衡不变,故B错误;
C.25℃,溶液的pH可能为7,如强酸强碱正盐如氯化钠、弱酸弱碱盐醋酸铵溶液显中性,故C错误;
D.水解和酸碱中和反应为可逆,有弱离子水解平衡存在,可存在中和反应,强酸强碱盐溶液中不存在中和反应,故D错误;
故选A.
点评 本题考查盐类水解,为高频考点,把握水解原理及应用、水的电离平衡移动为解答的关键,侧重分析与应用能力的考查,注意选项C为解答的难点,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 淀粉、油脂及其水解产物均不属于电解质 | |
| B. | 葡萄糖可用于补钙药物制剂的合成 | |
| C. | 石油是复杂的混合物,其分馏产物为纯净物 | |
| D. | 天然气的产量用来衡量一个国家石油化工的发展水平 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
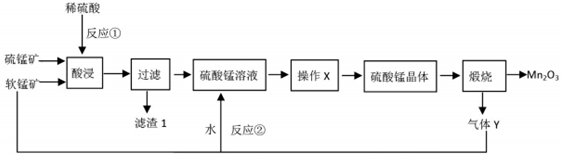
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若a>b,且c(X-)=c(Y-),则相同浓度时,酸性HX<HY | |
| B. | 若a=b,pH(NaX)>pH(NaY),则相同条件时,酸性HX<HY | |
| C. | 若a=b,且c(X-)=c(Y-)+c(HY),则相同条件时,酸性HX<HY | |
| D. | 若等体积混合,且c(X-)+c(Y-)+c(HX)+c(HY)=0.1mol/L,则一定有a+b=0.2mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 空气中:SO2、NO、N2、NH3 | |
| B. | 明矾溶液中:Na+、K+、CH3COO-、HCO3- | |
| C. | 过量铁与稀硫酸反应后的溶液中:[Fe(CN)6]3-、NH4+、Cl-、NO3- | |
| D. | 常温下,水电离出的c(H+)=1×10-12mol/L的溶液中:Ba2+、Na+、Cl-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题



 .
. .
. 有多种同分异构体,试写出所有苯环上含有1个醛基和2个羟基,且核磁共振氢谱显示为4组峰的芳香族化合物的结构简式
有多种同分异构体,试写出所有苯环上含有1个醛基和2个羟基,且核磁共振氢谱显示为4组峰的芳香族化合物的结构简式 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | a+3b | B. | $\frac{a}{2}$+3b | C. | $\frac{a}{2}$+3b+$\frac{7}{2}$ w | D. | 3(b-w) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com