
在恒容密闭容器中发生反应2SO2+O2 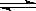 2 SO3,当其他条件不变时,只改变一个条件,将生成SO3的反应速率的变化填入下表格里(填“增大”、“减小”或“不变”)。
2 SO3,当其他条件不变时,只改变一个条件,将生成SO3的反应速率的变化填入下表格里(填“增大”、“减小”或“不变”)。
| 编号 | 改变的条件 | 生成的SO3的速率 |
| (1) | 升高温度 | |
| (2) | 充入一定量N2 | |
| (3) | 减少SO3的浓度 | |
| (4) | 使用催化剂 | |
| (5) | 压缩体积 |
 成功训练计划系列答案
成功训练计划系列答案 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案 一卷搞定系列答案
一卷搞定系列答案 名校作业本系列答案
名校作业本系列答案 轻巧夺冠周测月考直通名校系列答案
轻巧夺冠周测月考直通名校系列答案科目:高中化学 来源: 题型:
按要求完成下列问题:
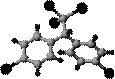
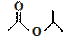 ⑴某有机物的键线式是 请写出它与NaOH溶液反应的化学方程式 ▲ :
⑴某有机物的键线式是 请写出它与NaOH溶液反应的化学方程式 ▲ :
⑵DDT人类合成的第一种有机氯农药,其分子结构球棍模型如
右图所示。请分析该物质的核磁共振1H谱图中有 ▲ 个
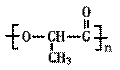 吸收峰。
吸收峰。
 ⑶)F和G( ) 是日常生活中常用的两种合成高分子材料,可由某烃 经下列反应得到。
⑶)F和G( ) 是日常生活中常用的两种合成高分子材料,可由某烃 经下列反应得到。
请回答下列问题:
①F的结构简式为 ▲ 。
②C中所含官能团的名称为 ▲ ,用 ▲ 仪,可以测定D中所含官能团。
③A→B的化学方程式为 ▲ 。
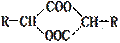
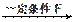 ④已知 2RCH(OH)COOH 2H2O +
④已知 2RCH(OH)COOH 2H2O +
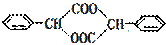 请参考题目中的合成途径,若合成 ,起始原料的某烃的结构简式为 ▲ ,最少用 ▲ 步反应,可以合成产物。
请参考题目中的合成途径,若合成 ,起始原料的某烃的结构简式为 ▲ ,最少用 ▲ 步反应,可以合成产物。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知反应:CO(g)  C(s) +
C(s) + 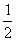 O2(g)的△H为正值,△S为负值。设△H和△S不随温度而变化,下列说法中正确的是( )
O2(g)的△H为正值,△S为负值。设△H和△S不随温度而变化,下列说法中正确的是( )
A.低温下是自发变化
B.高温下是自发变化
C.低温下是非自发变化,高温下是自发变化
D.任何温度下都是非自发变化
查看答案和解析>>
科目:高中化学 来源: 题型:
一定温度下,可逆反应2NO2  2NO+O2在恒容密闭容器中反应,达到平衡状态的标志是:
2NO+O2在恒容密闭容器中反应,达到平衡状态的标志是:
①单位时间内生成n mol O2的同时生成2n mol NO2;
②单位时间内生成n mol O2 的同时生成2n mol NO;
③混合气体的密度不再改变的状态;④混合气体的颜色不再改变的状态;
⑤密闭容器中压强不再改变的状态;
⑥混合气体的平均相对分子质量不再改变的状态。
A.②③⑤⑥ B.①④⑤⑥ C.①③④⑥ D.全部
查看答案和解析>>
科目:高中化学 来源: 题型:
下表物质与其所含化学键类型、所属化合物类型完全正确的一组是( )
| 选项 | A | B | C | D |
| 物质 | MgCl2 | CO2 | HCl | NaOH |
| 所含化学 键类型 | 离子键、 共价键 | 共价键 | 离子键 | 离子键、 共价键 |
| 所属化合 物类型 | 离子 化合物 | 共价 化合物 | 离子 化合物 | 共价 化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
将等物质的量的A、B混合于2L的密闭容器中,发生如下反应:3A(g)+B(g) XC(g)+2D(g),经5分钟后,测得D的浓度为0.5mol/L,CA:CB=3:5,C的平均速率为0.1mol/L.min。求
XC(g)+2D(g),经5分钟后,测得D的浓度为0.5mol/L,CA:CB=3:5,C的平均速率为0.1mol/L.min。求
(1)此时CA=
(2)反应开始前容器中的A、B的物质的量nA=nB=
(3)B的平均反应速率VB=
(4)X=
(5)此时容器内的压强与反应开始时压强的比为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
美国“海狼”潜艇上的核反应堆内使用了液态铝钠合金(单质钠和单质铝熔合而成)作载热介质,有关说法不正确的是( )
A.原子半径:Na>Al
B.若把铝钠合金投入一定量的水中只得到无色溶液,则n(Al)≤n(Na)
C.m g不同组成的铝钠合金投入足量盐酸中,若放出H2越多,则铝的质量分数越小
D.铝钠合金投入到足量氯化铜溶液中,肯定有氢氧化铜沉淀生成
查看答案和解析>>
科目:高中化学 来源: 题型:
现有五种可溶性物质A、B、C、D、E,它们所含阴、阳离子互不相同,分别含有五种阳离子Na+、Al3+、Mg2+、Ba2+、Fe3+和五种阴离子Cl-、OH-、NO 、CO
、CO 、X中的一种。
、X中的一种。
(1)某同学通过比较分析,认为无需检验就可判断其中必有的两种物质是________和________(填化学式)。
(2)为了确定X,现将(1)中的两种物质记为A和B,含X的物质记为C,当C与B溶液混合时,产生红褐色沉淀和无色无味气体;当C与A的溶液混合时产生棕黄色沉淀,向该沉淀中滴入稀硝酸沉淀部分溶解,最后留有白色沉淀不再溶解。则X为________。
A.SO B.SO
B.SO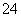
C.CH3COO- D.SiO
(3)将Cu投入到装有D溶液的试管中,Cu不溶解;再滴加稀H2SO4,Cu逐渐溶解,管口附近有红棕色气体出现。则物质D一定含有上述离子中的________(填相应的离子符号)。有关反应的离子方程式为___________________。
(4)利用上述已经确定的物质,可以检验出D、E中的阳离子,请简述实验操作步骤、现象及结论:__________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
乙二酸(H2C2O4)俗称草酸,是一种重要的化工原料。查阅资料,了解到以下有关信息:
①乙二酸易溶于水,加热至100℃开始升华,125℃时迅速升华,157℃时大量升华并开始分解。乙二酸受热分解生成水、二氧化碳和一种常见的还原性气体。
②乙二酸的钙盐——乙二酸钙为不溶于水的白色晶体。
(1)请写出乙二酸受热分解的化学方程式______________________。
(2)化学兴趣小组的同学用实验证明乙二酸晶体受热分解生成的气体成分。他们利用下图提供的装置,自选试剂,提出了下列实验方案:按A→B→C→C→C→D→E顺序从左至右连接装置,检验乙二酸晶体受热分解生成的气体成分。
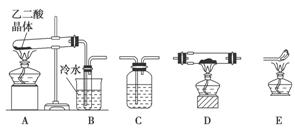
请你按整套装置从左至右的顺序填写下表中的空格:
| 仪器符号 | 仪器中所加物质 | 装置作用 |
| B | ||
| C | ||
| C | 氢氧化钠浓溶液 | |
| C | ||
| D | ||
| E |
(3)上述实验中能说明乙二酸受热分解生成了还原性气体的实验现象是________________________________________________________________。
(4)检验乙二酸具有较强的还原性,通常选用的试剂是_______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com