

| A、该物质的分子式为C16H16O3 |
| B、该物质分子内所碳原子有可能在同一平面内 |
| C、该物质可发生加成、取代、氧化等反应 |
| D、该物质可使酸性高锰酸钾溶液和溴水褪色,且原理相同 |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2014-2015学年山东省高三上学期12月月考化学试卷(解析版) 题型:选择题
W、X、Y、Z是短周期元素,其部分性质如下表
W | 单质是淡黄色固体 |
X | 在地壳中的含量居第二位 |
Y | 原子最外层电子数是电子总数的2/3 |
Z | 第三周期原子半径最小的金属 |
下列说法正确的是
A.Z的氧化物属于碱性氧化物
B.最高价氧化物对应水化物的酸性:Y>X
C.离子半径:Z>W
D.气态氢化物的热稳定性:X>W
查看答案和解析>>
科目:高中化学 来源: 题型:

| 金属离子 | 开始沉淀时的pH | 沉淀完全的pH |
| Al3+ | 3.4 | 4.7 |
| Cu2+ | 4.1 | 6.9 |
| Mg2+ | 9.4 | 12.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| 物质 | 沸点(℃) |
| 乙醇 | 78.5 |
| 乙酸 | 117.9 |
| 乙酸乙酯 | 77 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、ClO2是还原剂 |
| B、1 mol ClO2转移3mol电子 |
| C、CN-离子转化为NO2和CO2 |
| D、氧化剂与还原剂的物质的量之比是1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、R元素最高价氧化物所对应的水化物具有两性,但不会溶于稀氨水 |
| B、Y分别可与X和Z形成原子个数比为1:1的化合物,且形成的化合物晶体类型相同 |
| C、Y的氢化物分子间存在氢键,因此Y的氢化物的稳定性大于W的氢化物的稳定性 |
| D、原子半径从小到大:X<Y<Z<R<W |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、葡萄糖和果糖互为同分异构体,淀粉和纤维素也互为同分异构体 |
| B、淀粉、油脂和蛋白质都能发生水解反应 |
| C、多糖、蛋白质、脂肪和聚丙烯都属于高分子化合物 |
| D、汽油、柴油和植物油都是碳氢化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
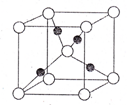 A、B、C、D、E为前四周期中原子序数依次增大的元素,相关的信息如下:
A、B、C、D、E为前四周期中原子序数依次增大的元素,相关的信息如下:| 元素 | 相关信息 |
| A | A元素原子核外只有三个能级,且每个能级上含有相等的电子数 |
| B | B在短周期元素中外围电子具有最多的未成对电子 |
| C | 短周期中,C的最高价氧化物对应水化物M碱性最强 |
| D | 基态原子第三能层上有7种运动状态不同的电子 |
| E | 一种核素的质量数为63,中子数为34 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com