
已知:①Co2O3在酸性溶液中易被还原成Co2+;②Co2O3、Cl2、FeCl3、I2的氧化性依次减弱。则下列在水溶液中的反应不可能发生的是( )
A.3Cl2+6FeI2===2FeCl3+4FeI3 B.Cl2+FeI2===FeCl2+I2
C.Co2O3+6HCl===2CoCl2+Cl2↑+3H2O D.2Fe3++2I-===2Fe2++I2
 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案科目:高中化学 来源: 题型:阅读理解
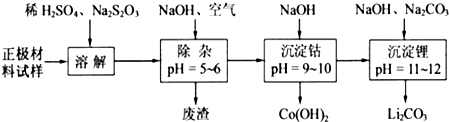
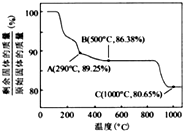
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Cl2+FeI2═FeCl2+I2 | B、3Cl2+6FeI2═2FeCl3+4FeI3 | C、2Fe3++2I-═2Fe2++I2 | D、Co2O3+6HCl═2CoCl2+Cl2↑+3H2O |
查看答案和解析>>
科目:高中化学 来源:2013届福建省三明市泰宁一中高三第二次月考化学试卷(带解析) 题型:单选题
已知:①Co2O3在酸性溶液中易被还原成Co2+;②Co2O3、Cl2、FeCl3、I2的氧化性依次减弱。则下列在水溶液中的反应不可能发生的是( )
| A.3Cl2+6FeI2===2FeCl3+4FeI3 | B.Cl2+FeI2===FeCl2+I2 |
| C.Co2O3+6HCl===2CoCl2+Cl2↑+3H2O | D.2Fe3++2I-===2Fe2++I2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com