
| A. | 二氧化硅能与氢氟酸反应,可用于制光导纤维 | |
| B. | 氧化铝熔点很高,可用于制耐火材料 | |
| C. | 新制氢氧化铜悬浊液具有碱性,可用于检验醛基 | |
| D. | 浓硫酸具有脱水性,可用于干燥氯气 |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③ | B. | ②③ | C. | ①② | D. | ①②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铁件表面镀铬时,铁件与外电源正极相连 | |
| B. | 反应CaO(s)+3C(s)═CaC2(s)+CO(g)在高温下能自发进行,则该反应的△H<0 | |
| C. | 用湿润的pH试纸测定0.1 mol•L-1的Na2CO3溶液的pH,其pH将偏大 | |
| D. | 已知(CH3CO)2O与水反应可生成乙酸(△H<0),向0.1 mol•L-1的乙酸溶液中加入少量(CH3CO)2O,溶液的pH和乙酸的电离程度均减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 二氧化氯被世界卫生组织(WHO)确认为第四代A1型消毒剂.
二氧化氯被世界卫生组织(WHO)确认为第四代A1型消毒剂.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | W10O21 | B. | W8O22 | C. | W10O27 | D. | W5O14 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 肉桂酸(
肉桂酸(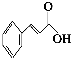 )在化妆行业及香料行业中属于明星物质,而且其需求量愈来愈大,如图是该物质的合成及其应用.根据图示回答下列问题:
)在化妆行业及香料行业中属于明星物质,而且其需求量愈来愈大,如图是该物质的合成及其应用.根据图示回答下列问题: ,其分子中所有的碳原子是否可能处于同一个平面?可能(填“可能”或“不可能”).
,其分子中所有的碳原子是否可能处于同一个平面?可能(填“可能”或“不可能”).  +
+ $→_{△}^{浓H_{2}SO_{4}}$
$→_{△}^{浓H_{2}SO_{4}}$ +H2O.
+H2O.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com