
【题目】某种激光染料,应用于可调谐染料激光器,它由C、H、O三种元素组成,分子球棍模型如图所示,下列有关叙述正确的是

(1)分子式为C10H9O3(2)不能溶于水
(3)1mol该物质最多能与4molH2加成(4)能使酸性KMnO4溶液褪色
(5) 1mol该物质最多能与含2molNaOH的溶液反应.
A. (1)(2)(3)(4) B. (2)(4)(5)
C. (2)(3)(4) D. (1)(2)(3)(4)(5)
【答案】C
【解析】由有机物的价键规则(碳原子形成4条键,氧原子形成2条键,氢原子形成1条键)可知该有机物的结构简式为 ;①由有机物的结构简式可知分子式为C10H8O3,故①错误;②为酯类化合物,不能溶于水,故②正确;③香豆素-4中含有苯环和碳碳双键,1mol该物质最多能与4molH2加成,故③正确;④香豆素-4中含有碳碳双键,酚羟基,都能被酸性KMnO4溶液氧化而使溶液褪色,故④正确;⑤1mol酚羟基消耗1mol氢氧化钠;1mol羧基消耗1mol氢氧化钠;若有酯的结构,则先让酯进行酸性水解,再看产物能否和氢氧化钠反应:若酸性水解的产物是羧酸和醇,1mol酯只能和1mol氢氧化钠反应;若酸性水解的产物是羧酸和酚类物质,则1mol酯能和2mol氢氧化钠反应,所以根据酚羟基、酯基推断香豆素-4最多能与含3 mol NaOH的溶液反应,故⑤错误;故选C。
;①由有机物的结构简式可知分子式为C10H8O3,故①错误;②为酯类化合物,不能溶于水,故②正确;③香豆素-4中含有苯环和碳碳双键,1mol该物质最多能与4molH2加成,故③正确;④香豆素-4中含有碳碳双键,酚羟基,都能被酸性KMnO4溶液氧化而使溶液褪色,故④正确;⑤1mol酚羟基消耗1mol氢氧化钠;1mol羧基消耗1mol氢氧化钠;若有酯的结构,则先让酯进行酸性水解,再看产物能否和氢氧化钠反应:若酸性水解的产物是羧酸和醇,1mol酯只能和1mol氢氧化钠反应;若酸性水解的产物是羧酸和酚类物质,则1mol酯能和2mol氢氧化钠反应,所以根据酚羟基、酯基推断香豆素-4最多能与含3 mol NaOH的溶液反应,故⑤错误;故选C。


科目:高中化学 来源: 题型:
【题目】25℃时,水溶液中c(H+)与c(OH-)的变化关系如图中曲线a c所示,下列判断错误的是

A.a c曲线上的任意一点都有c(H+)·c(OH-)=10-14
B.b d线段上任意一点对应的溶液都呈中性
C.d点对应溶液的温度高于25℃,pH<7
D.CH3COONa溶液不可能位于c点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,向一定浓度的Na2X溶液中滴入盐酸,溶液的pH与离子浓度变化关系如图所示。

已知:H2X是二元弱酸,Y表示![]() 或
或![]() ,pY=﹣lgY.下列叙述不正确的是( )
,pY=﹣lgY.下列叙述不正确的是( )
A. 曲线n表示pH与p![]() 的变化关系
的变化关系
B. Ka2(H2X)=1.0×10﹣10.3
C. NaHX溶液中c(H+)>c(OH﹣)
D. 当溶液呈中性时,c(Na+)=c(HX﹣)+2c(X2﹣)+c(Cl﹣)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某两种气态烃组成的混合物,取其2.24L(标准状况下)充分燃烧,得到0.16mol二氧化碳气体和3.6g液态水.据此判断下列分析中不正确的是
A. 此混合气体中可能含有乙烷
B. 此气体中一定含有甲烷
C. 此混合气体中一定不含有丙烷
D. 此气体若是乙烯与甲烷的混合气体,则甲烷与乙烯的体积比为2:3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机化合物A(C8H8O2)为一种无色液体。从A出发可发生如图的一系列反应。则下列说法正确的是

A.A的结构中含有碳碳双键
B.G的同分异构体中属于酯且能发生银镜反应的只有一种
C.上述各物质中能发生水解反应的有A、B、D、G
D.根据图示可推知D为苯酚
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用纤维素为主要原料制备乙酸乙酯的路线如下:

下列说法正确的是![]()
A.![]() 和
和![]() 都发生了氧化还原反应
都发生了氧化还原反应
B.M虽然分子结构中无醛基,但仍然可以发生银镜反应
C.步骤![]() ,1molM完全反应可以生成3mol乙醇
,1molM完全反应可以生成3mol乙醇
D.若用淀粉替代纤维素,一定条件下也能按照此路线制备乙酸乙酯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,aL密闭容器中加入1molN2和3molH2发生N2+3H2![]() 2NH3的反应,下列叙述中能说明该反应已达到化学平衡状态的是( )
2NH3的反应,下列叙述中能说明该反应已达到化学平衡状态的是( )
A.v(N2正)=2v(NH3正)
B.3v(H2正)=v(N2逆)
C.单位时间内有0.3molH2消耗的同时,生成0.2molNH3
D.单位时间内有1个N≡N键断裂的同时,有6个N—H键断裂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关电解质溶液的说法正确的是( )
A.向AgCl、AgBr的饱和溶液中加入少量AgNO3,溶液中![]() 不变
不变
B.将CH3COONa溶液从20℃升温至30℃,溶液中![]() 增大
增大
C.向盐酸中加入氨水至中性,溶液中![]() >1
>1
D.向0.1molL-1CH3COOH 溶液中加入少量水,溶液中 减小
减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CCUS是一种二氧化碳的捕获、利用与封存的技术,这种技术可将CO2资源化,产生经济效益。请回答下列问题:
(1)利用废气中的CO2为原料可制取甲醇。一定条件下,在恒容密闭容器中发生反应CO2(g)+3H2(g)CH3OH(g)+H2O(g)。
①已知:H2(g)、CH3OH(1)的燃烧热(△H)分别为-285.8kJmol-1和-726.5kJmol-1;CH3OH(1)=CH3OH (g) △H=+35.2kJmol-1;H2O(1)=H2O(g) △H=+44kJmol-1。
则CO2(g)+3H2(g)CH3OH(g)+H2O(g) △H=___kJmol-1。有利于提高H2平衡转化率的条件是___(填选项字母)。
A.高温低压 B.低温高压 C.高温高压 D.低温低压
②某温度下,向体积为2L的容器中充入6molH2、4molCO2,发生反应CO2(g)+3H2(g)CH3OH(g)+H2O(g),达到平衡时H2的转化率为50%,其平衡常数为___ (保留两位小数)。
③起始条件(T1℃、2L密闭容器)如表所示:
CO2/mol | H2/mol | CH3OH/mol | H2O/mol | |
I(恒温恒容) | 2 | 6 | 0 | 0 |
II(绝热恒容) | 0 | 0 | 2 | 2 |
达到平衡时,该反应的平衡常数:K(I)___K(Ⅱ)(填“>”“<”或“=”,下同);平衡时CH3OH的浓度:c(I)___c(Ⅱ)。
(2)CO2可用来合成低碳烯烃:2CO2(g)+6H2(g)CH2=CH2(g)+4H2O(g) △H=-127.8 kJmol-1。0.1MPa下,按n(CO2)︰n(H2)=1︰3的投料比充入体积固定的密闭容器中,发生上述反应,不同温度(T)下平衡时的四种气态物质的体积分数(φ)如图所示:
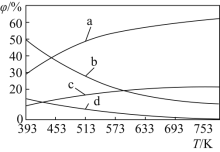
①曲线b、c表示的物质分别为___、___(填化学式)。
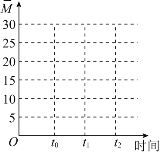
②保持温度不变,在体积为VL的恒容容器中以n(CO2)︰n(H2)=2︰3的投料比加入反应物,t0时达到化学平衡。t1时将容器体积瞬间扩大至2VL并保持不变,t2时重新达到平衡。请在图中画出容器内混合气体的平均相对分子质量M随时间的变化趋势图象___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com