
| ×å ÖÜĘŚ | I A | ¢ņA | ¢óA | ¢ōA | ¢õA | ¢öA | ¢÷A | O |
| 1 | A | |||||||
| 2 | D | E | G | I | ||||
| 3 | B | C | F | H |
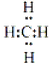 £®
£®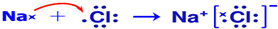
·ÖĪö ÓÉŌŖĖŲŌŚÖÜĘŚ±ķµÄĪ»ÖĆæÉÖŖ£¬AĪŖH£¬BĪŖNa£¬CĪŖAl£¬DĪŖC£¬EĪŖN£¬FĪŖP£¬GĪŖF£¬HĪŖCl£¬IĪŖNe£¬
£Ø1£©ÉĻŹöŌŖĖŲ£¬FĪŽÕż¼Ū£¬FµÄ·Ē½šŹōŠŌ×īĒ棬NaµÄ½šŹōŠŌ×īĒ棻
£Ø2£©×īøß¼ŪŃõ»ÆĪļµÄĖ®»ÆĪļÖŠ£¬NaOHµÄ¼īŠŌ×īĒ棬øßĀČĖįµÄĖįŠŌ×īĒ棬ĒāŃõ»ÆĀĮ¾ßÓŠĮ½ŠŌ£»
£Ø3£©·Ē½šŹōŠŌŌ½Ē棬¶ŌÓ¦Ēā»ÆĪļŌ½ĪČ¶Ø£»
£Ø4£©AŗĶD×é³É»ÆŗĻĪļĪŖ¼×Ķ飻
£Ø5£©BŗĶH×é³É»ÆŗĻĪļĪŖNaCl£¬ĪŖĄė×Ó»ÆŗĻĪļ£»
£Ø6£©BµÄ×īøß¼ŪŃõ»ÆĪļµÄĖ®»ÆĪļĪŖNaOH£¬CµÄ×īøß¼ŪŃõ»ÆĪļµÄĖ®»ÆĪļĪŖĒāŃõ»ÆĀĮ£¬¶žÕß·“Ӧɜ³ÉĘ«ĀĮĖįÄĘŗĶĖ®£®
½ā“š ½ā£ŗÓÉŌŖĖŲŌŚÖÜĘŚ±ķµÄĪ»ÖĆæÉÖŖ£¬AĪŖH£¬BĪŖNa£¬CĪŖAl£¬DĪŖC£¬EĪŖN£¬FĪŖP£¬GĪŖF£¬HĪŖCl£¬IĪŖNe£¬
£Ø1£©ÉĻŹöŌŖĖŲ£¬Ö»ÓŠøŗ¼Ū¶ųĪŽÕż¼ŪµÄŹĒF£¬Ńõ»ÆŠŌ×īĒæµÄµ„ÖŹŹĒF2£¬»¹ŌŠŌ×īĒæµÄµ„ÖŹŹĒ£¬
¹Ź“š°øĪŖ£ŗF£» F2£»Na£»
£Ø2£©×īøß¼ŪŃõ»ÆĪļµÄĖ®»ÆĪļ¼īŠŌ×īĒæµÄŹĒNaOH£¬ĖįŠŌ×īĒæµÄŹĒH2SO4£¬³ŹĮ½ŠŌµÄŹĒAl£ØOH£©3£¬
¹Ź“š°øĪŖ£ŗNaOH£»H2SO4£»Al£ØOH£©3£»
£Ø3£©·Ē½šŹōŠŌŌ½Ē棬¶ŌÓ¦Ēā»ÆĪļŌ½ĪČ¶Ø£¬ŌņA·Ö±šÓėD”¢E”¢F”¢G”¢HŠĪ³ÉµÄ»ÆŗĻĪļÖŠ£¬×īĪČ¶ØµÄHCl£¬¹Ź“š°øĪŖ£ŗHCl£»
£Ø4£©AŗĶD×é³É»ÆŗĻĪļĪŖ¼×Ķ飬µē×ÓŹ½ĪŖ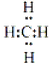 £¬¹Ź“š°øĪŖ£ŗ
£¬¹Ź“š°øĪŖ£ŗ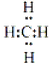 £»
£»
£Ø5£©BŗĶH×é³É»ÆŗĻĪļĪŖNaCl£¬ĪŖĄė×Ó»ÆŗĻĪļ£¬ÓƵē×ÓŹ½±ķŹ¾BŗĶH×é³É»ÆŗĻĪļµÄŠĪ³É¹ż³ĢĪŖ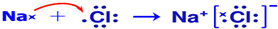 £¬
£¬
¹Ź“š°øĪŖ£ŗ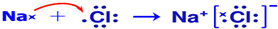 £»
£»
£Ø6£©BµÄ×īøß¼ŪŃõ»ÆĪļµÄĖ®»ÆĪļĪŖNaOH£¬CµÄ×īøß¼ŪŃõ»ÆĪļµÄĖ®»ÆĪļĪŖĒāŃõ»ÆĀĮ£¬¶žÕß·“Ӧɜ³ÉĘ«ĀĮĖįÄĘŗĶĖ®£¬Ąė×Ó·“Ó¦ĪŖOH-+Al£ØOH£©3ØTAlO2-+2H2O£¬
¹Ź“š°øĪŖ£ŗOH-+Al£ØOH£©3ØTAlO2-+2H2O£®
µćĘĄ ±¾Ģāæ¼²éĪ»ÖĆ”¢½į¹¹ÓėŠŌÖŹ£¬ĪŖøßĘµæ¼µć£¬°ŃĪÕŌŖĖŲµÄĪ»ÖĆ”¢ŠŌÖŹ”¢ŌŖĖŲ»ÆŗĻĪļĪŖ½ā“šµÄ¹Ų¼ü£¬²ąÖŲ·ÖĪöÓėÓ¦ÓĆÄÜĮ¦µÄ漲飬עŅā¹ęĀÉŠŌÖŖŹ¶¼°ŌŖĖŲ»ÆŗĻĪļÖŖŹ¶µÄÓ¦ÓĆ£¬ĢāÄæÄŃ¶Č²»“ó£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÓĆĖ«ŃõĖ®“śĢęøßĆĢĖį¼ŲÖĘŃõĘų | |
| B£® | ÓƶąĮæµÄĀČĘų½ųŠŠŠŌÖŹŹµŃé | |
| C£® | ÓĆäåĖ®“śĢęµāĖ®½ųŠŠŻĶČ”ŹµŃé | |
| D£® | ÓĆĶ·Ū“śĢęĶĖæ½ųŠŠĶŗĶÅØĻõĖįµÄ·“Ó¦ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
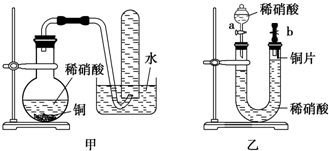
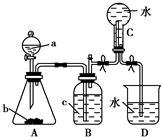 ČēĶ¼×°ÖĆŹĒijÖÖĘųĢåXµÄÖĘČ”×°ÖĆŗĶŹÕ¼Æ×°ÖĆ£Ø±ŲŅŖŹ±æɼÓČČ£©£®ĖłÓƵďŌ¼Į“ÓĻĀĮŠŹŌ¼Į֊єȔ2”«3ÖÖ£ŗĮņ»ÆŃĒĢś”¢¶žŃõ»ÆĆĢ”¢ĶŠ¼”¢ĀČ»Æļ§”¢Ļ”ĻõĖį”¢ÅØŃĪĖį”¢ÕōĮóĖ®£®Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
ČēĶ¼×°ÖĆŹĒijÖÖĘųĢåXµÄÖĘČ”×°ÖĆŗĶŹÕ¼Æ×°ÖĆ£Ø±ŲŅŖŹ±æɼÓČČ£©£®ĖłÓƵďŌ¼Į“ÓĻĀĮŠŹŌ¼Į֊єȔ2”«3ÖÖ£ŗĮņ»ÆŃĒĢś”¢¶žŃõ»ÆĆĢ”¢ĶŠ¼”¢ĀČ»Æļ§”¢Ļ”ĻõĖį”¢ÅØŃĪĖį”¢ÕōĮóĖ®£®Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĶʶĻĢā
 X”¢Y”¢Z”¢W”¢RĪåÖÖŌŖĖŲĪ»ÓŚŌŖĖŲÖÜĘŚ±ķĒ°ĖÄÖÜĘŚ£¬ĖüĆĒµÄŌ×ÓŠņŹżŅĄ“ĪŌö“ó
X”¢Y”¢Z”¢W”¢RĪåÖÖŌŖĖŲĪ»ÓŚŌŖĖŲÖÜĘŚ±ķĒ°ĖÄÖÜĘŚ£¬ĖüĆĒµÄŌ×ÓŠņŹżŅĄ“ĪŌö“ó| ŌŖĖŲ | Ļą¹ŲŠÅĻ¢ |
| X | Ō×ÓŗĖĶāµÄ¼Ūµē×ÓÅŲ¼Ź½ĪŖnsnnp2n |
| Y | ŌŖĖŲÖÜĘŚ±ķÖŠµēøŗŠŌ×īĒæµÄŌŖĖŲ |
| Z | ZÓėWĪ»ÓŚĶ¬ÖÜĘŚ£¬ĒŅ×īĶā²ćÓŠĮ½øöĪ“³É¶Ōµē×Ó |
| w | µ„ÖŹĪŖµ»ĘÉ«¹ĢĢ壬ÄÜŌŚ»šÉ½æŚ·¢ĻÖ |
| R | Ō×ӵĻłĢ¬Ī“³É¶Ōµē×ÓÖĀŹĒĶ¬ÖÜĘŚ×ī¶ąµÄŌŖĖŲ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
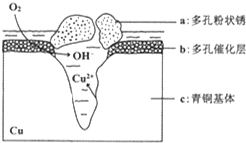 ĶŹĒŅ»ÖÖÖŲŅŖµÄÓŠÉ«½šŹō£¬½üÄźĄ“ÓĆĶ¾Ō½Ą“Ō½¹ć·ŗ£®Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
ĶŹĒŅ»ÖÖÖŲŅŖµÄÓŠÉ«½šŹō£¬½üÄźĄ“ÓĆĶ¾Ō½Ą“Ō½¹ć·ŗ£®Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | CuÓėĻõĖį | B£® | ³ĪĒåµÄŹÆ»ŅĖ®ÓėCO2 | ||
| C£® | NaÓėO2 | D£® | AlCl3Óė°±Ė® |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| ×éŗĻŠņŗÅ | ¢ń | ¢ņ | ¢ó | ¢ō | ¢õ | ¢ö |
| ×éŗĻŹż¾Ż |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
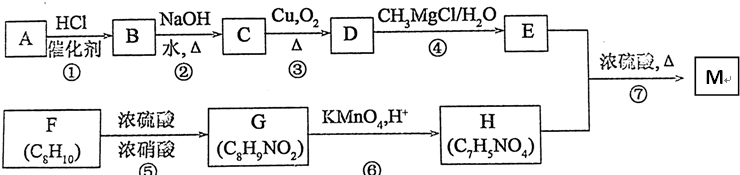
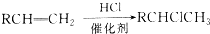
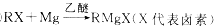
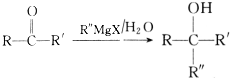
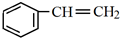 £¬CÖŠ¹ŁÄÜĶŵÄĆū³ĘĪŖōĒ»ł£®
£¬CÖŠ¹ŁÄÜĶŵÄĆū³ĘĪŖōĒ»ł£®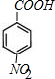 +
+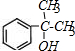 $?_{”÷}^{ÅØĮņĖį}$
$?_{”÷}^{ÅØĮņĖį}$ +H2O£®
+H2O£® ”¢
”¢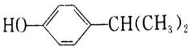 £®
£®²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com