
已知25 ℃、101 kPa下,石墨、金刚石燃烧的化学方程式分别为:C(石墨) + O2(g) = CO2(g),1 moL C(石墨) 完全燃烧放热393.51 kJ;C(金刚石) + O2(g) = CO2(g),1 moL C(金刚石) 完全燃烧 放热 395.41 kJ。据此推理所得到的下列结论中,正确的是
A.金刚石比石墨稳定 B.石墨转化为金刚石是物理变化
C.石墨的能量比金刚石的能量高 D.由石墨制备金刚石一定是吸热反应
科目:高中化学 来源: 题型:
下列有关热化学方程式的评价合理的是( )
|
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 10-9 |
| a-0.01 |
| 10-9 |
| a-0.01 |
查看答案和解析>>
科目:高中化学 来源:2014届四川省绵阳市高二12月月考化学试卷(解析版) 题型:实验题
已知25℃、101 kPa下,稀的强酸与强碱溶液反应的中和热为57.3 kJ/mol。
(1)写出表示稀硫酸与稀烧碱溶液发生反应的中和热的热化学方程式: 。
(2)学生甲用稀硫酸与稀烧碱溶液测定中和热装置如图。
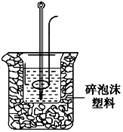
①实验时所需的玻璃仪器除烧杯、量筒外还需: 。
②该装置中有一处错误是: ,如果用该错误装置测定,结果会 (填“偏高”“偏低”“无影响”)
③如果,该生用50 mL 0.25 mol/L的稀硫酸与50 mL 0.55 mol/L的稀烧碱溶液,他用试剂的用量的理由是: 。在该实验中需要测定某种数据,完成一次实验,需要测定该数据的次数为 次。
④若反应前溶液以及中和后的混合液的密度均设为 1 g/cm3,混合前酸与碱的温度均为 t1,混合后溶液的温度为 t2,比热容为 4.18 J/(g·℃)。那么该生测定中和热:ΔH= 。
(3)学生乙用2 mol/L的硫酸来测定与锌粒和锌粉反应的快慢,设计如图(Ⅰ)装置:
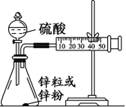
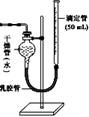
图Ⅰ 图Ⅱ
①该生两次实验测定时间均设定为10 min,那么他还要测定的另一个数据是:
。
②如果将图Ⅰ装置中的气体收集装置改为图Ⅱ,实验完毕待冷却后,该生准备读取滴定管上液面所处的刻度数,发现滴定管中液面高于干燥管中液面,应先采取的操作是: 。
③该实验结果中,你估计与酸反应较快的是 。
查看答案和解析>>
科目:高中化学 来源:2014届福建省高二第一次月考化学试卷(解析版) 题型:选择题
已知25℃、101 kPa下,石墨、金刚石燃烧的热化学方程式分别为C(石墨) + O2(g)
==== CO2(g) 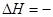 393.51
kJ/mol①;C(金刚石) + O2(g) ==== CO2(g)
393.51
kJ/mol①;C(金刚石) + O2(g) ==== CO2(g) 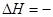 395.41
kJ/mol②,据此判断,下列说法正确的是( )
395.41
kJ/mol②,据此判断,下列说法正确的是( )
A. 由石墨制备金刚石是吸热反应;等质量时,石墨的能量比金刚石的低
B. 由石墨制备金刚石是吸热反应;等质量时,石墨的能量比金刚石的高
C. 由石墨制备金刚石是放热反应;等质量时,石墨的能量比金刚石的低
D. 由石墨制备金刚石是放热反应;等质量时,石墨的能量比金刚石的高
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com