
【题目】在无色透明的溶液中,可以大量共存的离子组是( )
A.Cl-、Na+、AlO2-、MnO4-B.Na+、Cl-、SO42-、K+
C.Al3+、SO42—、Cu2+、NO3-D.K+、Ag+、NO3—、I-
科目:高中化学 来源: 题型:
【题目】根据下列实验操作和现象能推出相应结论的是
选项 | 实验操作和现象 | 结论 |
A | 向NaAlO2溶液中滴加NaHCO3 溶液,产生白色沉淀 | AlO2-与HCO3-发生了相互促进的水解反应 |
B | 向溶有SO2的BaCl2溶液中通入气体X,出现白色沉淀 | X不一定具有氧化性 |
C | 灼热的木炭加入浓硝酸中,放出红棕色气体 | 一定是木炭与浓硝酸反应生成了NO2 |
D | 将乙醇与浓硫酸共热,制得的气体直接通入酸性KMnO4溶液中,酸性KMnO4溶液褪色 | 说明制得的气体中含有乙烯 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇是一种可再生能源,又是一种重要的化工原料.具有广阔的开发和应用前景。工业上可用如下方法合成甲醇:CO(g)+2H2(g)![]() CH3OH(g).
CH3OH(g).
(1) 已知:①2CH3OH(l)+3O2(g)![]() 2CO2(g)+4H2O(g)△H=-1275.6kJ·mol-1;
2CO2(g)+4H2O(g)△H=-1275.6kJ·mol-1;
②2CO(g)+O2(g)![]() 2CO2(g)△H=-566.0kJ·mol-1;
2CO2(g)△H=-566.0kJ·mol-1;
③H2O(l)=H2O(g)△H=+44.0kJ·mol-1.
则甲醇液体不完全燃烧生成CO和液态水的热化学方程式为__________。
(2) 在一定温度下,向2L密闭容器中充人1mol CO和2mol H2,发生反应CO(g)+2H2(g)![]() CH3OH(g),5min反应达到平衡,此时CO的转化率为80%。
CH3OH(g),5min反应达到平衡,此时CO的转化率为80%。
①前5min内甲醇的平均反应速率为__________;已知该反应在低温下能自发进行,则反应的△H_______0(填“>”“<”或“=”)。
②在该温度下反应的平衡常数K=__________。
③某时刻向该平衡体系中加人CO、H2、CH3OH各0.2mol后,则v正__________v逆(填“>”“=”或“<”)。
④当反应达到平衡时,__________(填字母)。
a.混合气体的压强不再发生变化 b.反应物不再转化为生成物
c.v正(CO)=2v逆(H2) d.v(H2)=2v(CH3OH)
e.三种物质的浓度比恰好等于化学方程式中各物质的化学计量数之比
(3) "甲醇---过氧化氢燃料电池"的结构主要包括燃料腔、 氧化剂腔和质子交换膜三部分.放电过程中其中一个腔中生成了CO2。
①放电过程中生成H+的反应,发生在__________腔中,该腔中的电极反应式为__________.
②该电池工作过程中,当消耗甲醇4.8g时.电路中通过的电量为__________(法拉第常数F=9.65×104C·mol-1)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在细胞内含量极少,但对维持生命活动必不可少的元素有
A. Fe Mn Zn Mg B. Zn Cu Mg Ca
C. Zn Cu B Mn D. Mg Mn Cu Mo
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图中甲为甲烷和O2构成的燃料电池示意图,电解质为KOH溶液,乙为电解饱和MgCl2溶液的装置,其中乙装置中X为阳离子交换膜。用该装置进行实验,反应开始后观察到Fe电极附近出现白色沉淀。下列说法正确的是
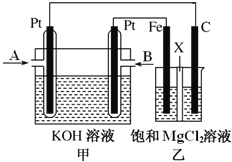
A. 甲中A处通入CH4,电极反应式为CH4+10OH--8e-=== ![]() +7H2O
+7H2O
B. 乙中电解MgCl2溶液的总反应为2Cl-+2H2O![]() Cl2↑+H2↑+2OH-
Cl2↑+H2↑+2OH-
C. 理论上甲中每消耗22.4 L CH4(标准状况下),乙中产生4 mol Cl2
D. 甲、乙中电解质溶液的pH都增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定量的甲烷燃烧后得到的产物为CO、CO 2 和水蒸气,此混合气体质量为 49.6 g ,当其缓慢经过无水氯化钙(足量)时,氯化钙增重 25.2 g ,则原混合气体中CO 的质量为( )
A. 26.4 g B. 19.7 g C. 13.2 g D. 11.2 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】因发生氧化还原反应在水溶液中不能大量共存的离子组是( )
A.Ca2+、Br - 、Fe3+ 、CO32-B.Fe2+、Cl-、NO3- 、H+
C.Fe3+ 、Ca2+、 H+ 、NO3-D.NO3-、OH- 、Cl-、Ba2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按系统命名法填写下列有机物的名称及有关内容。
(1).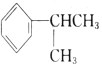 的名称是________.
的名称是________.
(2). 的分子式为__,1mol该烃完全燃烧消耗O2__mol.
的分子式为__,1mol该烃完全燃烧消耗O2__mol.
(3).分子式为C4H8的所有烯烃的结构简式及名称:________.
(4).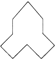 的名称是________.
的名称是________.
(5)写出下列有机物的结构简式.
①环戊烯:________________
②3-甲基-1-丁炔:___________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲烷作为一种新能源在化学领域应用广泛,请回答下列问题。
(1)高炉冶铁过程中,甲烷在催化反应室中产生水煤气(CO和H2)还原氧化铁,有关反应为:CH4(g)+CO2(g)===2CO(g)+2H2(g) ΔH=260 kJ·mol-1
已知:2CO(g)+O2(g)===2CO2(g)
ΔH=-566 kJ·mol-1。
则CH4与O2反应生成CO和H2的热化学方程式为_________________________________。
(2)如下图所示,装置Ⅰ为甲烷燃料电池(电解质溶液为KOH溶液),通过装置Ⅱ实现铁棒上镀铜。
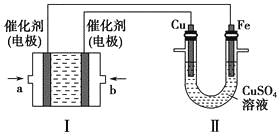
①a处应通入________(填“CH4”或“O2”),b处电极上发生的电极反应式是__________________________________。
②电镀结束后,装置Ⅰ中溶液的pH________(填写“变大”“变小”或“不变”,下同),装置Ⅱ中Cu2+的物质的量浓度________。
③电镀结束后,装置Ⅰ溶液中的阴离子除了OH-以外还含有________(忽略水解)。
④在此过程中若完全反应,装置Ⅱ中阴极质量变化12.8 g,则装置Ⅰ中理论上消耗甲烷________L(标准状况下)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com