
【题目】D是一种催眠药,F是一种香料,它们的合成路线如下:
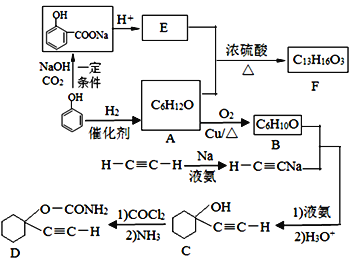
(1)A的化学名称是___,C中含氧官能团的名称为_____。
(2)F的结构简式为____,A和E生成F的反应类型为____。
(3)A生成B的化学方程式为________。
(4)写出由C合成D的第二个反应的化学方程式:________。
(5)同时满足下列条件的E的同分异构体有___种(不含立体异构)。
①遇FeCl3溶液发生显色反应;
②能发生银镜反应
(6)以乙炔和甲醛为起始原料,选用必要的无机试剂合成1,3-丁二烯,写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)_____。
(7)
乙炔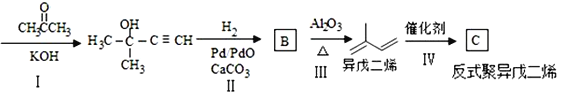
①写出C的结构简式:___
②写出从I至IV的反应类型分别为:_______
【答案】环己醇 羟基 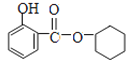 酯化(取代)反应 2
酯化(取代)反应 2![]() +O2
+O2![]() 2
2![]() +2H2O
+2H2O 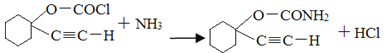 9
9 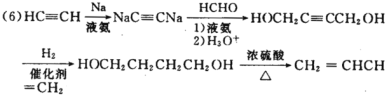
 加成、加成、消去、加聚
加成、加成、消去、加聚
【解析】
(1)苯酚与氢气发生加成反应生成A,A的化学名称为环己醇;根据C的结构简式可知C中含氧官能团的名称为羟基;
(2)E是邻羟基苯甲酸,与A发生酯化反应生成F,则F的结构简式为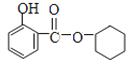 ;其反应类型为酯化(取代)反应;
;其反应类型为酯化(取代)反应;
(3)A发生催化氧化生成B,则A生成B的化学方程式为:2![]() +O2
+O2![]() 2
2![]() +2H2O;
+2H2O;
(4)C合成D的第二个反应是氯原子被氨基取代,反应的化学方程式为: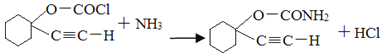 ;
;
(5)①遇FeCl3溶液发生显色反应,说明含有酚羟基;②能发生银镜反应,说明含有醛基;如果苯环上含有2个取代基,应该是-OH和-OOCH,有邻间对三种,若含有3个取代基,应该是2个酚羟基、1个醛基,有6种,共9种;
(6)根据题干信息结合逆推法可知乙炔和甲醛为起始原料合成1,3-丁二烯的合成路线为: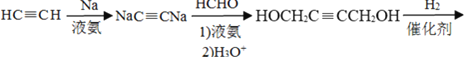
 ;
;
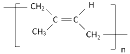
(7)①异戊二烯通过1,4加成进行缩合生成反式聚异戊二烯,根据名称可书写出其结构简式为: ;
;
②根据反应条件以及反应物与生成物的结构可知,从I至IV的反应类型分别为:加成、加成、消去、加聚。


科目:高中化学 来源: 题型:
【题目】实验室中,采用废易拉罐(主要成分为Al,含有少量的Fe、Mg杂质)制备明矾[KAl(SO4)2·12H2O]的过程如图所示。下列说法正确的是
![]()
A. 试剂①可选用盐酸或NaOH溶液
B. 过滤操作中使用的玻璃仪器只有漏斗、烧杯
C. 滤液A到沉淀B的反应中无CO2生成
D. 最后一步操作是蒸发结晶
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能源问题是当今世界的重要课题,研究反应中的能量变化尤为重要。下列变化过程中的能量变化符合图示过程的是( )

A.焦炭制水煤气B.酸碱中和反应
C.铝与氧化铁的高温反应D.浓硫酸的稀释
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究电化学腐蚀及防护的装置如右图所示。下列有关说法错误的是( )

A. d为石墨,铁片腐蚀加快
B. d为石墨,石墨上电极反应为:O2 + 2H2O + 4e == 4OH–
C. d为锌块,铁片不易被腐蚀
D. d为锌块,铁片上电极反应为:2H+ + 2e == H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“84消毒液”是一种以NaClO为主的高效消毒剂,被广泛用于宾馆、旅游、医院、食品加工行业、家庭等的卫生消毒,某“84消毒液”瓶体部分标签如图1所示,该“84消毒液”通常稀释100倍(体积之比)后使用,请回答下列问题:
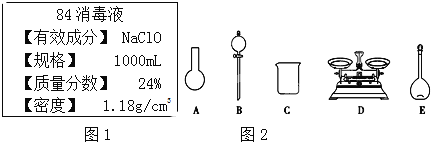
(1)此“84消毒液”的物质的量浓度约为______mol/L(计算结果保留一位小数)。
(2)某同学量取此“84消毒液”,按说明要求稀释后用于消毒,则稀释后的溶液中c(Na+)=___mol/L。
(3)该同学参阅读该“84消毒液”的配方,欲用NaClO固体配制480 mL含NaClO质量分数为24%的消毒液。
①如图2所示的仪器中配制溶液需要使用的是______(填仪器序号),还缺少的玻璃仪器是_______。
②下列操作中,容量瓶不具备的功能是_____(填仪器序号)。
a.配制一定体积准确浓度的标准溶液 b.贮存溶液
c.测量容量瓶规格以下的任意体积的溶液 d.准确稀释某一浓度的溶液
e.用来加热溶解固体溶质
③请计算该同学配制此溶液需称取称量NaClO固体的质量为______g。
(4)若实验遇下列情况,导致所配溶液的物质的量浓度偏高是______。(填序号)。
A.定容时俯视刻度线 B.转移前,容量瓶内有蒸馏水
C.未冷至室温就转移定容 D.定容时水多用胶头滴管吸出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室可通过蒸馏石油得到多种沸点范围不同的馏分,装置如图所示。下列说法不正确的是
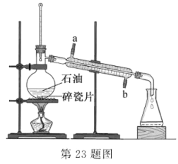
A.沸点较低的汽油比沸点较高的柴油先馏出
B.蒸馏烧瓶中放人沸石可防止蒸馏时发生暴沸
C.冷凝管中的冷凝水应该从 a 口进 b 口出
D.温度计水银球的上限和蒸馏烧瓶支管口下沿相平
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关热化学方程式的叙述正确的是
A. 反应物的总能量低于生成物的总能量时,该反应必须加热才能发生
B. 2NaOH(aq)+H2SO4(aq)=Na2SO4(aq)+2H2O(l) △H=-akJ·mol-1,则中和热为a/2kJ·mol-1
C. 2H2(g)+O2(g)=2H2O(l);△H1=-akJ·mol-1,则氢气燃烧热为akJ·mol-1
D. N2(g)+3H2(g)=2NH3(g);△H=-akJ·mol-1,则将14gN2(g)和足量H2置于一密闭容器中,充分反应后放出0.5akJ的热量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知下列热化学方程式:①H2(g)+![]() O2(g)→H2O+285.8kJ ②C(s)+O2(g)→CO2(g)+393.5kJ ③C(s)+H2O(g)→CO(g)+H2(g)-131.5kJ
O2(g)→H2O+285.8kJ ②C(s)+O2(g)→CO2(g)+393.5kJ ③C(s)+H2O(g)→CO(g)+H2(g)-131.5kJ
上述反应中表明反应物的总能量高于生成物的总能量的是___(选填编号)。热化学方程式③所表示的意义是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由SO2和O2制备SO3(熔点16.8 ℃,沸点44.8 ℃)的模拟装置如图所示(加热和夹持装置省略):
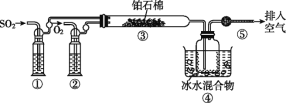
下列说法正确的是( )
A.装置①中的试剂为饱和NaHSO3溶液
B.实验室可用铜与浓硫酸在常温条件下制取SO2
C.装置③反应管中的铂石棉用作反应的催化剂
D.从装置⑤逸出的气体有过量的SO2和O2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com