
| A. | H2O2分子的空间构型为直线形 | |
| B. | CO2分子为含有极性键的极性分子 | |
| C. | BF3分子中的B原子不满足8电子稳定结构 | |
| D. | CH3COOH分子中C原子均为sp2杂化 |
分析 A.H2O2分子中氧原子形成2个σ键,含有2对孤电子对,O原子及其连接的H原子、O原子形成V形结构;
B.CO2分子为直线型对称结构;
C.原子最外层电子数+化合价绝对值=8,该原子满足8电子结构;
D.CH3COOH分子中甲基中碳原子形成4个σ键,没有孤对电子,采取sp3杂化.
解答 解:A.H2O2分子中氧原子形成2个σ键,含有2对孤电子对,O原子及其连接的H原子、O原子形成V形结构,H2O2分子的空间构型不是直线形,为展开书页形结构,故A错误;
B.CO2分子为直线型对称结构,分子中正负电荷重心重合,属于非极性分子,故B错误;
C.BF3分子中的B原子的最外层电子数+B的化合价绝对值=6,不满足8电子结构,故C正确;
D.CH3COOH分子中羧基中C原子形成3个σ键,没有孤对电子,采取sp2杂化,但甲基中碳原子形成4个σ键,没有孤对电子,采取sp3杂化,故D错误,
故选C.
点评 本题考查较为综合,涉及分子结构与性质,涉及空间构型判断、分子极性、8电子结构、杂化方式判断,为高频考点,侧重考查学生的分析能力,注意掌握空间构型的判断,难度不大.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯能够使溴水褪色,是因为乙烯和溴水反应生成了2-溴乙烷 | |
| B. | 将红热的铜丝插入到1-丙醇中,可以制得丙酮 | |
| C. | 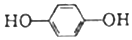 和苯酚互为同系物 和苯酚互为同系物 | |
| D. | 分子式为C10H12具有两个邻位链烃取代基的芳香烃有4种(不考虑立体异构) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 图1所示的装置可用于干燥、收集并吸收多余的氨气 | |
| B. | 用图2的装置可以验证生铁片在该雨水中是否会发生吸氧腐蚀 | |
| C. | 图3所示装置用于Cu和浓H2SO4反应制取少量的SO2气体 | |
| D. | 图4所示装置用于除去碳酸氢钠固体中的少量碳酸钠 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 利用丁达尔效应鉴别FeCl3溶液和Fe(OH)3胶体 | |
| B. | 只能利用焰色反应可鉴别KCl溶液和Na2SO4溶液 | |
| C. | 用水润湿pH试纸测量某溶液的PH | |
| D. | 实验室用NaOH溶液除去Cl2中的少量HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
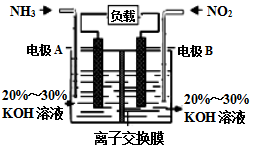 2017年春节,京津冀及周边区域遭遇“跨年”雾霾,二氧化硫、氮氧化物以及可吸入颗粒物这三项是雾霾主要组成,消除氮氧化物污染是研究方向之一.
2017年春节,京津冀及周边区域遭遇“跨年”雾霾,二氧化硫、氮氧化物以及可吸入颗粒物这三项是雾霾主要组成,消除氮氧化物污染是研究方向之一.物质 浓度(mol/L) 时间(min) | NO | N2 | CO2 |
| 0 | 0.100 | 0 | 0 |
| 10 | 0.058 | 0.021 | 0.021 |
| 20 | 0.040 | 0.030 | 0.030 |
| 30 | 0.040 | 0.030 | 0.030 |
| 40 | 0.032 | 0.034 | 0.017 |
| 50 | 0.032 | 0.034 | 0.017 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 等质量的铝分别与足量Fe2O3或Fe3O4发生铝热反应时,转移电子的数目相等 | |
| B. | 质量分数分别为40%和60%的硫酸溶液等体积混合,所得溶液的质量分数为50% | |
| C. | 金属钠着火时,立即用泡沫灭火器灭火 | |
| D. | 洗涤做焰色反应的铂丝,可选用稀盐酸或稀硫酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯和苯都能使溴水褪色,褪色的原因相同 | |
| B. | 分子式为C2H6O2且能与NaOH溶液反应的有机物一定是乙酸 | |
| C. | 油脂和纤维素都是能发生水解反应的高分子化合物 | |
| D. | 甲烷、苯、乙醇、乙酸和酯类都可以发生取代反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验 | 现象 | 结论 | |
| A | 含HCl、BaCl2的FeCl3溶液 | 产生白色沉淀 | SO2有还原性 |
| B | H2S溶液 | 产生黄色沉淀 | SO2有氧化性 |
| C | 酸性KMnO4溶液 | 紫色溶液褪色 | SO2有漂白性 |
| D | Na2SiO3溶液 | 产生胶状沉淀 | 酸性:H2SO3>H2SiO3 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com