
(10分)已知A(g)+B(g) 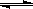 C(g)+D(g)反应的平衡常数和温度的关系如下:
C(g)+D(g)反应的平衡常数和温度的关系如下:
|
|温度/ ℃ |
700 |
900 |
830 |
1000 |
1200 |
|
平衡常数 |
1.7 |
1.1 |
1.0 |
0.6 |
0.4 |
回答下列问题:
(1).该反应的平衡常数表达式K= 。
(2).830℃时,向一个5 L的密闭容器中充入0.20mol的A和0.80mol的B,如反应初始6s内A的平均反应速率v(A)=0.003 mol·L-1·s-1。,则6s时c(A)= mol·L-1, 若反应经一段时间后,达到平衡时A的转化率为 ,如果这时向该密闭容器中再充入1 mol氩气,平衡时A的转化率为 ;
(3).1200℃时反应C(g)+D(g) 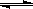 A(g)+B(g)的平衡常数的值为
。
A(g)+B(g)的平衡常数的值为
。
(1) (2)0.022 80% 80%
(3)2.5
(2)0.022 80% 80%
(3)2.5
【解析】试题分析:(1)该反应平衡常数表达式为 。
。
(2)v(A)=△c(A)/t,A浓度变化为0.003×6=0.018mol/L,所以6s时A的物质的量浓度为(0.04-0.018)mol/L=0.022mol/L;设达到平衡时转化的A的物质的量浓度为xmol/L。
A(g) + B(g)  C(g)+D(g)
C(g)+D(g)
始(mol/L)0.04 0.16
平(mol/L)0.04-x 0.16-x x x
830℃时K=1得(0.04-x)(0.16-x) =x·x解得x=0.032。
所以A的转化率为0.032/0.04×100%=80%。若向溶液中再充入氩气,各组分浓度不变,平衡不移动。A的转化率仍为80%。
(3)C(g)+D(g)
 A(g)+B(g)与A(g)+B(g)
A(g)+B(g)与A(g)+B(g)  C(g)+D(g)平衡常数互为倒数,1200℃时反应C(g)+D(g)
C(g)+D(g)平衡常数互为倒数,1200℃时反应C(g)+D(g)  A(g)+B(g)的平衡常数K=1/0.4=2.5。
A(g)+B(g)的平衡常数K=1/0.4=2.5。
考点: 化学平衡常数 转化率 化学反应速率
点评: 反应物、生成物互为颠倒,平衡常数互为倒数。


 长江作业本同步练习册系列答案
长江作业本同步练习册系列答案科目:高中化学 来源:2012-2013学年陕西省三原县北城中学高二第四次月考化学试卷(带解析) 题型:填空题
(10分)已知A(g)+B(g) C(g)+D(g)反应的平衡常数和温度的关系如下:
C(g)+D(g)反应的平衡常数和温度的关系如下:
| |温度/ ℃ | 700 | 900 | 830 | 1000 | 1200 |
| 平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
 A(g)+B(g)的平衡常数的值为 。
A(g)+B(g)的平衡常数的值为 。查看答案和解析>>
科目:高中化学 来源:2011-2012学年湖北省武汉市五校高一下学期期中统考化学试卷(带解析) 题型:计算题
(10分) (1)已知某反应的各物质浓度数据如下:
_ 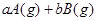

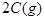
起始浓度(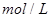 ): 1.5 1.0 0
): 1.5 1.0 0
2s末浓度(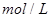 ): 0.9 0.8 0.4
): 0.9 0.8 0.4
则①a= ,b= 。
②2s内B的转化率= 。
(2)由碳棒,铁片和200mL 1.5mol/L的稀硫酸组成的原电池中,当在碳棒上产生气体3.36L(标准状况)时,求
③有 mol电子从 通过电线到 (填“铁片”或“碳棒”)。
④此时溶液中H+的物质的量浓度为 (不考虑溶液体积变化)。
(3)将2.3g金属钠放入足量的m g重水(D2O)中,完全反应后,所得溶液中溶质的质量分数是 (用含m的代数式表示。)
查看答案和解析>>
科目:高中化学 来源:2014届湖北省武汉市五校高一下学期期中统考化学试卷(解析版) 题型:计算题
(10分) (1)已知某反应的各物质浓度数据如下:
_
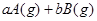

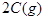
起始浓度(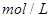 ):
1.5
1.0 0
):
1.5
1.0 0
2s末浓度(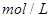 ):
0.9 0.8
0.4
):
0.9 0.8
0.4
则①a= ,b= 。
②2s内B的转化率= 。
(2)由碳棒,铁片和200mL 1.5mol/L的稀硫酸组成的原电池中,当在碳棒上产生气体3.36L(标准状况)时,求
③有 mol电子从 通过电线到 (填“铁片”或“碳棒”) 。
④此时溶液中H+的物质的量浓度为 (不考虑溶液体积变化)。
(3)将2.3g金属钠放入足量的m g重水(D2O)中,完全反应后,所得溶液中溶质的质量分数是 (用含m的代数式表示。)
查看答案和解析>>
科目:高中化学 来源: 题型:
( 10分)已知:
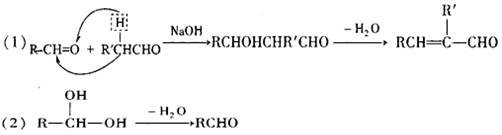
甲苯及其卤代物是有机化工的基本原料,由它出发可制造某些香料、药物及广泛应用于印刷、电子工业中的感光树脂的重要中间体,它们之间的关系如下图所示:
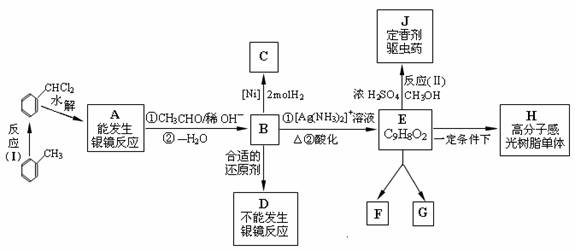
图中 B、D、E 都能使溴水褪色, E 在光等辐射能作用下可以发生二聚加成反应, 生成互为同分异构体的环状化合物 F 和 G; E 还可以在一定条件下形成一种优质高分子感光树脂的单体H。
请回答下面问题:
(1)写出有机物的结构简式: A____ __、C____ ____、D______ ___、E 。
(2)反应(I)的类型是________ ______,反应(II)的类型是______ ________。
(3)完成化学方程式: A→B:___________________ __________________。
(4)同种类、互为同分异构体的 F 和 G 的结构简式为:
F__________________________、G__________ _______________。查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com