
| A. | X和R在同一主族 | |
| B. | 含氧酸酸性:W>R | |
| C. | X与W可以形成酸性氧化物 | |
| D. | X、Z形成的化合物中可能含有共价键 |
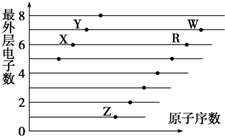
分析 都是短周期元素,由最外层电子数与原子序数关系可知,X、Y处于第二正确,X的最外层电子数为6,故X为O元素,Y的最外层电子数为7,故Y为F元素;Z、R、W处于第三周期,最外层电子数分别为1、6、7,故Z为Na元素、R为S元素、W为Cl元素,据此进行解答.
解答 解:都是短周期元素,由最外层电子数与原子序数关系可知,X、Y处于第二正确,X的最外层电子数为6,故X为O元素,Y的最外层电子数为7,故Y为F元素;Z、S、R、W处于第三周期,最外层电子数分别为1、3、6、7,故Z为Na元素、S为Al、R为S元素、W为Cl元素.
A.氧和硫位于同 一主族,故A正确;
B.含氧酸酸性:W不一定大于R,例如次氯酸的酸性弱于硫酸,故B错误;
C.氧和氯可形成Cl2O5等酸性氧化物,故C正确;
D.氧和钠可形成过氧化钠,过氧化钠中有共价键,故D正确,
故选B.
点评 本题考查结构性质位置关系、元素周期律等,难度不大,根据最外层电子数及原子序数的关系确定元素是解题的关键,注意整体把握元素周期表的结构.


 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C(s)+O2(g)═CO2(g);△H=+393.5kJ•mol-1 | |
| B. | 2SO2+O2═2SO3;△H=-196.6kJ•mol-1 | |
| C. | 2H2(g)+O2(g)═2H2O(l);△H=-571.6KJ | |
| D. | H2(g)+1/2O2(g)═H2O(l);△H=-285.8kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用蒸发的方法使NaCl从溶液中析出时,应将蒸发皿中NaCl溶液小火加热蒸干 | |
| B. | 配制100ml1.00mol/L的NaCl溶液,需用托盘天平准确称量5.9g氯化钠固体 | |
| C. | 利用蒸馏的方法进行乙醇与水的分离时,温度计水银球应放在液面以下来准确测定温度 | |
| D. | 用浓硫酸配制一定物质的量的浓度的稀硫酸时,向浓硫酸中加水稀释,冷却至室温后才能够移到容量瓶 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 71g氯气通入足量水中,反应生成的HClO分子数为NA | |
| B. | 1mol硝基与NA个二氧化氮气体分子所含电子数相等 | |
| C. | 在反应2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2中,每生成1molO2该反应共转移的电子数为6NA | |
| D. | 1L 1mol/LAlCl3溶液中所含阳离子数小于NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com