
| A. | CH2=CH-CH=CH2 | B. | CH2=CH-C≡CH | C. | 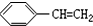 | D. | 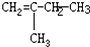 |
分析 在常见的有机化合物中甲烷是正四面体结构,乙烯和苯是平面型结构,乙炔是直线型结构,碳碳单键可以旋转,其它有机物可在此基础上进行判断.
解答 解:A.CH2=CH-CH=CH2相当于两个碳碳双键通过一个碳碳单键相连,所有原子都有可能处于同一平面,故A错误;
B.CH2=CH-C≡CH相当于一个碳碳双键和一个碳碳参键通过一个碳碳单键相连,所有原子都一定处在同一平面上,故B正确;
C. 中相当于苯环与碳碳双键通过一个碳碳单键相连,乙烯和苯是平面型结构,所有原子都有可能处在同一平面上,故C错误;
中相当于苯环与碳碳双键通过一个碳碳单键相连,乙烯和苯是平面型结构,所有原子都有可能处在同一平面上,故C错误;
D.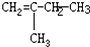 分子中的甲基是和甲烷具有相似的结构为空间四面体,所以原子不可能处于同一平面,故D正确.
分子中的甲基是和甲烷具有相似的结构为空间四面体,所以原子不可能处于同一平面,故D正确.
故选B.
点评 本题考查有机物的空间结构,题目难度不大,注意把握甲烷、乙烯、乙炔和苯的结构特点.


科目:高中化学 来源: 题型:选择题
| A. | H2O比H2S稳定,是因为H2O分子间存在氢键 | |
| B. | P的非金属性强于Si,H3PO4比H2SiO3的酸性强 | |
| C. | 锂所在周期元素最高价氧化物对应的水化物中,酸性最强的是HNO3 | |
| D. | I的原子半径大于Br,HBr比HI的热稳定性强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验目的 | 实验方案 | |
| A | 证明溴乙烷发生消去反应有乙烯生成 | 向试管中加入适量的溴乙烷和NaOH的乙醇溶液,加热,将反应产生的气体通入溴的四氯化碳溶液 |
| B | 证明Mg(OH)2沉淀可以转化为Fe(OH)3沉淀 | 向1mL 1mol/L NaOH溶液中先加入3滴1mol/L MgCl2溶液,再加入3滴1mol/L FeCl3溶液 |
| C | 除去甲烷中的乙烯 | 将混合气通入溴水洗气 |
| D | 探究温度对化学平衡的影响 | 将NO2球浸泡在冷、热水中,观察颜色的变化 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
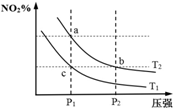 在密闭容器中发生反应N2O4(g)?2NO2(g)△H=+57kJ•mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.下列说法正确的是( )
在密闭容器中发生反应N2O4(g)?2NO2(g)△H=+57kJ•mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.下列说法正确的是( )| A. | 反应温度:T1>T2 | B. | b、c两点的反应速率:v(b)>v(c) | ||
| C. | a、c两点气体的颜色:a浅,c深 | D. | a、b两点的平衡常数:Kb>Ka |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳氢化合物的通式为CnH2n+2 | |
| B. | 石油的主要成分是碳氢化合物 | |
| C. | 乙炔是含碳量最高的碳氢化合物 | |
| D. | 分子式为C4H10的烃有三种同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | a和b不连接时,铁片上会有金属铜析出 | |
| B. | a和b用导线连接时,铜片上发生的反应为:Cu2++2e-═Cu | |
| C. | 无论a和b是否连接,铁片均会溶解,溶液均从蓝色逐渐变成浅绿色 | |
| D. | a和b连接时,铜片上发生氧化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一定含有双键 | B. | 一定含有三键 | ||
| C. | 一定含有不饱和键 | D. | 可能含有苯环 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com