
����Ŀ����ʮ��������ѧ�����߶�̼����������⻯�����˹㷺������о���ȡ����һЩ��Ҫ�ɹ�����֪��C(s)��O2(g)��CO2(g)����H����393 kJ��mol��1
2CO (g)��O2(g)��2CO2(g)����H����566 kJ��mol��1
2H2(g)��O2(g)��2H2O(g)����H����484 kJ��mol��1
��1����ҵ�ϳ����ý�ˮ�����絽���ȵ�̿����ʵ��ú���������Ƶ�CO��H2�����÷�Ӧ���Ȼ�ѧ����ʽ��_______________��
��2������ú��������������̿�㽻�����������ˮ���������������Ŀ����__________�������������ڼ��Ⱥʹ����ºϳ�Һ��ȼ�ϼ״����÷�Ӧ����ʽΪ_______________��
��3�����ӹ�ҵ��ʹ�õ�һ����̼���Լ״�Ϊԭ��ͨ�����⡢�ֽ�������Ӧ�õ���
��һ����2CH3OH(g) === HCOOCH3(g)+2H2(g) ��H>0
�ڶ�����HCOOCH3(g) === CH3OH(g) +CO(g) ��H>0
���Լ״���һ����̼�ķ�ӦΪ___________��Ӧ��������������������������
��4����ѧ���õ����ز�����ͭ��װ��ͼ���˹����ϵͳ�����ø�װ�óɹ���ʵ������
CO2��H2O�ϳ�CH4��
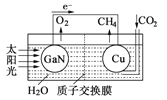
��д��ͭ�缫����ĵ缫��Ӧʽ____________��
��Ϊ��߸��˹����ϵͳ�Ĺ���Ч�ʣ�����װ���м�������___________��ѡ����������������������������
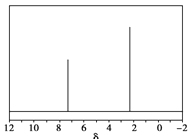
��5����Ȼ��Ҳ��������������ԭ�ϣ������ѧ����������Ȼ��������������÷�����X������������X����Է�������Ϊ106����˴Ź���������ͼ����X�Ľṹ��ʽΪ_____________��
���𰸡�C(s)��H2O(g)= CO (g)��H2(g)����H��+132 kJ��mol��1 �ò���̿ȼ�գ��ṩ̿��ˮ������Ӧ����Ҫ������ CO + 2H2![]() CH3OH ���� CO2��8e����8H����CH4��2H2O ����
CH3OH ���� CO2��8e����8H����CH4��2H2O ���� ![]()
��������
��1����֪����C(s)��O2(g)��CO2(g)����H����393 kJ��mol��1����2CO (g)��O2(g)��2CO2(g)����H����566 kJ��mol��1����2H2(g)��O2(g)��2H2O(g)����H����484 kJ��mol��1�����ݸ�˹���ɣ���-1/2����-1/2���۵�ˮ������̿��Ӧ����CO��H2���Ȼ�ѧ����ʽ��C(s)��H2O(g)="=CO" (g)��H2(g)����H��+132 kJ��mol��1��
��2��ú����Ϊ���ȷ�Ӧ���ʷ�Ӧ����������̿�㽻�����������ˮ���������������Ŀ�����ò���̿ȼ�գ��ṩ̿��ˮ������Ӧ����Ҫ��������CO��H2�ڼ��Ⱥʹ���������Һ��ȼ�ϼ״����÷�Ӧ����ʽΪCO + 2H2![]() CH3OH��
CH3OH��
��3����֪����2CH3OH(g) ==HCOOCH3(g)+2H2(g) ��H>0����HCOOCH3(g) ==CH3OH(g) +CO(g) ��H>0�����ݸ�˹���ɣ���+�ڵ�CH3OH(g) ="=" CO(g)+2H2(g)����H>0�����Լ״���һ����̼�ķ�ӦΪ���ȷ�Ӧ��
��4���������װ��֪��װ��Ϊԭ��أ���ط�ӦΪCO2+2H2O==CH4+2O2��������GaN�缫�����·����ͭ�缫����GaNΪԭ��صĸ�����ͭ�缫Ϊԭ��ص����������ӽ���ĤΪ���ӽ���Ĥ����������ҺΪ������Һ����ͭ�缫Ϊԭ��ص�������������ԭ��Ӧ��CO2�õ������ɼ��飬�����Ϊ������Һ��ͨ�������Ӻ�ˮƽ���ɺ�ԭ�ӣ��缫��ӦʽΪCO2��8e����8H����CH4��2H2O���ڵ����Ϊ������Һ��Ϊ��߸��˹����ϵͳ�Ĺ���Ч�ʣ�����װ���м����������ᡣ
��5��������X����Է�������Ϊ106���������෨�ƶ�X�ķ���ʽΪC8H10����˴Ź���������2���壬X�����к���2����ԭ�ӣ���X�Ľṹ��ʽΪ![]()



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��G��һ���������ϵ���Ҫ�ɷ�֮һ���ϳ�·�����£�

��֪����RCH=CH2+CH2=CHR��![]() CH2=CH2+RCH=CHR��
CH2=CH2+RCH=CHR��
��G�Ľṹ��ʽΪ��
��1��(CH3)2C=CH2��������___��̼ԭ����ͬһƽ���ڡ�
��2��D�����к��еĺ���������������___��F�Ľṹ��ʽΪ___��
��3��A��B�Ļ�ѧ����ʽΪ___����Ӧ����Ϊ___��
��4������C�Ļ�ѧ����ʽΪ___��
��5��ͬʱ��������������D��ͬ���칹���ж��֣����ܷ���������Ӧ������ˮ�⣻�۱�����ֻ��һ��ȡ��������д����������2�����ʵĽṹʽ___��___��
��6������ѧ����֪ʶ�Լ���Ŀ�е������Ϣ��д���ɱ�ϩ��ȡCH2=CHCH=CH2�ĺϳ�·�ߣ����Լ���ѡ����___
���ϳ�·�߳��õı�ʾ��ʽΪ��![]() ��
��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ˮ�帻Ӫ����������ˮ����N��P��Ӫ���κ�������������ˮ����Ⱦ����ȥ��ˮ����N��P�ķ����ܶࡣ
(1)��ѧ������ȥ��ˮ���е�PO![]() �����õĻ�������AlCl3��Ca(OH)2�ȡ�
�����õĻ�������AlCl3��Ca(OH)2�ȡ�
��AlCl3��Һ��Al3+ˮ������ӷ���ʽΪ___��
��Ca5(PO4)3OH��KspΪ6.8��10-37�����ܶȻ���������ʽΪKsp[Ca5(PO4)3OH]=___��
(2)Ϊ̽������ˮ�а�̬��(NH3��N)��PO![]() ͬʱȥ������n(NH4Cl):n(Na2HPO4):n(MgCl2)=1:1:1����ˮ�У�ʵ���ò�ͬpH�£���̬����PO
ͬʱȥ������n(NH4Cl):n(Na2HPO4):n(MgCl2)=1:1:1����ˮ�У�ʵ���ò�ͬpH�£���̬����PO![]() ��ȥ������ͼ(a)��ʾ��
��ȥ������ͼ(a)��ʾ��

��֪��(I)ȥ������Ҫ��ӦΪ��Mg2++NH![]() +HPO
+HPO![]() +6H2O
+6H2O![]() MgNH4PO4��6H2O��+H+��
MgNH4PO4��6H2O��+H+��
(II)����ʱ��Ksp(MgNH4PO4��6H2O)=2.5��10-13��Ksp[Mg(OH)2]=1.8��10-11��Ksp[Mg3(PO4)2]= 6.3��10-31��
��pH��8.5��10.5ʱ����̬����PO![]() ȥ������pH�����������ԭ����___ (��ƽ���ƶ��Ƕ�˵��)��
ȥ������pH�����������ԭ����___ (��ƽ���ƶ��Ƕ�˵��)��
�ڵ�pH��10.5ʱ����̬����PO![]() ȥ������pH�������С����ԭ����___(��ƽ���ƶ��Ƕ�˵��)��
ȥ������pH�������С����ԭ����___(��ƽ���ƶ��Ƕ�˵��)��
(3)һ�ֽ�ûʽSMDDC��ؿ�����ȥ������ˮ����̬������װ����ͼ(b)��ʾ��

��װ�ù���ʱ��H+��___��(�X����Y")��Ǩ�ơ�
��X����(CH2O)n��CO2�ĵ缫��ӦʽΪ___��Y����NO![]() ��N2�ĵ缫��ӦʽΪ___��
��N2�ĵ缫��ӦʽΪ___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ױ�������Ҫ���л�����ԭ�ϣ������������л����ͨ�������������ӡ����������ȱ�������ϩ�ȡ�
��1�����и��������У�����������KMnO4��Һ�������______������ĸ����
a ���ͼױ� b ���ͼ��� c ��ϩ�ͱ� d ��ϩ����Ȳ
��2���ڱ���ȩ�������ܹ�ƽ���ԭ�������______����һ�������£�1 mol����ȩ������������Cu��OH��2��ַ�Ӧ������Cu2O�����ʵ���Ϊ______mol��
��3���Ա�Ϊ��Ҫԭ����ȡ����ϩ�ĺϳ�·������ͼ�ɱ�ʾ���£�

��B�к��������ŵ�������______��
��A��B��C��D�к�������̼ԭ�ӵ���______������ĸ����
��д��C����ᷴӦ������Ӧ���Ļ�ѧ����ʽ��______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ȣ��׳��Ȼ�������SOCl2����һ��Һ̬������е�77�棬��ũҩ����ҩ��ҵ���л��ϳɵ�������;�㷺��ʵ���Һϳ�ԭ����SO2+Cl2+SCl2=2SOCl2������װ����ͼ��ʾ��

��ش��������⣺
��1������c��������_______________��
��2��ʵ�����ö���������Ũ���Ṳ�ȷ�Ӧ�����ӷ���ʽΪ________________________________��
��3��װ��e�в�����Cl2����װ��d��������ϴ��ƿ�������������ƿ����Cl2������һ��ϴ��ƿӦ������Լ���_______________________��
��4������Ӧ������Cl2�����Ϊ896 mL(��ת��Ϊ��״����SO2����)�����õ�������SOCl2 4.76 g����SOCl2�IJ���Ϊ__________��������λ��Ч���֣���
��5�������������õ�SOCl2�м�������NaOH��Һ�������õõ���ɫ��ҺW��������ҺW�д���Cl-�ķ�����_______________________________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ں��º��ݵ��ܱ������У��п��淴Ӧ��![]() �����в���˵����Ӧ�Ѵﵽƽ��״̬���ǣ� ��
�����в���˵����Ӧ�Ѵﵽƽ��״̬���ǣ� ��
A.![]()
B.��Ӧ���е�ѹǿ����ʱ��ı仯���仯
C.����������ɫ���ֲ���
D.��������ƽ����Է����������ֲ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ���ǣ� ��
A.H2(g)+I2(g)![]() 2HI(g)�������������䣬��С��Ӧ������������淴Ӧ���ʲ���
2HI(g)�������������䣬��С��Ӧ������������淴Ӧ���ʲ���
B.C(s)+H2O(g)![]() H2(g)+CO(g)��̼���������ٸı�˵����Ӧ�Ѵ�ƽ��
H2(g)+CO(g)��̼���������ٸı�˵����Ӧ�Ѵ�ƽ��
C.��ѹǿ������ʱ��仯��˵����Ӧ2A(��)+B(g)![]() 2C(��)�Ѵ�ƽ�⣬��A��C����ͬʱ������
2C(��)�Ѵ�ƽ�⣬��A��C����ͬʱ������
D.��ѹ�����·�����ӦN2(g)+3H2(g)![]() 2NH3(g)��������ѹǿ���ٸı�ʱ����Ӧ�ﵽƽ��״̬
2NH3(g)��������ѹǿ���ٸı�ʱ����Ӧ�ﵽƽ��״̬
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪298 Kʱ���ϳɰ���ӦN2(g)��3H2(g)![]() 2NH3(g)����H����92.0 kJ��mol��1�������¶��µ�1 mol N2��3 mol H2����һ�ܱ������У��ڴ�������ʱ���з�Ӧ����÷�Ӧ�ų�������Ϊ(�ٶ�����������û��������ʧ)
2NH3(g)����H����92.0 kJ��mol��1�������¶��µ�1 mol N2��3 mol H2����һ�ܱ������У��ڴ�������ʱ���з�Ӧ����÷�Ӧ�ų�������Ϊ(�ٶ�����������û��������ʧ)
A. һ��С��92.0 kJ B. һ������92.0 kJ
C. һ������92.0 kJ D. ��ȷ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾװ���У��Թ��ڵ�FeI2��Һ�е���KSCN��Һ��ʵ���п���ͨ��Cl2���ٶȣ��Թ����ȹ۲쵽��ɫ����۲쵽��ɫ������˵����ȷ����(����)

A����Cl2�к��϶�HCl��ʵ������л������������
B��ͨ������Cl2�����Թܣ��²����ɫ���ϲ���ɫ
C����ʵ�����֤�����ԣ�Cl2>I2>Fe3��
D���Թ��ڷ�Ӧ�����ӷ���ʽ�ɱ�ʾΪFe2����2I����Cl2=I2��Fe3����2Cl��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com