
| A. | 化学实验基本方法 | B. | 物质的分类 | ||
| C. | 离子反应 | D. | 氧化还原反应 |
 天天向上口算本系列答案
天天向上口算本系列答案科目:高中化学 来源: 题型:选择题
| A. | (NH4)2CO3在室温下就能自发地分解产生氨气是因为生成了易挥发的气体,使体系的熵增大 | |
| B. | 低温更有利于2NO(g)+O2(g)═2NO2(g)的自发进行 | |
| C. | 由于2Na+2H2O=2NaOH+H2↑反应在常温下能自发进行,故该反应一定是放热反应 | |
| D. | 常温下,CO2(g)+C(s)═2CO(g)不能自发进行,则该反应的△H>0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④②③ | B. | ②③④① | C. | ②③①④ | D. | ①④③② |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2A3++2B-═2A2++B2 | B. | C2+2B-═2C-+B2 | ||
| C. | 2A2++C2═2A3++2C- | D. | B2+2C-═C2+2B- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 要完成实验需称取10.6gNa2CO3﹒10H2O晶体 | |
| B. | 本实验需用到的仪器是天平、药匙、玻璃棒、烧杯、100mL容量瓶 | |
| C. | 配制时若容量瓶不干燥,含有少量蒸馏水会导致浓度偏低 | |
| D. | 定容时俯视刻度线会导致浓度偏高 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
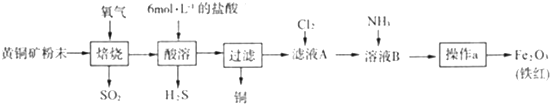
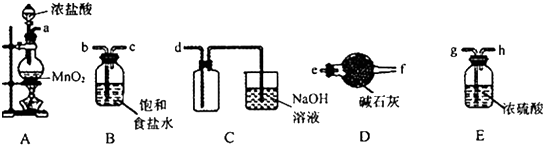
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
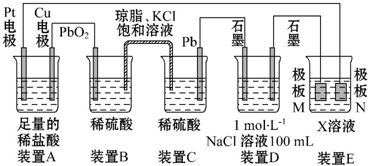
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com