

A.可回收物 B.可堆肥垃圾
C.可燃垃圾 D.有害垃圾
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:058
纯碱中常含有少量的NaCl等杂质,利用下图仪器装置可用来测定纯碱中Na2CO3的质量分数。
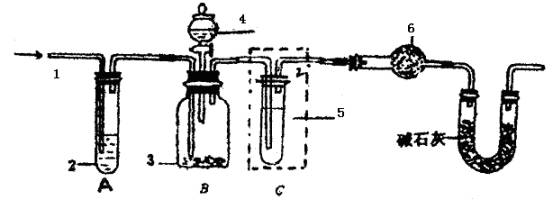
图中:1.空气 2.某溶液 3.纯碱 4.稀硫酸 6.碱石灰
其实验步骤是:
a.按上图所示,组装好实验仪器,并检查其气密性;
b.准确称量盛有碱石灰的干燥管D的质量(设为m1 g);
c.准确称量一定量的纯碱(设为n g);并将其放进广口瓶内;
d.从分液漏斗中缓缓滴入一定量稀硫酸,并从“1”处缓缓鼓入空气,至B反应器中不再产生气体为止。
e.准确称量干燥管D的总质量(设为m2 g)。
根据上述实验,回答下列问题:
(1)该实验进行至操作d时,要缓缓鼓入空气,鼓入空气的作用是 。装置A中盛装的液体“2”应选用 ;装置A的作用是 。如果撤去装置A,直接向装置B中缓缓鼓入空气,则会导致实验测定结果 (填偏大、偏小和不变)。
(2)在空白格内画出装置C及试剂;装置C盛放的试剂“5”是 ;说明装置C的作用是 ;如果撤去装置C,则会导致实验测定结果 。(填偏大、偏小和不变)
(3)根据此实验,计算纯碱中Na2CO3的质量分数的数学式为 (用m1、m2、n表示)。
(4)装置E的作用是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下图中各方框中的字母表示有关的一种反应物或生成物(某些物质略去)其中常温下B、D、G、I、J为气体,其中B可使湿润的红色石蕊试纸变蓝,A~N的所有物质中只有G为单质,其余为化合物。N为不溶于水的无机酸。

回答下列问题:
(1)A的名称为 ,F的化学式是 ;H的化学式是 ,L的化学式是 。
(2)写出实验室制取I的离子方程式:
(3)写出G的一种同素异形体的化学式: 该物质与G在化学性质上的共同点是 。
(4)已知工业上生产0.1molB放出4.62kJ热量,写出该反应的热化学方程式:
(5)在反应C+E→G+F中,每生成1molG转移 mol电子。
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
题目:化学电池在通讯、交通及日常生活中有着广泛的应用。
前常用的镍(Ni)镉(Cd)电池,其电池总反应可以表示为:
Cd+2NiO(OH)+2H2O ![]() 2Ni(OH)2+Cd(OH)2
2Ni(OH)2+Cd(OH)2
(1)已知Ni(OH)2和Cd(OH)2均难溶于水但能溶于酸,放电就是使用电池的过程,充电是给电池补充电量的过程。以下说法中正确的是
① 以上反应不属于置换反应 ② 以上反应是复分解反应
③ 充电时化学能转变为电能 ④ 放电时化学能转变为电能
A.①③ B.②④ C.①④ D.②③
(2)废弃的镍镉电池已成为重要的环境污染物,有资料表明一节废镍锡电池可以使一平方米面积的耕地失去使用价值。在酸性土壤中这种污染尤为严重。这是因为
(3)另一种常用的电池是锂电池(它是一种碱金属元素,其相对原子质量为7,由于它的比容量(单位质量电板材料所能转换的电量)特别大而广泛应用于心脏起搏器,一般使用的时间可长达十年。它的负极用金属锂制成;电池总反应可表示为:Li+MnO2→LiMnO2试回答:锂电池比容量特别大的原因是
锂电池中的电解质溶液需用非水溶剂配制,为什么这种电池不能使用电解质的水溶液?请用化学方程式表示其原因
(4)下图是废弃镍钢电池中的重金属渗入水体后,进入人体的一条途径:
生物体D中重金属浓度 (大于、等于、小于)生物体A中重金属浓度,这是通过食物链 作用所引起的。除上述途径外,被污染水体中的重金属还可以直接通过 (途径)_________进入人体。
(5)下图是两个电池外壳上的说明文字某型号进口电池
某型号进口电池 | 某型号国产电池 |
| GNY 0.6(KR-AA) |
上述进口电池的电动势是 伏。上述国产电池最多可放出 毫安时的电量;若该电池平均工作电流为0.03安,则最多可使用 小时。
查看答案和解析>>
科目:高中化学 来源: 题型:
(I)乙苯的结构简式可以表示为 ,下图是一种形状酷似一条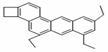 小狗的有机物,化学家Tim Rickard将其取名为“doggycene”。
小狗的有机物,化学家Tim Rickard将其取名为“doggycene”。
doggycene的分子式为 ;
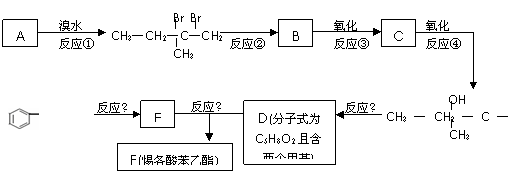
试回答下列问题:
⑴A的结构简式为 ;F的结构简式为 。
⑵反应②中另加的试剂是 ;反应⑤的一般条件是 。
⑶反应③的化学方程式为 。
⑷上述合成路线中属于取代反应的是 (填编号)。
![]()
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
随着人类对温室效应和资源短缺等问题的重视,如何降低大气中CO2的含量及有效地开发利用CO2,引起了各国的普遍重视。
(1)目前,用超临界CO2(其状态介于气态和液态之间)代替氟利昂作冷剂已成为一种趋势,这一做法对环境的积极意义在于 。
(2)将CO2转化成有机物可有效实现碳循环。CO2转化成有机物的例子很多,如:
a.6CO2+6H2O  C6H12O6+6O2 b .CO2+3H2?
C6H12O6+6O2 b .CO2+3H2?  CH3OH+H2O
CH3OH+H2O
c.CO2+CH4  CH3COOH d. 2CO2+6H2
CH3COOH d. 2CO2+6H2  CH2==CH2+4H2O
CH2==CH2+4H2O
以上反应中,最节能的是 ,原子利用率最高的是 。
(3)为探究用CO2来生产燃料甲醇的反应原理,现进行如下实验:
在体积为1L的密闭容器中,充入1molCO2和3molH2,一定条件下发生反应:
CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g)△H=-49.0kJ/mol
CH3OH(g)+H2O(g)△H=-49.0kJ/mol
|
①从反应开始到平衡,氢气的平均反应速率v(H2)= mol/(L·min)
②该反应的平衡常数表达式为 ,升高温度,平衡常数的数值将
(填“增大”、“减小”或“不变”)。
③下列措施中能使n(CH3OH)/n(CO2)增大的是 .
A.升高温度 B.充入He(g),使体系压强增大
C.将H2O(g)从体系中分离 D.再充入1molCO2和3molH2
(4)氢气是合成氨的重要原料,合成氨反应的热化学方程式如下:
N2(g)+3H2(g) ![]() 2NH3(g) △H=-93.4kJ/mol
2NH3(g) △H=-93.4kJ/mol
①当合成氨反应达到平衡后,改变某一外界条件(不改变N2、H2和NH3的量),反应速率与时间的关系如下图所示。
|
图t1时引起平衡移动的条件可能是 。
其中表示平衡混合物中NH3含量最高的一段时间是 。
②温度为T°C时,将3amolH2和amolN2放入带有活塞的密闭容器中,如果活塞能自由移动,充分反应后测得N2的转化率为50%。如果在相同温度下将3amolH2、amolN2和2amolNH3气体放入该容器中,平衡时H2的转化率为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com