
| a | b | ||
| x | y | z |
分析 由五种短周期主族元素的相对位置,可知a、b为第二周期元素,x、y、z为第三周期元素,元素z最外层电子数是其电子层数的2倍,可知z为S元素,结合位置可知y为Si,x为Al,元素y的原子核外电子数是b的2倍,b为N,a为c,以此来解答.
解答 解:由上述分析可知,a为c,b为N,x为Al,y为Si,z为S,
(1)x在周期表中的位置是第三周期第ⅢA族,其单质可采用电解熔融Al2O3的方法制备,故答案为:第三周期第ⅢA族; Al2O3;
(2)x的最高价氧化物的水化物与NaOH溶液反应的离子方程式为Al(OH)3+OH-═AlO2-+2H2O,故答案为:Al(OH)3+OH-═AlO2-+2H2O;
(3)分子(ab)2的结构式为N≡C-C≡N,与NaOH溶液反应的化学方程式为(CN)2+2NaOH═NaCN+NaCNO+H2O,
故答案为:N≡C-C≡N;(CN)2+2NaOH═NaCN+NaCNO+H2O.
点评 本题考查位置、结构与性质,为高频考点,把握元素的位置、性质、元素化合物知识为解答本题的关键,侧重分析与应用能力的考查,注意(3)为解答的难点,题目难度不大.


科目:高中化学 来源: 题型:解答题
| 符合的条件 | 物质的代号 |
| 混合物 | |
| 可以导电的物质 | |
| 非电解质 | |
| 既不是电解质,也不是非电解质 | |
| 强电解质 | |
| 弱电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 16.4mol/L | B. | 17.4mol/L | C. | 18.4mol/L | D. | 19.4mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

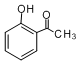 ;②
;②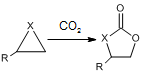 ( X=O,N,S;R为烃基); ③RCOOR+2R′OH→R′COOR′+2ROH
( X=O,N,S;R为烃基); ③RCOOR+2R′OH→R′COOR′+2ROH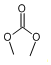 .
.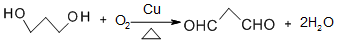 .
.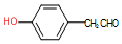 .
.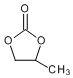 的合成路线.
的合成路线.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| X | Y | |
| Z | W |
| A. | X的氢化物可用作制冷剂 | |
| B. | Y与氢元素形成的物质中只含有极性共价键 | |
| C. | 4种元素的原子半径最大的是W | |
| D. | 4种元素中Z的最高价氧化物对应水化物的酸性最强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
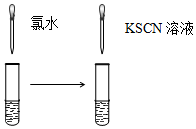
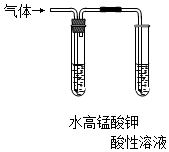
| A.验证FeCl3溶液中是否含有Fe2+ | B.检验溴乙烷消去的产物 |
 |  |
| C.检验氯气与亚硫酸钠是否发生反应 | D.对比Fe3+和Cu2+对H2O2分解的催化效果 |
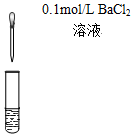 反应后混合液 | 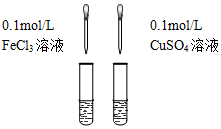 等体积5%的H2O2溶液 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 元素代号 | X | Y | Z | W |
| 原子半径/pm | 66 | 70 | 143 | 160 |
| 主要化合价 | -2 | +5、+3、-3 | +3 | +2 |
| A. | W和Y形成的化合物为共价化合物 | |
| B. | Y的最高价氧化物对应的水化物为强酸 | |
| C. | Y的简单气态氢化物的沸点高于X的简单气态氢化物 | |
| D. | 工业上经常采用电解Z的氯化物溶液制备Z单质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4+、Cl-、Fe3+、K+ | B. | Na+、SO32-、K+、Cl- | ||
| C. | MnO4-、Fe2+、Na+、SO42- | D. | K+、SO42-、HCO3-、Na+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 澄清石灰水与过量碳酸氢钠溶液反应:HCO3-+Ca2++OH-═CaCO3↓+H2O | |
| B. | 硫酸氢钠碳酸氢钠溶液中加入氢氧化钡溶液至中性:H++SO42-+Ba2++OH-═BaSO4↓+2H2O | |
| C. | 向氢氧化钠溶液中通入足量CO2+2OH-+CO2?CO32-+H2O | |
| D. | 向氢氧化钡溶液中加入过量硫酸:2H++SO42-+Ba2++2OH-?BaSO4↓+2H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com