
分析 氯气溶于水发生反应Cl2+H2O?HCl+HClO,新制氯水含有Cl2、H2O、HClO、H+、Cl-等粒子,其中H+可与碳酸钙等物质反应,而Cl2、HClO具有强氧化性,HClO具有漂白性,溶液中含有Cl-可与硝酸银反应生成白色AgCl沉淀,以此解答该题.
解答 解:(1)氯气微溶于水,溶液中存在氯气,且颜色是黄绿色,故答案为:Cl2;
(2)溶液中含有Cl-,Cl-可与硝酸银反应生成白色AgCl沉淀,故答案为:Cl-;
(3)HClO具有漂白性,可使有色物质褪色,故答案为:HClO.
点评 本题综合考查氯气和氯水的性质,注意把握氯气和水反应的特点以及氯水的成分和性质,为高考高频考点,侧重于基础知识的综合运用,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 一定不存在Ba2+,NH4+可能存在 | B. | CO32- 可能存在 | ||
| C. | Na+一定存在 | D. | 一定不存在Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{1}{44}$mol-1 | B. | $\frac{x}{22}$mol-1 | C. | $\frac{3x}{44}$mol-1 | D. | $\frac{44x}{3}$mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
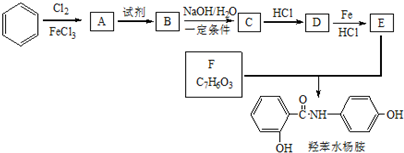
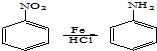
 .
. 、
、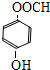 (任意一种).
(任意一种).查看答案和解析>>
科目:高中化学 来源: 题型:填空题
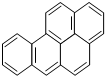 ,它是一种稠环芳香烃,其化学式为C20H12,此物质中碳元素和氢元素的质量比为20:1.
,它是一种稠环芳香烃,其化学式为C20H12,此物质中碳元素和氢元素的质量比为20:1.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用小苏打检验面团发酵产生的酸 | |
| B. | 用碘酒证明马铃薯中含有淀粉 | |
| C. | 用食醋除去热水瓶中的水垢 | |
| D. | 用淀粉直接检验加碘盐中含的碘元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NO3- | B. | Cu2+ | C. | Mg2+ | D. | Ba2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
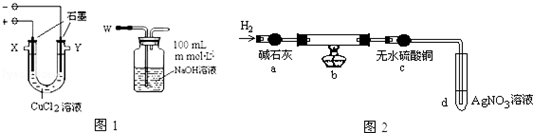
| 物质名称及化学式 | 氯化亚铜CuCl | 碱式氯化铜Cu2(OH)3Cl |
| 性质 | 白色固体、不溶水 | 绿色固体、不溶水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
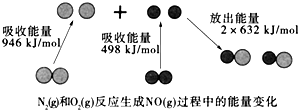
| A. | 该反应的热化学方程式为:N2(g)+O2(g)=2NO(g)△H=+180 kJ•mol-1 | |
| B. | 1 mol N2(l)和NA个 O2(l)反应生成2mol NO(g)时,吸收的能量为180 kJ | |
| C. | 1 mol N2(g)和1 mol O2(g)具有的总能量小于2 mol NO(g)具有的总能量 | |
| D. | 通常情况下,N2(g)和O2(g)混合不能直接生成NO(g) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com