
【题目】下列卤代烃在KOH醇溶液中加热不反应的是
①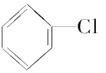 ②
②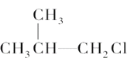 ③(CH3)3C-CH2Cl④CHCl2-CHBr2⑤
③(CH3)3C-CH2Cl④CHCl2-CHBr2⑤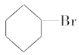 ⑥CH3Cl
⑥CH3Cl
A.②④B.②③⑤C.①③⑥D.全部
 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案科目:高中化学 来源: 题型:
【题目】目前Haber-Bosch法是工业合成氨的主要方式,其生产条件需要高温高压。为了有效降低能耗,过渡金属催化还原氮气合成氨被认为是具有巨大前景的替代方法。催化过程一般有吸附—解离—反应—脱附等过程,图示为N2和H2在固体催化剂表面合成氨反应路径的势能面图(部分数据略),其中“*”表示被催化剂吸附。
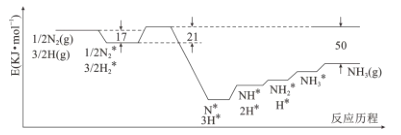
(1)氨气的脱附是____过程(填“吸热”或“放热”),合成氨的热化学方程式为_____
(2)合成氨的捷姆金和佩热夫速率方程式为 w= k1 p(N2)![]() -k2
-k2![]() ,w为反应的瞬时总速率,为正反应和逆反应速率之差,k1、k2是正、逆反应速率常数。合成氨反应N2+3H22NH3的平衡常数Kp=_________(用k1,k2表示)(注:Kp用各物质平衡分压来表示)。
,w为反应的瞬时总速率,为正反应和逆反应速率之差,k1、k2是正、逆反应速率常数。合成氨反应N2+3H22NH3的平衡常数Kp=_________(用k1,k2表示)(注:Kp用各物质平衡分压来表示)。
(3)若将2.0molN2和6.0molH2通入体积为1L的密闭容器中,分别在T1和T2温度下进行反应。曲线A表示T2温度下n(H2)的变化,曲线B表示T1温度下n(NH3)的变化,T2温度下反应到a点恰好达到平衡。
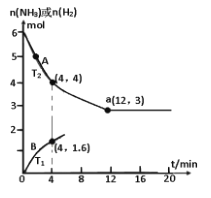
①温度T1___T2 (填“>”、“<”或“=”下同),T1温度下恰好平衡时,曲线B上的点为b(m, n ),则m___12,n__2。
②T2 温度下,反应从开始到恰好平衡时平均速率v(N2) =_____。
③T2温度下,合成氨反应N2+3H22NH3的平衡常数的数值是____;若某时刻,容器内气体的压强为起始时的80%,则此时v(正)____v(逆)(填“>”、“<”或“=”)。
(4)工业上通过降低反应后混合气体的温度而使氨气分离出来。这种分离物质的方法, 其原理类似于下列方法中的___(填序号)。
A.过滤 B.蒸馏 C.渗析 D.萃取
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应。应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”。 请回答该实验中的问题。
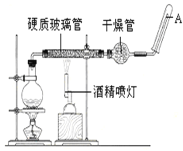
(1)写出该反应的化学方程式____________________。圆底烧瓶中盛装水,烧瓶里应事先放置____,其作用是_____。
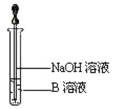
(2)该同学欲确定反应后硬质试管中固体物质的成分,设计了如下实验方案:①待硬质试管冷却后,取少许其中的固体物质溶于稀硫酸得溶液B;②取少量溶液B滴加KSCN溶液,溶液未变红色,该同学马上另取少量溶液B,使其跟NaOH溶液反应。若按图所示的操作,可观察到________________________________________ 的现象,请写出与上述现象相关的反应的化学方程式___________________________ ,____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用如图装置可以验证非金属性的变化规律。
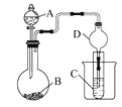
(1)仪器A的名称为________,干燥管D的作用是________________。
(2)已知在常温下,高锰酸钾和浓盐酸反应能生成氯气。实验室中现有药品Na2S溶液、KMnO4、浓盐酸、MnO2,请选择合适药品设计实验验证氯的非金属性大于硫的;装置A、B、C中所装药品分别为________、________、________,装置C中的实验现象为_________________,离子方程式为______。
(3)若要证明非金属性:S>C>Si,则A中加________、B中加Na2CO3、C中加________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.乙醇、乙酸都可以看成是乙烷分子中的氢原子被羟基或羧基取代后的产物
B.下列分子式C2H6O、CF2Cl2、C2H4O2均可表示一种纯净物
C.C4H9OH属于醇的同分异构体的数目与C5H10O2属于羧酸的同分异构体的数目相同
D.有机物![]() 和
和![]() 的一溴取代物的同分异构体数目相同
的一溴取代物的同分异构体数目相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知NA是阿伏加德罗常数的值,下列说法正确的是
A.32 g S8与S6(![]() )的混合物中所含共价键数目为NA
)的混合物中所含共价键数目为NA
B.1 L 0.1 mol·L-1 H2C2O4溶液中含C2O![]() 离子数为0.1NA
离子数为0.1NA
C.2 mol NO与2 mol O2在密闭容器中充分反应,转移的电子数为8NA
D.56g铁片投入足量浓H2SO4中生成NA个SO2分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知![]() ,
,![]() 。若在500℃和催化剂的作用下,反应在容积固定的密闭容器中进行,下列有关说法正确的是
。若在500℃和催化剂的作用下,反应在容积固定的密闭容器中进行,下列有关说法正确的是
A.达到平衡时,![]() 和
和![]() 的浓度一定相等
的浓度一定相等
B.反应体系中,当混合物的密度保持不变,反应达到平衡
C.使用催化剂、增大压强和升高温度均有利于加快反应速率
D.投入![]() 和
和![]() ,达平衡时反应放出热量为198.0 kJ
,达平衡时反应放出热量为198.0 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D、E五种短周期元素,其中D与A、B、C均能形成原子个数比为1∶1与1∶2的两类化合物X、Y,E的某种含氧酸或含氧酸盐在一定条件下可分解生成D的单质。
(1)由上述条件可以确定的元素编号及对应元素名称是____________,其中原子间通过共用一对电子而形成的单质的电子式为________________,E能形成多种含氧酸,其中酸性最强的含氧酸的分子式为______________。
(2)若所有可能的X、Y中,C、D形成的是离子化合物,其中一种物质中含有两类化学键,那么另一种物质的形成过程用电子式可表示为______________________________________。
(3)若上述X、Y存在如下变化:X+Y→Z+D2,且X、Y中各原子(离子)最外层上均有8个电子,则该反应的化学方程式为__________________,反应物中存在非极性键的物质是__________,生成物中存在非极性键的物质是_____________,由此说明化学反应的本质是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是中学化学中常见物质之间的一些反应关系,其中部分产物未写出。常温下X是固体,B和G是液体,其余均为气体。根据下图关系推断:

(1)写出化学式:X_______,A________,B_______。
(2)实验室收集气体D和F的方法依次是_______法、________法。
(3)写出C→E的化学方程式:____________。
(4)请写出A与E反应生成D的化学方程式:_______________
(5)检验物质A的方法和现象是________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com