
【题目】“结晶玫瑰”是具有强烈玫瑰香气的结晶型固体香料,在香料和日用化工产品中具有广阔的应用价值。其化学名称为“乙酸三氯甲基苯甲酯”,目前国内工业上主要使用以下路径来合成结晶玫瑰:
I.由苯甲醛和氯仿合成三氯甲基苯基甲醇。
Ⅱ.三氯甲基苯基甲醇与乙酸酐发生乙酰化反应制得“结晶政瑰”。
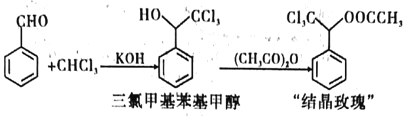
已知:
三氯甲基苯基甲醇 | 相对分子质量:225.5。无色液体。不溶于水,密度比水大,溶于乙醇 |
乙酸酐 | 无色液体。与水反应生成乙酸,溶于乙醇 |
“结晶玫瑰” | 相对分子质量:267.5。白色晶体。熔点:88℃。不溶于水,溶于乙醇 |
具体实验步骤如下:
I.由苯甲醛和氯仿合成三氯甲基苯基甲醇。
步骤一:装置如图所示。依次将苯甲醛、氯仿加入三颈烧瓶中,仪器A中加入KOH和助溶剂。滴加A中试剂并搅拌,开始反应并控制在一定温度下进行。

步骤二:反应结束后,将混合物依次用5%的盐酸、蒸馏水洗涤。
步骤三:将洗涤后的混合物蒸馏,除去其他有机杂质,加无水琉酸镁,过滤。滤液即为粗制三氯甲基萃基甲醇。
Ⅱ.三氯甲基苯基甲醇与乙酸酐发生乙酰化反应制得“结晶玫瑰”。
步骤四:向另一三颈瓶中加入制备的三氯甲基苯基甲醇、乙酸酐,并加入少量浓硫酸催化反应,加热控制反应温度在90℃~110℃之间。
步骤五:反应完毕后,将反应液倒入冰水中,冷却结晶获得“结晶玫瑰”。
请回答下列问题:
(1)仪器A的名称是_________。实验装置B中,冷凝水应从_____口进(填“a”或“b”)。
(2)步骤二中,用5%的盐酸洗涤的主要目的是___________。在洗涤、分液操作中,应充分振荡,然后静置,待分层后有机层应___________ (填序号)。
A.直接从上口倒出
B.先将水层从上口倒出,再将有机层从下口放出
C.直接从下口放出
D.先将水层从下口放出,再将有机层从下口放出
(3)步骤三中,加入无水硫酸镁的目的是___________。若未加入无水硫酸镁,直接将蒸馏所得物质进行后续反应,会使“结晶玫瑰”的产率偏______(填“高”或“低”),其原因是___________ (利用平衡移动原理解释)。(已知Ⅱ的具体反应如图所示)

(4)步骤四中,加料时,应先加入三氯甲基苯基甲醇和乙酸酐,然后慢慢加入浓硫酸并搅拌,主要是为了__________。加热反应时,为较好的控制温度,最适宜的加热方式为_____(填“水浴加热”或“油浴加热”)。
(5)22.55g三氟甲基苯基甲醇与足量乙酸酐充分反应得到结晶玫瑰21.40g,则产率是_____。
【答案】 恒压滴液漏斗 b 除去未反应完的KOH C 除水干燥 低 若不干燥,乙酸酐会与水反应生成乙酸,使“结晶玫瑰”的合成反应平衡逆向移动,产品产率降低 防止放热过快而迸溅 油浴加热 80%
【解析】(1)通过实验装置图可知,仪器A的名称是恒压滴液漏斗,实验装置B中,冷凝水应采用逆流原理,冷凝效果好,所以冷凝水下口进上口出,b口进,正确答案:恒压滴液漏斗;b。
(2)步骤1中加入了氢氧化钾试剂,一部分参与了反应,还会有剩余的KOH,所以步骤2中用5%的盐酸洗涤的主要目的是除去未反应完的KOH;有机物密度比水大,在下层,因此在洗涤、分液操作中,应充分振荡,然后静置,待分层后有机层应直接从下口放出,C操作正确;正确答案:除去未反应完的KOH;C。
(3)无水硫酸镁具有吸水作用,可以做干燥剂,步骤三中,加入无水硫酸镁的目的是除水干燥;根据信息可知,若不干燥,乙酸酐会与水反应生成乙酸,增大乙酸的浓度,使“结晶玫瑰”的合成反应平衡逆向移动,产品产率降低;正确答案:低;若不干燥,乙酸酐会与水反应生成乙酸,使“结晶玫瑰”的合成反应平衡逆向移动,产品产率降低。
(4)浓硫酸溶于水放出大量的热,因此步骤四中,加料时,应先加入三氯甲基苯基甲醇和乙酸酐,然后慢慢加入浓硫酸并搅拌,主要是为了防止放热过快而迸溅;通过题中信息加热控制反应温度在90℃~110℃之间可知,最适宜的加热方式为油浴加热,而水浴加热温度不能超过100℃;正确答案:防止放热过快而迸溅;油浴加热。
(5)根据反应 可知,1mol三氟甲基苯基甲醇充分反应生成结晶玫瑰1mol,22.55g三氟甲基苯基甲醇即为0.1mol,生成结晶玫瑰0.1mol,质量为26.75 g,所以22.55g三氟甲基苯基甲醇与足量乙酸酐充分反应得到结晶玫瑰21.40g,则产率是21.40/26.75×100%=80%,正确答案:80%。
可知,1mol三氟甲基苯基甲醇充分反应生成结晶玫瑰1mol,22.55g三氟甲基苯基甲醇即为0.1mol,生成结晶玫瑰0.1mol,质量为26.75 g,所以22.55g三氟甲基苯基甲醇与足量乙酸酐充分反应得到结晶玫瑰21.40g,则产率是21.40/26.75×100%=80%,正确答案:80%。


 小学课时特训系列答案
小学课时特训系列答案科目:高中化学 来源: 题型:
【题目】中药药剂砒霜(主要成分为As2O3,微溶于水),可用于治疗急性白血病。工业上用含硫化砷(As2S3)的废渣生产砒霜的工艺流程如图所示:

(1)硫化砷中砷元素化合价为__________,其难溶于水,“碱浸”过程中硫元素价态不变,发生的主要反应的离子方程式为________________________。
(2)氧化脱硫过程中被氧化的元素是____________。
(3)还原过程中H3AsO4转化为H3AsO3,反应的化学方程式是____________________。
(4)“沉砷”是在一定温度下将砷元素转化为Ca5(AsO4)3OH沉淀的过程,主要反应有:
a.Ca(OH)2(S)![]() Ca2+(aq) +2OH-(aq) Ksp=10-7
Ca2+(aq) +2OH-(aq) Ksp=10-7
b.Ca5(AsO4)3OH (S)![]() 5Ca2+(aq)+OH-(aq)+3AsO43-(aq) Ksp=10-40
5Ca2+(aq)+OH-(aq)+3AsO43-(aq) Ksp=10-40
加入石灰乳调溶液中c(OH-) =0.01mol L-1,此时溶液中c(AsO43-) =________________。(已知: ![]() =2. 15)
=2. 15)
(5)还原后加热溶液,H3AsO3分解为As2O3,结晶得到粗As2O3。As2O3在不同温度和不同浓度硫酸中的溶解度度(S)曲线如下图所示。

为了提高粗As2O3的沉淀率,“结晶”过程进行的操作是蒸发浓缩,冷却结晶,过滤,洗涤,在此过程中应控制的条件为_________________。
(6)在工业生产中,最后一步所得滤液可循环使用,其目的是____________________。
(7)砷元素广泛存在于自然界,砷与其化合物被运用在农药、除草剂、杀虫剂等。
①砷的常见氧化物有As2O3和As2O5,其中As2O5热稳定性差。根据图1写出As2O5分解为As2O3的热化学方程式___________________________________________。

②砷酸钠具有氧化性,298 K时,在100 mL烧杯中加入10 mL 0.1 mol/L Na3AsO4溶液、20 mL 0.1 mol/L KI溶液和20 mL 0.05 mol/L硫酸溶液,发生下列反应:AsO43-(无色)+2I-+2H+![]() AsO33-(无色)+I2(浅黄色)+H2O ,测得溶液中c(I2)与时间(t)的关系如图2所示(溶液体积变化忽略不计)。下列情况表明上述可逆反应达到平衡状态的是_______(填字母代号)。
AsO33-(无色)+I2(浅黄色)+H2O ,测得溶液中c(I2)与时间(t)的关系如图2所示(溶液体积变化忽略不计)。下列情况表明上述可逆反应达到平衡状态的是_______(填字母代号)。
a.溶液颜色保持不再变化 b.c(AsO33-)+c(AsO43-)不再变化
c.AsO43-的生成速率等于I2的生成速率 d. ![]() 保持不再变化
保持不再变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】纳米铜是一种性能优异的超导材料,以辉铜矿(主要成分为Cu2S)为原料制备纳米铜粉的工艺流程如图1所示。
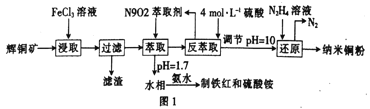
(1)用黄铜矿(主要成分为CuFeS2)、废铜渣和稀硫酸共同作用可获得较纯净的Cu2S,其原理如图2所示,该反应的离子方程式为____________________________。
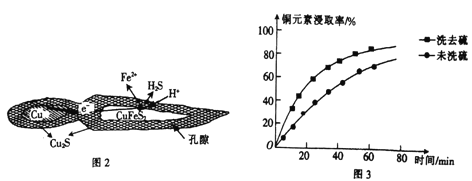
(2)从辉铜矿中浸取铜元素时,可用FeCl 3溶液作浸取剂。
①反应:Cu2S+4FeCl3=2CuCl2+4FeCl下标2+S,每生成1molCuCl2,反应中转移电子的物质的量为_____;浸取时,在有氧环境下可维持Fe3+较高浓度,有关反应的离子方程式为_________。
②浸取过程中加入洗涤剂溶解硫时,铜元素浸取率的变化如图3所示,未洗硫时铜元素浸取率较低,其原因是________________。
(3)“萃取”时,两种金属离子萃取率与pH的关系如图4所示。当pH>1.7时,pH越大,金属离子萃取率越低,其中Fe3+萃取率降低的原因是_________________。

(4)用“反萃取”得到的CuSO4 溶液制备纳米铜粉时,该反应中还原产物与氧化产物的质量之比为_____。
(5)在萃取后的“水相”中加入适量氨水,静置,再经过滤、_____、干燥、____等操作可得到Fe2O3 产品。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A. 用鼻子对着盛有氯气的瓶口,就可以嗅到氯气的气味
B. 用向下排空气法可以收集到纯净的氯气
C. 贮氯罐意外泄漏,应沿逆风方向疏散群众
D. 氯气车间液氯泄漏时,应弯腰逃离氯气泄漏区域
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钼是一种重要的过渡金属元素,通常用作合金及不锈钢的添加剂,可增强合金的强度、硬度、可焊性等。钼酸钠晶体(Na2MoO4·2H2O)可作为无公害型冷却水系统的金属腐蚀抑制剂,如图15是化工生产中以辉钼矿(主要成分为硫化钼MoS2)为原料来制备金属钼、钼酸钠晶体的主要流程图。

回答下列问题:
(1)已知反应③为复分解反应,则钼酸中钥的化合价为___________。
(2)反应⑥的离子方程式为___________。
(3)辉钼矿灼烧时的化学方程式为____________。
(4)操作X为_________。已知钼酸钠在一定温度范围内的析出物质及相应物质的溶解度如下表所示,则在操作X中应控制温度的最佳范围为_______(填序号)。
温度(℃) | 0 | 4 | 9 | 10 | 15.5 | 32 | 51.5 | 100 | >100 |
析出物质 | Na2MoO4·10H2O | Na2MoO4·2H2O | Na2MoO4 | ||||||
溶解度 | 30.63 | 33.85 | 38.16 | 39.28 | 39.27 | 39.82 | 41.27 | 45.57 | |
A.0℃~10℃ B.10℃~100℃ C.15.5℃~50℃ D.100℃以上
(5)制备钼酸钠晶体还可用通过向精制的辉钼矿中直接加入次氯酸钠溶液氧化的方法,若氧化过程中,还有硫酸钠生成,则氧化剂与还原剂的物质的量之比为_________。
(6)Li、MoS2可充电电池的工作原理为xLi+nMoS2![]() Lix(MoS2)n[Lix(MoS2)n附着在电极上],则电池充电时阳极的电极反应式为___________________。
Lix(MoS2)n[Lix(MoS2)n附着在电极上],则电池充电时阳极的电极反应式为___________________。
(7)可用还原性气体(CO和H2)还原MoO3制钼,工业上制备还原性气体CO![]() 2CO+2H2。含甲烷体积分数为90%的7L(标准状况)天然气与足量二氧化碳在高温下反应,甲烷转化率为80%,用产生的CO和H2还原MoO3制钼,理论上能生产钼的质量为_________。
2CO+2H2。含甲烷体积分数为90%的7L(标准状况)天然气与足量二氧化碳在高温下反应,甲烷转化率为80%,用产生的CO和H2还原MoO3制钼,理论上能生产钼的质量为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有下列原子:①12C;②39K;③40Ca;④13C;⑤14N;⑥40Ar。请回答下列问题(填写相应的序号):
(1)互为同位素的是___。
(2)中子数相等,但质子数不相等的是___、___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验现象或事实解释正确的是( )。
选项 | 实验现象或事实 | 解释 |
A | 检验待测液中S | 先滴入盐酸可排除Ag+、C |
B | 制备乙酸乙酯时,导管应伸入试管至饱和Na2CO3溶液的液面上方 | 乙酸乙酯易溶于碳酸钠溶液,防止发生倒吸 |
C | 向Fe(NO3)2溶液中加入稀硫酸,试管口有红棕色气体产生 | 溶液中N |
D | 含Mg(HCO3)2的硬水长时间充分加热,最终得到的沉淀物的主要成分为Mg(OH)2,而不是MgCO3 | Ksp(MgCO3)<Ksp[Mg(OH)2] |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】页岩气是从页岩层中开采的一种非常重要的天然气资源,页岩气的主要成分是甲烷,是公认的洁净能源。
(1)页岩气不仅能用作燃料,还可用于生产合成气(CO和H2)。CH4与H2O(g)通入聚焦太阳能反应器,发生反应CH4(g)+H2O(g) = CO(g)+3H2(g) ΔH1。已知:CH4、H2、CO的燃烧热(ΔH)分别为-a kJ·mol-1、-b kJ·mol-1、-c kJ·mol-1;H2O(l)=H2O(g) ΔH=+d kJ·mol-1。
则ΔH1=______________(用含字母a、b、c、d的代数式表示)kJ·mol-1。
(2)用合成气生成甲醇的反应为CO(g)+2H2(g)![]() CH3OH(g) ΔH2,在10 L恒容密闭容器中按物质的量之比1∶2充入CO和H2,测得CO的平衡转化率与温度和压强的关系如图所示:
CH3OH(g) ΔH2,在10 L恒容密闭容器中按物质的量之比1∶2充入CO和H2,测得CO的平衡转化率与温度和压强的关系如图所示:

200 ℃时n(H2)随时间的变化如下表所示:
t/min | 0 | 1 | 3 | 5 |
n(H2)/mol | 8.0 | 5.4 | 4.0 | 4.0 |
①ΔH2____(填“>”“<”或“=”)0。
②写出两条可同时提高反应速率和CO转化率的措施:_____。
③下列说法正确的是____(填字母)。
a.温度越高,该反应的平衡常数越大
b.达平衡后再充入稀有气体,CO的转化率提高
c.容器内气体压强不再变化时,反应达到最大限度
d.图中压强:p1<p2
④0~3 min内用CH3OH表示的反应速率v(CH3OH)=____mol·L-1·min-1。
⑤200 ℃时,该反应的平衡常数K=____。向上述200 ℃达到平衡的恒容密闭容器中再加入2 mol CO、4 mol H2、2 mol CH3OH,保持温度不变,则化学平衡____(填“正向”“逆向”或“不”)移动。
(3)甲烷、氧气和KOH溶液可组成燃料电池。标准状况下充入5.6 L甲烷,测得电路中转移1.2 mol电子,则甲烷的利用率为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据最新报道,贵州发现超大型锰矿,整个矿区资源量超两亿吨。锰矿是继铁矿、铝矿之后,排在第三位的金属矿产,属国家战略紧铁矿产之一,在电池、磁性新材料等方面都有广泛应用。中国是全球最大的锰矿石和锰系材料生产、清费大国,回答下列问题:
(1)基态锰原子的价层电子排布式为_________。
(2)铜锰氧化物(CuMn2O4) 能在常温下催化氧化空气中的一氧化碳和甲醛(HCHO)。
①CO 和N2 互为等电于体。CO 分子中σ键和π键数目之比为________。
②HCHO分子的H-C-H 键角______(填“大于”“小于”或“等于”)CO2的键角,理由是__________。
③ 向一定物质的量浓度的Cu(NO3)2和Mn(NO3)2溶被中加入Na2CO3溶液,所得沉淀经高温灼烧,可制得CuMn2O4。CO32-的空间构型是____________。
(3)晶体熔点: Fe2O3晶体______Al2O3晶体(填“>”“<”或“=”),理由是___________。
(4)锰、铁的第三电离能(I3) 较大的是_______(填素符号)。
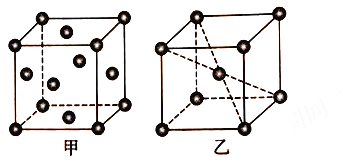
(5) 铝晶胞如图26甲所示。铝晶胞中,铝原子的配位数为________。已知铝的晶体密度为ρ g·cm-3,N A代表阿伏加德罗常数的值,设铝原子的半径为rpm,则r=_______。
(6)锰晶胞如图乙所示。已知锰晶胞参数为a nm。设锰晶胞中两个锰原子核之间最短距离为dnm,则d=_____。锰晶胞中Mn 的空间利用率φ=____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com