
密闭容器左边充入的是体积比为2∶1的NO和H2的混合气体,右边充人的是N2,中间是一个可自由移动的密封隔板,开始时隔板位置如图所示.然后向左边缓缓通入一定量O2,充分反应后,恢复至原来温度,隔板位置位于容器正中间(忽略NO2转化为N2O4的变化),则通入O2的体积与左边原混合气体的体积在同温同压下的比值为________;反应后所得混合气体的平均相对分子质量为________
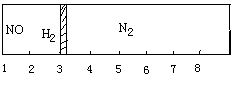
 培优三好生系列答案
培优三好生系列答案科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
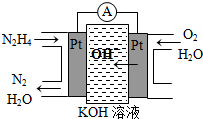 Ⅰ.肼(N2H4)又称联氨,广泛用于火箭推进剂、有机合成及燃料电池,NO2的二聚体N2O4则是火箭中常用氧化剂.试回答下列问题
Ⅰ.肼(N2H4)又称联氨,广泛用于火箭推进剂、有机合成及燃料电池,NO2的二聚体N2O4则是火箭中常用氧化剂.试回答下列问题| 物质 | CO | H2 | CH3OH |
| 浓度(mol?L-1) | 0.9 | 1.0 | 0.6 |
| 2 |
| 3 |
| 2 |
| 3 |
查看答案和解析>>
科目:高中化学 来源:黄冈重点作业 高三化学(下) 题型:022
密闭容器左边充入的是体积比为2∶1的NO和H2的混合气体,右边充人的是N2,中间是一个可自由移动的密封隔板,开始时隔板位置如图所示.然后向左边缓缓通入一定量O2,充分反应后,恢复至原来温度,隔板位置位于容器正中间(忽略NO2转化为N2O4的变化),则通入O2的体积与左边原混合气体的体积在同温同压下的比值为________;反应后所得混合气体的平均相对分子质量为________

查看答案和解析>>
科目:高中化学 来源: 题型:
在一密闭容器中,用一不漏气的滑动活塞隔开,常温时在左边充入3/4体积H2和O2混合气体,在右边充入1/4体积N2。若将左边混合气体点燃充分反应后恢复到原温,活塞停留在中间,则反应前混合气体中H2和O2的体积比可能是
A.7:2 B.4:5 C.5:4 D.2:7
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com