
| A. | 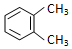 与 与 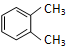 是同一种物质,说明苯分子中碳碳双键、碳碳单键交替排列 是同一种物质,说明苯分子中碳碳双键、碳碳单键交替排列 | |
| B. | 苯在空气中不易燃烧完全,燃烧时冒浓烟,说明苯组成中含碳量较高 | |
| C. | 煤干馏得到的煤焦油可以分离出苯,苯是无色无味的液态烃 | |
| D. | 向2mL苯中加入1mL溴的四氯化碳溶液,振荡后静置,可观察到液体分层,上层呈橙红色 |
分析 A.如果苯分子中碳碳双键、碳碳单键交替排列,则邻二取代物有两种;
B.烃分子中含碳量越高,燃烧越不充分,产生烟越浓;
C.苯具有芳香气味;
D.四氯化碳与苯互溶.
解答 解:A. 和
和 是同一种物质,说明苯分子中不是碳碳双键、碳碳单键交替排列,故A错误;
是同一种物质,说明苯分子中不是碳碳双键、碳碳单键交替排列,故A错误;
B.苯的分子式为C6H6,含碳量大,不易燃烧完全,燃烧时冒浓烟,故B正确;
C.苯具有芳香气味,为液体烃,故C错误;
D.四氯化碳与苯互溶,向2mL苯中加入1mL溴的四氯化碳溶液,振荡后静置,溶液不分层,故D错误;
故选:B.
点评 本题考查有机物的结构和性质,为高频考点,侧重学生的分析能力的考查,注意把握苯的结构和性质特殊性,难度不大,注意相关基础知识的积累.


 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电子由Zn电极流出,经KOH溶液流向正极 | |
| B. | 正极反应式为2FeO42-+10H++6e-=Fe2O3+5H2O | |
| C. | 该电池放电过程中电解质溶液浓度不变 | |
| D. | 电池工作时OH-向负极迁移 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
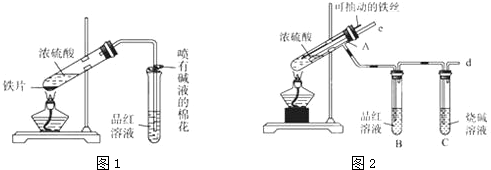
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H+、Ca2+、Cl-、CO32- | B. | Cl-、ClO-、K+、H+ | ||
| C. | Na+、Fe3+、SO42-、OH- | D. | Na+、Cu2+、Cl-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
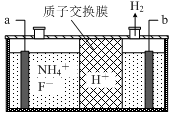 在微电子工业中NF3常用作氮化硅的蚀刻剂,工业上通过电解含NH4F等的无水熔融物生产NF3,其电解原理如图所示.
在微电子工业中NF3常用作氮化硅的蚀刻剂,工业上通过电解含NH4F等的无水熔融物生产NF3,其电解原理如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com