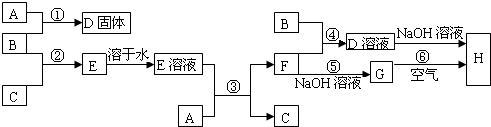
解:由B为黄绿色气体且为单质,可知B为Cl
2;由框图可知反应生成的固体D为固体单质A与Cl
2反应生成的一种氯化物;反应生成的E为Cl
2与气体单质C生成的一种可溶于水的氯化物,且E溶液和固体单质A又可以重新生成气体C和F,只有当C为H
2,F为一种氯化物时才能满足这一过程;而A与Cl
2反应已生成了一种氯化物D,F又是一种氯化物,所以A为变价金属,应为Fe,所以A为Fe,B为Cl
2,C为H
2,D为FeCl
3,E为HCl,F为FeCl
2,G为Fe(OH)
2,H为Fe(OH)
3,
(1)实验室制取B为Cl
2的化学方程式为:MnO
2+4HCl

MnCl
2+Cl
2↑+2H
2O;
故答案为:MnO
2+4HCl

MnCl
2+Cl
2↑+2H
2O;
(2)D中阳离子为Fe
3+,F中阳离子为Fe
2+,区别离子的方法是:溶液的颜色,三价铁离子溶液为黄色溶液,亚铁离子溶液为浅绿色溶液;或利用硫氰酸钾溶液遇到三价铁离子会生成血红色硫氰酸铁溶液,故答案为:取D、F少量溶液于试管中,分别加入KSCN溶液,溶液变血红色,证明是三价铁离子;
(3)G→H为Fe(OH)
2和O
2反应生成Fe(OH)
3的反应,反应的化学方程式为4Fe(OH)
2+O
2+2H
2O=4Fe(OH)
3,
故答案为:4Fe(OH)
2+O
2+2H
2O=4Fe(OH)
3;
(3)B+F→D的反应为Cl
2和FeCl
2生成FeCl
3的反应,反应的离子方程式为2Fe
2++Cl
2=2Fe
3++2Cl
-,
故答案为:2Fe
2++Cl
2=2Fe
3++2Cl
-;
(4)依据判断出的物质和转化关系分析,元素化合价变化的为氧化还原反应,A+B=D,B+C=E,E+A=F,B+F=D都是氧化还原反应,故答案为:4;
分析:由B为黄绿色气体且为单质,可知B为Cl
2;由框图可知反应生成的固体D为固体单质A与Cl
2反应生成的一种氯化物;反应生成的E为Cl
2与气体单质C生成的一种可溶于水的氯化物,且E溶液和固体单质A又可以重新生成气体C和F,只有当C为H
2,F为一种氯化物时才能满足这一过程;而A与Cl
2反应已生成了一种氯化物D,F又是一种氯化物,所以A为变价金属,应为Fe,所以A为Fe,B为Cl
2,C为H
2,D为FeCl
3,E为HCl,F为FeCl
2,G为Fe(OH)
2,H为Fe(OH)
3,根据对应物质的性质解答该题.
点评:本题考查无机物的推断,主要考查了铁及其化合物性质的应用,题目难度中等,本题注意推断Fe为解答该题的关键,从化合价变化的角度分析氧化还原反应.


 MnCl2+Cl2↑+2H2O;
MnCl2+Cl2↑+2H2O; MnCl2+Cl2↑+2H2O;
MnCl2+Cl2↑+2H2O;