




 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案科目:高中化学 来源:不详 题型:单选题
| A.未加入稀盐酸之前:c(HCN)>c(Na+)>c( CN-) >c(OH-)>c(H+) |
| B.加稀盐酸后溶液中c(CN-)+c(HCN)= c(Na+) |
| C.pH=7时,溶液中:c( Na+)=" c(" CN-) |
| D.加稀盐酸后H2O的电离程度减小 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.稀氨水 | B.氢氧化钠 | C.碳酸镁 | D.碳酸钠 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.与水反应有乙炔生成 | B.与水反应有Mg(OH)2生成 |
| C.有C-C键 | D.有C22-离子 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.ROH是一种强碱 |
| B.等物质的量浓度的MOH与盐酸反应,所得溶液呈中性,则MOH的体积大于盐酸的体积 |
| C.在x点,c(M+)=c(R+) |
| D.稀释前,c(ROH)=10 c(MOH) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
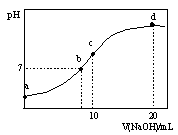
| A.点a所示溶液中:c(NH4+)>c(SO42-)>c(H+)>c(OH-) |
| B.点b所示溶液中:c(NH4+)=c(Na+)>c(H+)=c(OH-) |
| C.点c所示溶液中:c(SO42-)+ c(H+)= c(NH3·H2O )+ c(OH-) |
| D.点d所示溶液中:c(SO42-)>c(NH3·H2O )>c(OH-)>c(NH4+) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.c(NH4+)+c(H+)=c(OH-)+c(Cl-) |
| B.c(NH4+)+c(NH3·H2O)=2c(Cl-) |
| C.2c(OH-)—2c(H+)=c(NH4+)—c(NH3·H2O) |
| D.c(H+)=c(NH3·H2O)+c(OH-) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①④ | B.②③④ | C.②③ | D.①②③④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com