
在标准状况下,相同质量的下列气体,占有体积由大到小的顺序是
① Cl2 ② H2 ③ N2 ④ CO2 ⑤ O2
A.③ ② ④ ⑤ ① B.③ ② ④ ③ ①
② ④ ③ ①
C.① ④ ⑤ ② ③ D.② ③ ⑤ ④ ①
 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案科目:高中化学 来源:2016-2017学年遵义市高二上学期期中考试化学(文)试卷 题型:选择题
下列关于油脂的叙述中,不正确的是
A.油脂属于酯类
B.油脂没有固定的熔沸点
C.油脂是高级脂肪酸的甘油酯
D.油 脂都不能使溴水褪色
脂都不能使溴水褪色
查看答案和解析>>
科目:高中化学 来源:2016-2017学年遵义市高二上学期期中考试(理科)化学试卷 题型:选择题
已知:C(s)+CO2(g) 2CO(g)△H>0。该反应的达到平衡后,下列条件
2CO(g)△H>0。该反应的达到平衡后,下列条件
有利于反应向正方向进行的是
A.升高温度和 减小压强
减小压强
B.降低温度和减小压强
C.降低温度和增大压强
D.升高温度和增大压强
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山东省高一10月月考化学试卷(解析版) 题型:实验题
某同学按下图进行实验,在A中放的是干燥的红色布条,在B中放的是湿润的红色布条,在C中盛放的是氢氧化钠溶液,回答下列问题
①A中现象是 B中现象是
②结论是
③若C中盛有的是混有酚酞溶液的氢氧化钠溶液,当通入一定量的氯气时溶液红色褪去,有同学说红色消失的原因有两种可能,请你帮他写出哪两种可能?
a
b
请设计实验证明哪种可能正确
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山东省高一10月月考化学试卷(解析版) 题型:选择题
有0.1 mol Na2O和 Na2O2的混合物,溶于水后刚好被100 g 7.3﹪的盐酸中和,则混合物中Na2O和 Na2O2的物质的量之比为
A.11﹕1 B.2﹕1 C.3﹕4 D.任意比
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山东省高一10月月考化学试卷(解析版) 题型:选择题
现有盐酸、氯化钠、氢氧化钠和氯水四种溶液,可用来区别他们的一种试剂是
A.AgNO3 B.酚酞试剂 C.紫色石蕊溶液 D.饱和食盐水
查看答案和解析>>
科目:高中化学 来源:2017届安徽省高三上第二次月考化学试卷(解析版) 题型:实验题
某化学小组探究酸性条件下NO3-、SO42-、Fe3+三种微粒的氧化性强弱,设计如下实验(夹持仪器已略去,装置的气密性已检验)。(忽略氧气对反应的影响)
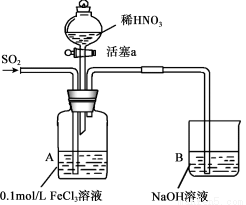
实验记录如下:
实验序号 | 实验操作 | 实验现象 |
I | 向A装置中通入一段时间的SO2气体。 | A中黄色溶液迅速变成深红棕色,最终变为浅绿色。 |
II | 取出少量A装置中的溶液,先加入KSCN溶液,再加入BaCl2溶液。 | 加入KSCN溶液后溶液不变色,再加入BaCl2溶液产生白色沉淀。 |
III | 打开活塞a,将过量稀HNO3加入装置A中,关闭活塞a | A中浅绿色溶液最终变为黄色。 |
IV | 取出少量A装置中的溶液,加入KSCN溶液;向A装置中通入空气。 | 溶液变为红色;液面上方有少量红棕色气体生成。 |
请回答下列问题:
(1)配制FeCl3溶液时,常常加入盐酸,目的是(用化学方程式和简单文字叙述): 。
(2)资料表明,Fe3+能与SO2结合形成深红棕色物质Fe(SO2)63+,反应方程式为: Fe3+ + 6SO2  Fe(SO2)63+。请用化学平衡移动原理解释实验I中溶液颜色变化的原因 。
Fe(SO2)63+。请用化学平衡移动原理解释实验I中溶液颜色变化的原因 。
(3)实验II中发生反应的离子方程式是 。
(4)实验III中,浅绿色溶液变为黄色的原因是(用离子方程式表示) 。
(5)实验IV中液面上方有少量红棕色气体生成,发生反应的方程式是 。
(6)综合上述实验得出的结论是:在酸性条件下,NO3-、SO42-、Fe3+三种微粒的氧化性由强到弱的顺序是: 。
查看答案和解析>>
科目:高中化学 来源:2017届安徽省高三上第二次月考化学试卷(解析版) 题型:选择题
下列有关化学用语表示正确的是( )
A.二氧化硅的分子式 SiO2
B.质子数为53,中子数为78的碘原子 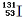
C.羟基的电子式 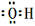
D.次氯酸的结构式:H﹣Cl﹣O
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省成都市高二10月阶段性考试化学试卷 题型:选择题
NA为阿伏加德罗常数,下列叙述错误的是
A. 28gC2H4和C4H8混合气体中含有氢原子总数为4NA
B. 常温常压下,Cu-Zn原电池中,正极产生1.12LH2时,转移的电子数应小于0.1NA
C. 15g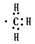 含有的电子数为9NA
含有的电子数为9NA
D. 2.1gDTO中所含中子数为NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com