
| A. | 可使石蕊试液褪色 | B. | 与足量的NaOH溶液反应生成Na2SO4 | ||
| C. | 不能与过氧化氢(H2O2)溶液反应 | D. | 能使品红褪色,加热后又出现红色 |
分析 A.二氧化硫具有漂白性,但不能漂白酸碱指示剂;
B.二氧化硫属于酸性氧化物,能和碱反应生成亚硫酸盐;
C.二氧化硫具有还原性,能被氧化剂氧化;
D.二氧化硫和有色物质反应生成无色物质而具有漂白性,但漂白性不稳定.
解答 解:A.二氧化硫具有漂白性,但不能漂白酸碱指示剂,二氧化硫和水反应生成亚硫酸,亚硫酸电离出氢离子而导致溶液呈酸性,所以二氧化硫能使石蕊试液变红色但不褪色,故A错误;
B.二氧化硫属于酸性氧化物,能和NaOH反应生成Na2SO3,不发生氧化还原反应,故B错误;
C.二氧化硫具有还原性,能被氧化剂双氧水氧化,所以二氧化硫能和双氧水反应,故C错误;
D.二氧化硫和有色物质反应生成无色物质而具有漂白性,但漂白性不稳定,加热后易复原,故D正确;
故选D.
点评 本题考查二氧化硫的漂白性、还原性,二氧化硫中S元素化合价处于中间价态,导致二氧化硫具有氧化性、还原性,注意二氧化硫和次氯酸漂白性原理的区别,易错选项是A,题目难度不大.


科目:高中化学 来源: 题型:选择题
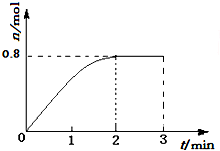 一定条件下,将3molA和1molB两种气体混合于固定容积为2L的密闭容器中,发生如下反应:3A(g)+B(g)?C(g)+2D(s).2min末该反应达到平衡,生成D的物质的量如图.下列判断正确的是( )
一定条件下,将3molA和1molB两种气体混合于固定容积为2L的密闭容器中,发生如下反应:3A(g)+B(g)?C(g)+2D(s).2min末该反应达到平衡,生成D的物质的量如图.下列判断正确的是( )| A. | 若混合气体的密度不再改变时,该反应不一定达到平衡状态 | |
| B. | 2min后,加压会使正反应速率加快,逆反应速率变慢,平衡正向移动 | |
| C. | 反应过程中A和B的转化率之比为3:1 | |
| D. | 该条件下此反应的化学平衡常数的数值约为0.91 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
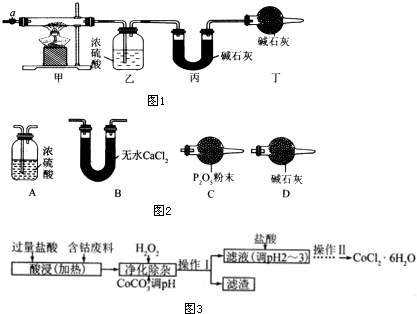
| 乙装置的质量/g | 丙装置的质量/g | |
| 加热前 | 80.00 | 62.00 |
| 加热后 | 80.36 | 62.88 |
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 |
| 开始沉淀(pH) | 2.3 | 7.5 | 7.6 | 3.4 |
| 完全沉淀(pH) | 4.1 | 9.7 | 9.2 | 5.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | BaSO3和BaSO4 | B. | BaS | C. | BaSO3 | D. | BaSO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| A元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素. |
| B元素原子的核外p电子数比s电子数少1. |
| C原子的第一至第四电离能分别是:I1=738kJ/mol I2=1451J/mol I3=7733kJ/mol I4=10540kJ/mol |
| D原子核外所有p轨道全满或半满. |
| E元素的主族序数与周期数的差为4. |
| F是前四周期中电负性最小的元素. |
| G在周期表的第七列. |
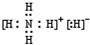 .
. ,该同学所画的电子排布图违背了泡利原理.
,该同学所画的电子排布图违背了泡利原理.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com